- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Хроматин и репарация
Содержание
- 2. Хроматин – участник ДНК репарацииРепарация ДНК в
- 3. Хроматин – участник ДНК репарацииКроме того, хроматин
- 4. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновНа
- 5. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистонов
- 6. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновБолее
- 7. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновКонсервативный
- 8. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновСразу
- 9. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистонов«Фокус»
- 10. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновКроме
- 11. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновФосфорилирование
- 12. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновMRN
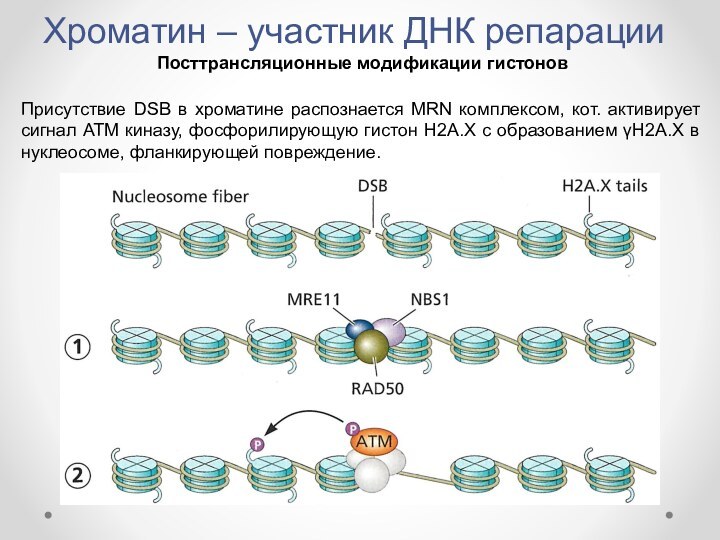
- 13. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновПрисутствие
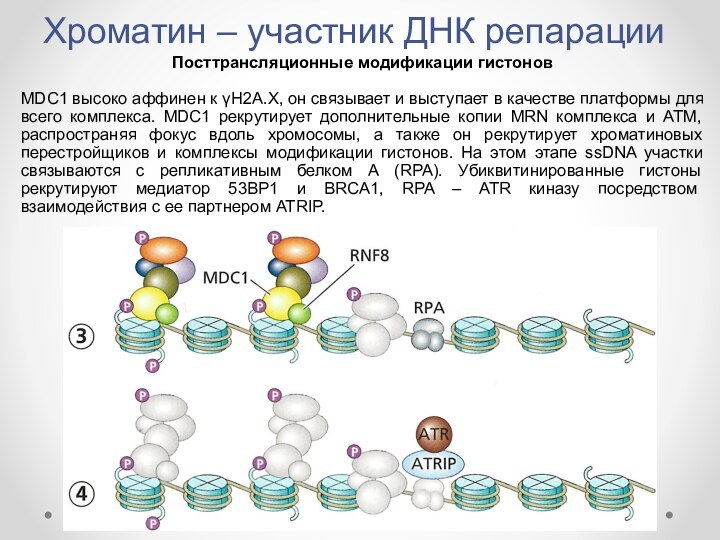
- 14. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновMDC1
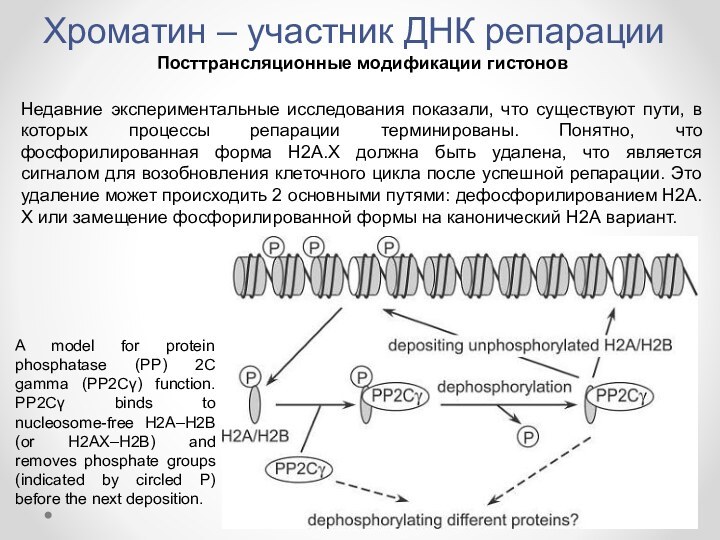
- 15. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновНедавние
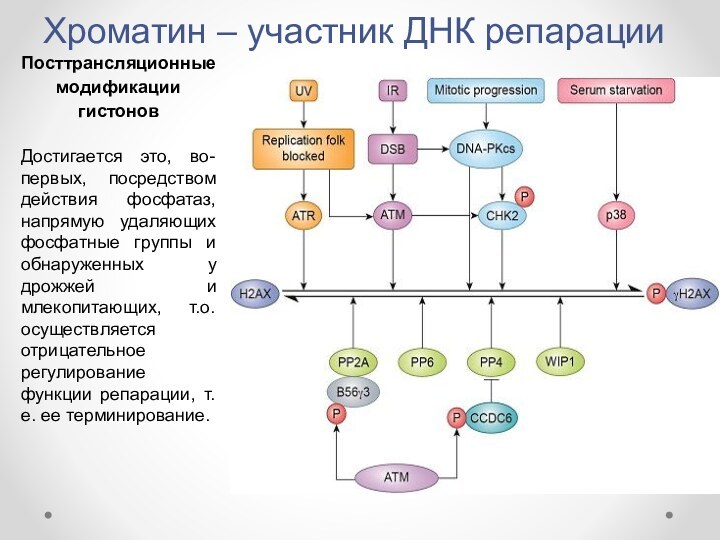
- 16. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновДостигается
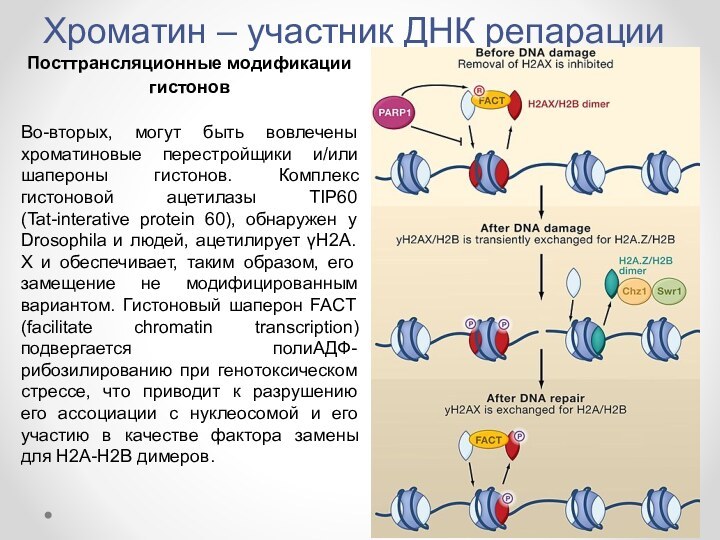
- 17. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновВо-вторых,
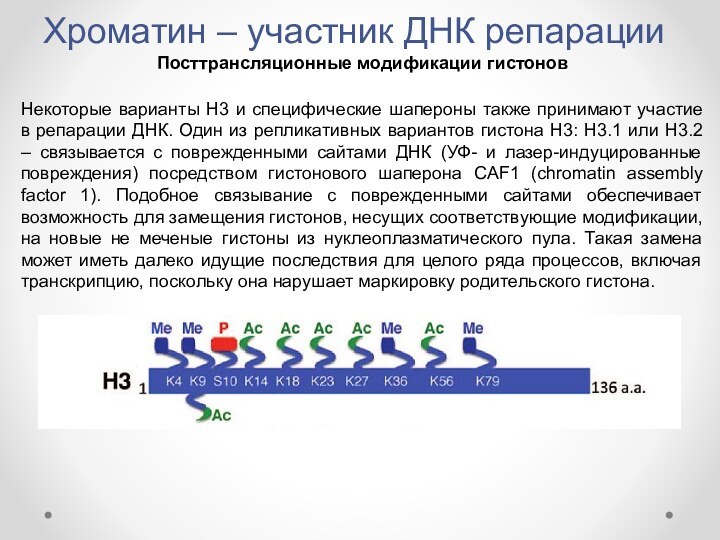
- 18. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновНекоторые
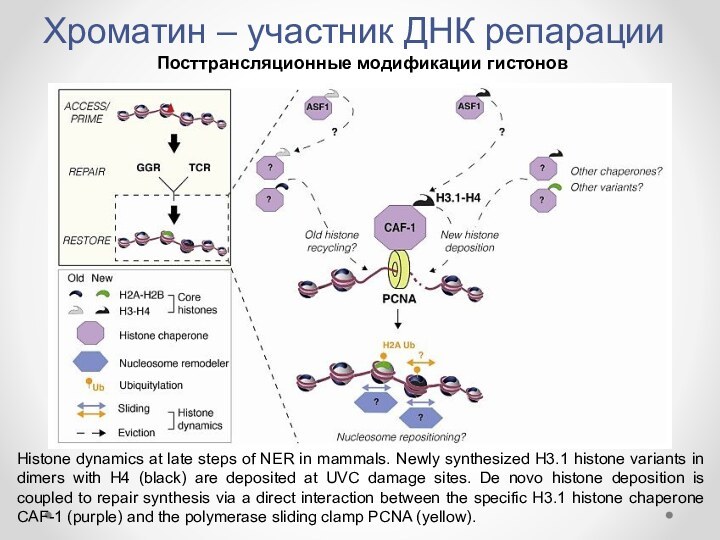
- 19. Хроматин – участник ДНК репарацииПосттрансляционные модификации гистоновHistone
- 20. Скачать презентацию
- 21. Похожие презентации
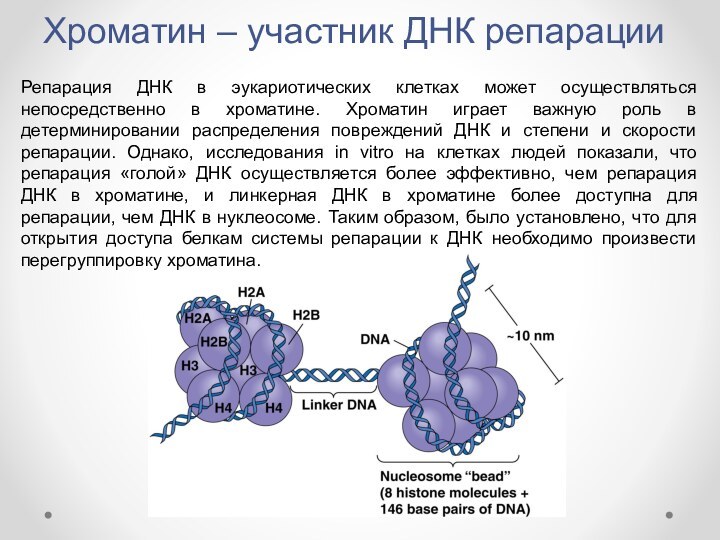
Хроматин – участник ДНК репарацииРепарация ДНК в эукариотических клетках может осуществляться непосредственно в хроматине. Хроматин играет важную роль в детерминировании распределения повреждений ДНК и степени и скорости репарации. Однако, исследования in vitro на клетках людей показали,







Слайд 3
Хроматин – участник ДНК репарации
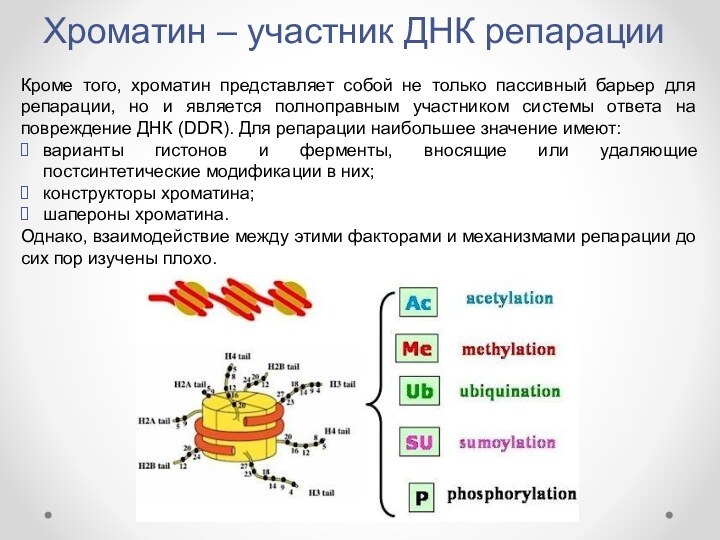
Кроме того, хроматин представляет
собой не только пассивный барьер для репарации, но и
является полноправным участником системы ответа на повреждение ДНК (DDR). Для репарации наибольшее значение имеют:варианты гистонов и ферменты, вносящие или удаляющие постсинтетические модификации в них;
конструкторы хроматина;
шапероны хроматина.
Однако, взаимодействие между этими факторами и механизмами репарации до сих пор изучены плохо.
Слайд 4
Хроматин – участник ДНК репарации
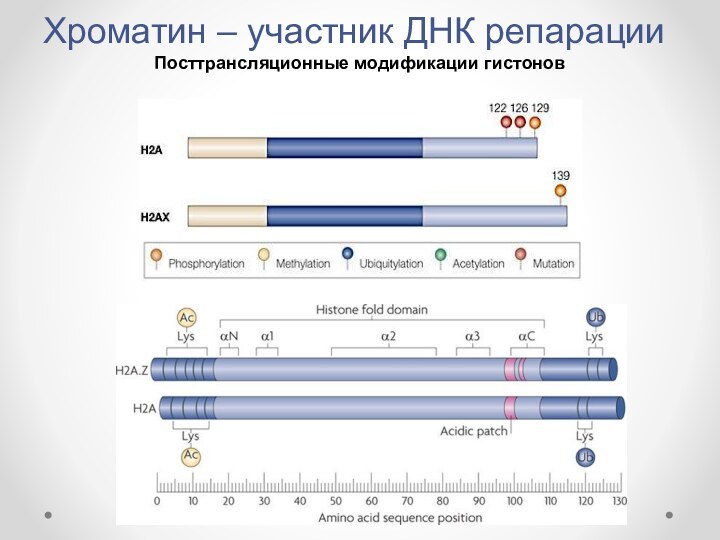
Посттрансляционные модификации гистонов
На сегодняшний
день известно, что три варианта гистона Н2А принимает активное
участие в репарации: Н2А.Х, H2A.Z и макроН2А.
Слайд 6
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
Более подробно
рассмотрим участие H2A.X и его фосфорилированый вариант γH2A.X.
Фосфорилирование
С-конца гистона H2A.X является одной самых первых стадий, происходящих при репарации двухцепочечных разрывов. H2A.X содержит коровую высоко-консервативную для всех H2A вариантов последовательность и короткий консервативный 4-АК-тный хвост, соединенный с кором посредством линкера вариабельной длины.
Слайд 7
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
Консервативный С-конец
выступает из частицы нуклеосомного кора рядом с точкой входа/выхода
ДНК. При этом относительное содержание гистонов у млекопитающих варьирует в зависимости от типа клеток, но в 30-нм фибрилле хроматина одна молекула гистона Н2А.Х может присутствовать в каждой пятой нуклеосоме. У дрожжей Н2А.Х является наиболее распространненным вариантом Н2А и составляет примерно 90% от всех гистонов Н2А. Фосфорилирование серина на С-конце приводит к появлению γH2A.X, не являющегося необходимым компонентом репарации двухцепочечных разрывов, что было показано на примере Н2А.Х-нокаутных мышей, сохраняющих жизнеспособность. Однако, присутствие данного аврианата гистона увеличивает начальную скорость репарации и может увеличивать точность этой репарации.
Слайд 8
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
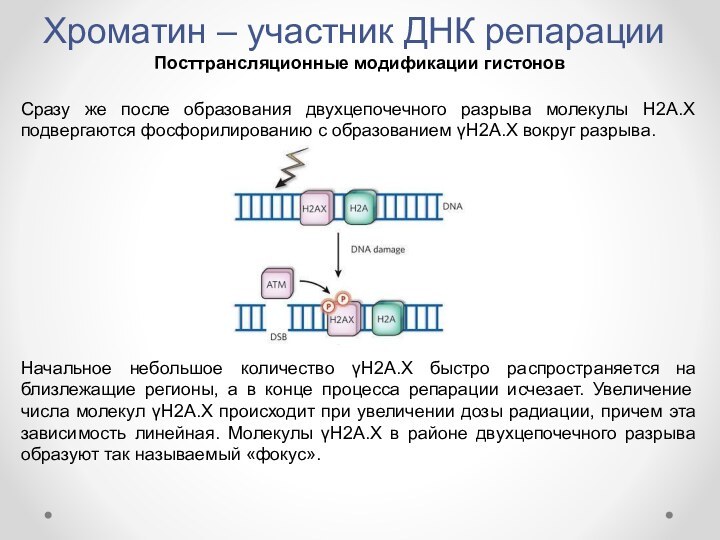
Сразу же
после образования двухцепочечного разрыва молекулы Н2А.Х подвергаются фосфорилированию с
образованием γН2А.Х вокруг разрыва.Начальное небольшое количество γН2А.Х быстро распространяется на близлежащие регионы, а в конце процесса репарации исчезает. Увеличение числа молекул γН2А.Х происходит при увеличении дозы радиации, причем эта зависимость линейная. Молекулы γН2А.Х в районе двухцепочечного разрыва образуют так называемый «фокус».
Слайд 9
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
«Фокус» представляет
собой большую структуру, образующуюся в течение нескольких минут после
облучения радиацией на каждом сайте, содержащем двухцепочечный разрыв. Обычно в клетках человека около 10% гистонов Н2А представлено Н2А.Х, таким образом, локус размером 40 Мб будет содержать примерно 40 000 молекул Н2А.Х, 10% из которых, по-видимому, фосфорилируются в любой момент времени. В теории около 200 «фокусов» покрывают геном человека.«Фокус» также содержит мириады белков, участвующих в ДНК репарации, и хроматин ремоделирующих факторов, которые рекрутируются к сайту с повреждением посредством прямых или непрямых взаимодействий с фосфорилированным γ эпитопом.
Слайд 10
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
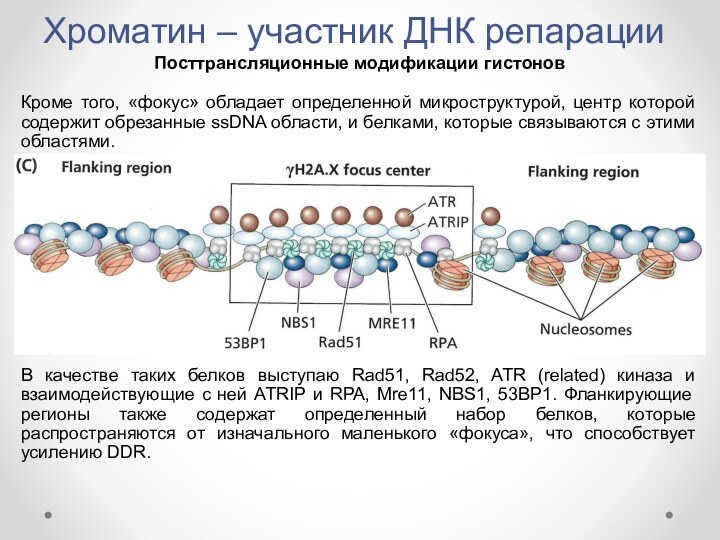
Кроме того,
«фокус» обладает определенной микроструктурой, центр которой содержит обрезанные ssDNA
области, и белками, которые связываются с этими областями.В качестве таких белков выступаю Rad51, Rad52, ATR (related) киназа и взаимодействующие с ней ATRIP и RPA, Mre11, NBS1, 53BP1. Фланкирующие регионы также содержат определенный набор белков, которые распространяются от изначального маленького «фокуса», что способствует усилению DDR.
Слайд 11
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
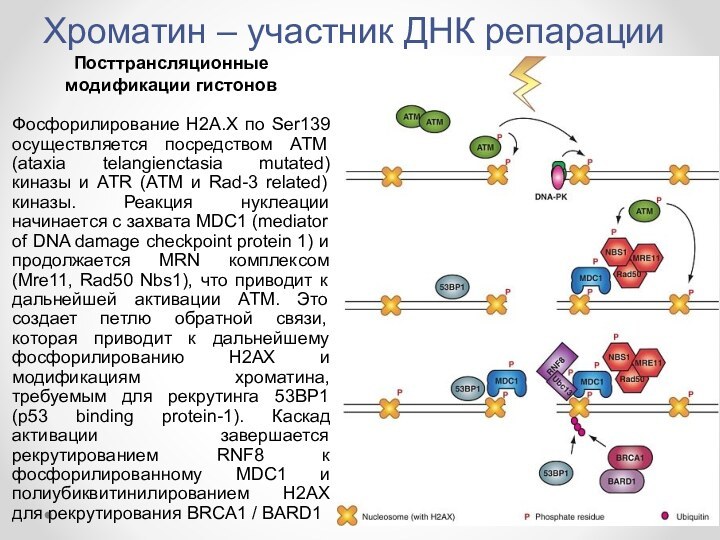
Фосфорилирование H2A.X
по Ser139 осуществляется посредством ATM (ataxia telangienctasia mutated) киназы
и ATR (ATM и Rad-3 related) киназы. Реакция нуклеации начинается с захвата MDC1 (mediator of DNA damage checkpoint protein 1) и продолжается MRN комплексом (Mre11, Rad50 Nbs1), что приводит к дальнейшей активации ATM. Это создает петлю обратной связи, которая приводит к дальнейшему фосфорилированию H2AX и модификациям хроматина, требуемым для рекрутинга 53BP1 (p53 binding protein-1). Каскад активации завершается рекрутированием RNF8 к фосфорилированному MDC1 и полиубиквитинилированием H2AX для рекрутирования BRCA1 / BARD1
Слайд 12
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
MRN комплекс,
медиатор MDC1, 53BP1 и BRCA1 обнаружены в центральном регионе,
однако, они могут также распространяться от физического разрыва на расстояния вплоть до Мб. Поведение белков в этих «фокусах» меняется зависимости от клеточного цикла: некоторые белки, в том числе Mre11, NBS1 и 53BP1 диссоциируют в фазе G2 и почти отсутствуют в метафазе, их структура восстанавливается в G1 фазе; другие белки такие, как MDC1 и BLM остаются в «фокусах» в течение всего клеточного цикла.Более того, «фокусы» γН2А.Х могут образовываться на поврежденных теломерах или в раковых клетках. При этом количество и размер фокусов γН2А.Х в раковых клетках очень вариабельны.
Таким образом, γН2А.Х может рассматриваться как первый элемент, обеспечивающий платформу для сборки функционального комплекса репарации и хроматиновых перестройщиков, необходимых для открытия структуры хроматина для начала репарации.
Слайд 13
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
Присутствие DSB
в хроматине распознается MRN комплексом, кот. активирует сигнал ATM
киназу, фосфорилирующую гистон Н2А.Х с образованием γН2А.Х в нуклеосоме, фланкирующей повреждение.
Слайд 14
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
MDC1 высоко
аффинен к γН2А.Х, он связывает и выступает в качестве
платформы для всего комплекса. MDC1 рекрутирует дополнительные копии MRN комплекса и ATM, распространяя фокус вдоль хромосомы, а также он рекрутирует хроматиновых перестройщиков и комплексы модификации гистонов. На этом этапе ssDNA участки связываются с репликативным белком А (RPA). Убиквитинированные гистоны рекрутируют медиатор 53ВР1 и BRCA1, RPA – ATR киназу посредством взаимодействия с ее партнером ATRIP.
Слайд 15
Хроматин – участник ДНК репарации
Посттрансляционные модификации гистонов
Недавние экспериментальные
исследования показали, что существуют пути, в которых процессы репарации
терминированы. Понятно, что фосфорилированная форма Н2А.Х должна быть удалена, что является сигналом для возобновления клеточного цикла после успешной репарации. Это удаление может происходить 2 основными путями: дефосфорилированием Н2А.Х или замещение фосфорилированной формы на канонический Н2А вариант.A model for protein phosphatase (PP) 2C gamma (PP2Cγ) function. PP2Cγ binds to nucleosome-free H2A–H2B (or H2AX–H2B) and removes phosphate groups (indicated by circled P) before the next deposition.