(1901-94 гг)
Первые исследования по применению квантовой механики к
теории химической связиМетод валентных связей, теория резонанса
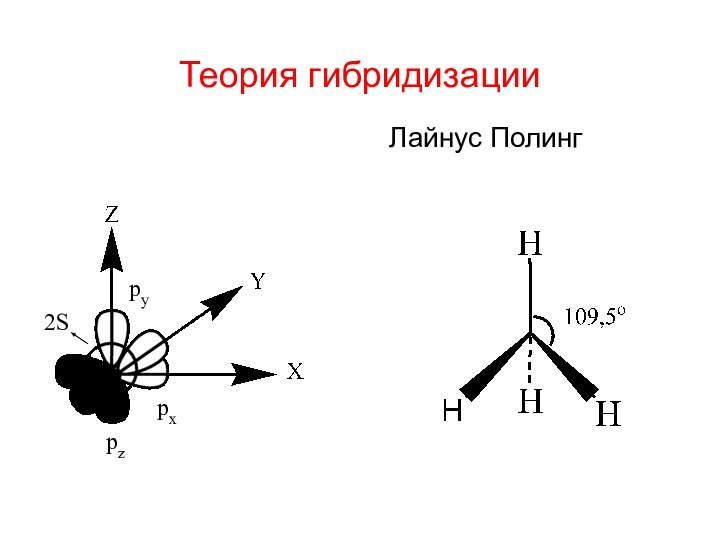
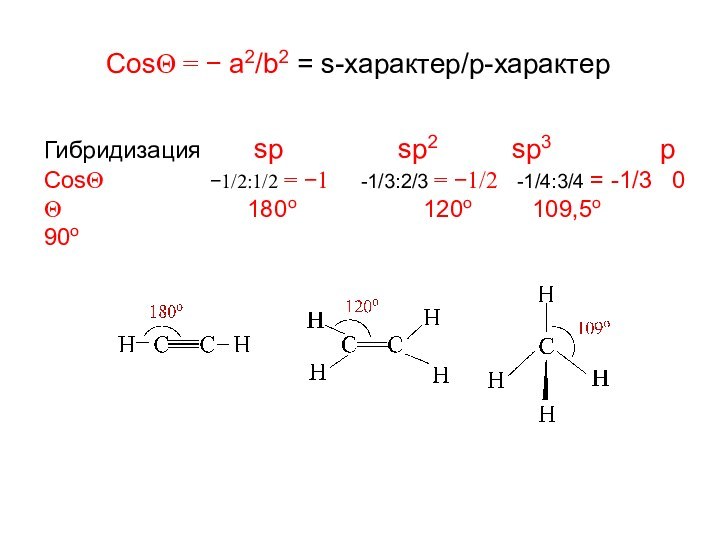
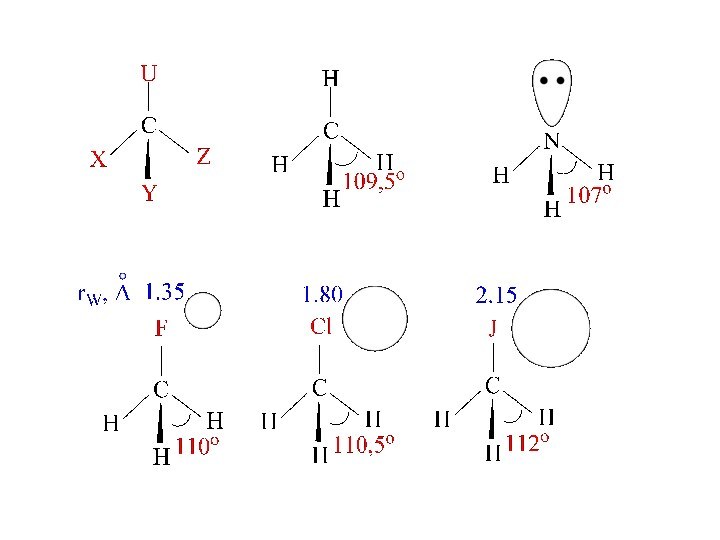
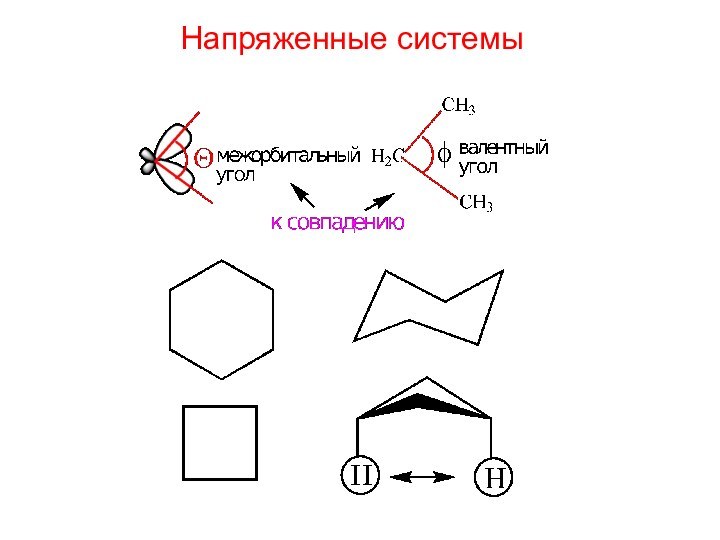
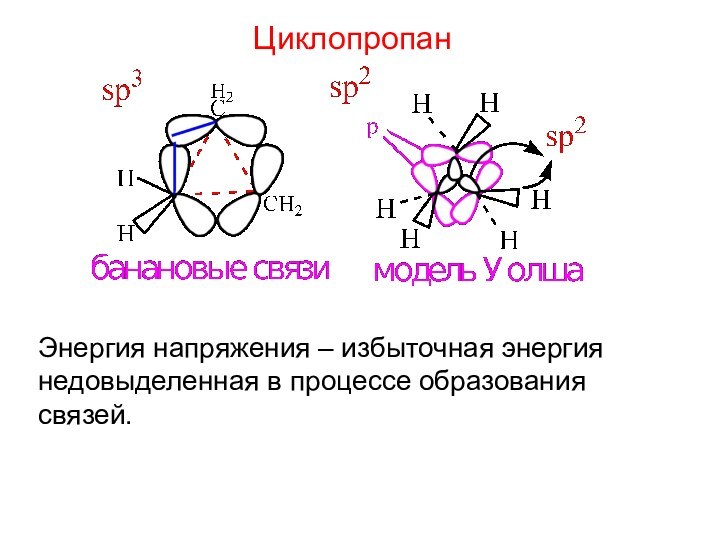
Теория гибридизации
Электроотрицательность атомов
Биохимические исследования
Нобелевская премия по химии (1954 г.)
Нобелевская премия мира (1962 г.) – Пагуошское
движение, против испытаний атомного оружия (11024 ученых)