задачи урока.
Цель урока: выяснить почему соли являются производными кислот
и оснований.
Задачи урока:
1.Дать определение солей.
2. Рассмотреть состав и название солей.
3. Продолжить обучение школьников определять степени окисления в сложных соединениях.
4. Научить, составлять формулы солей.
5. Познакомить учащихся с классификацией солей.
6. Познакомить с некоторыми свойства солей.
Слайд 3
Вопросы
4. Что такое кислоты?
1. Какие классы веществ
вы знаете?
2. Что такое оксиды?
3. Что такое основания?
5. Что
такое основные оксиды, кислотные оксиды, амфотерные?
Слайд 4
NO
HNO
NaOH
HNO
2
3
К какому
классу соединений относятся вещества, дать им названия
Слайд 5
CO
2
2
H CO
Mg(OH)
2
3
H SO
2
3
H SO
2
4
К
какому классу соединений относятся вещества, дать им названия
Слайд 6
ТЕСТ
1. Определите ряд формул состоящих только из:
кислотных оксидов ( I вариант)
основных оксидов: (II вариант)
а) Na2 O, N2O, CuO;
б) CO2, P2O5, Cl2O7;
в) MgO, BaO, K2O;
г) Li2O, CaO, CO.
ТЕСТ
2.
Выберите из списка веществ формулы: только кислот (I вариант), формулы только оснований (II вариант):
а) НСI, AICI3, CO2, H2SO4
б) H2SO4, HCI, HNO3, HF
в) NaOH, BaCI2, CO, Ca(OH)2
г) AI(OH)3, NaOH, KOH, Ba(OH)2
ТЕСТ
3. Выберите формулу оксида
серы (IV) – I вариант
Выберите формулу оксида углерода (II) –
II вариант:
а)H2S б) CO в) HNO3 г) ZnO д) SO2
ТЕСТ
4. * Выберите формулу серной кислоты
–
I вариант
* Выберите формулу сернистой кислоты –
II вариант
а) H2SiO3 б) H2SO4 в) H2SO3 г) H2S
ТЕСТ
5. * Выберите формулу гидроксида
калия –
I вариант
* Выберите формулу гидроксида кальция -
II вариант
а) Ba(OH)2, б) NaOH в) KOH г) Ca(OH)2
ТЕСТ
6. * Выберите формулы растворимого в
воде основания – I вариант
* Выберите формулы нерастворимого в воде основания – II вариант
а)Cu(OH)2 б) KOH в) LiOH г) AI(OH)3
ТЕСТ
7. * Выберите формулы, в
которых
лакмус меняет свой цвет
на красный – I вариант
* Выберите формулы, в которых лакмус меняет свой цвет на синий – II вариант
а) НСI б) H2SO4 в) NaOH г) KOH
к тесту.
I вариант
II вариант
1. б 1. в
2. б 2. г
3. д 3. б
4. б 4. в
5. в 5. г
6. б, в 6. а, г
7. а, б 7. в, г
Слайд 14
Критерии оценивая.
Оценка «5» -
одна ошибка
Оценка «4» - две ошибки
Оценка «3» - три
ошибки
Оценка «2» - четыре ошибки и больше.
Выберите формулы
веществ, которые вам не известны.
Na2SO4 HCI CO2
K2S H2SO4
AI2O3 ВаCl2 KOH
СОЛИ
Чем объединены и чем отличаются перечисленные
соединения:
Na2SO4 K2S ВаCl2
Cu(NO3)2 CaSiO3
K3PO4
СОЛИ
Слайд 17
Cоли – это сложные
вещества, состоящие из атомов металла
и кислотного остатка.
СОЛИ
Соли
С уверенностью можно
сказать, что, по крайней мере, одно химическое соединение в довольно чистом виде имеется в каждом доме, в каждой семье. Это – поваренная соль или как ее называют химики – хлорид натрия NaCl.
Соли
Гипс – кристаллогидрат сульфата кальция
СаSO4 * 2H2O
Соли
Из мрамора (СаСО3) сделан дворец в Индии
Тадж- Махал
Соли
Кристаллогидрат сульфата меди (II)
СuSO4* 5H2O
Безводный
сульфат меди(II)
Соли
* Кристаллогидрат железа или железный купорос
FeSO4* 7H2O
* Сульфат магния
–горькая английская соль
MgSO4
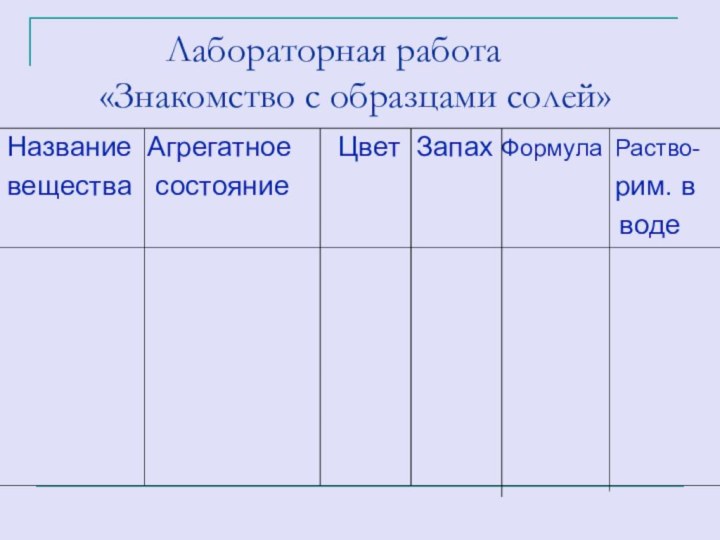
работа
«Знакомство с образцами солей»
Название Агрегатное
Цвет Запах Формула Раство-
вещества состояние рим. в
воде
Слайд 26
Составить формулу сульфата алюминия:
Составьте формулы:
сульфата натрия,
сульфата
кальция,
сульфата железа(III).
Al
2
+
SO
4
3
(
)
3
2
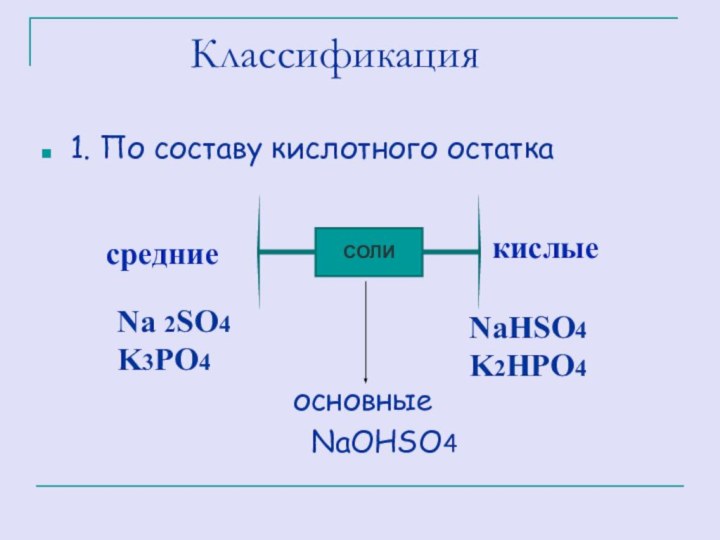
По составу кислотного остатка
основные
NaOHSO4
СОЛИ
средние
кислые
Na 2SO4
K3PO4
NaHSO4
K2HPO4
Классификация
2.
По растворимости
растворимые нерастворимые
в воде в воде
Na2SO4 AgCI
KNO3 BaSO4
Слайд 29
ЗАКРЕПЛЕНИЕ
1. Что такое соли?
2. Дать названия веществам: Ca(NO3)2,
K2SO3, Li2CO3, CuSO4. Определить растворимость этих веществ.
3. Составить формулы
солей: нитрита магния, силиката натрия, фосфата кальция.