- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по теме Алюминий
Содержание
- 2. Периодическая система химических элементов Д.И.Менделеева Группы элементов IIIIIIIVVIIVIVVIII321456712345678910sdp
- 3. Периодическая система химических элементов Д.И.Менделеева Группы элементов IIIIIIIVVIIVIVVIII321456712345678910Характеристика Подробнее
- 4. Алюминий 2. Электронное строение
- 5. Алюминий 1. Из истории открытияглавная ДалееВпервые Al
- 6. Алюминий 1. Из истории открытияГлавная Далее
- 7. Алюминий главнаяВставьте пропущенные словаАлюминий - элемент
- 8. Алюминий 2. Электронное строение27Аl+1302e8e3e1s22s22p63s23p1Краткая электронная запись1s22s22p63s23p1Порядок заполненияглавнаяДалее
- 9. Алюминий 3.Строение простого вещества Металл
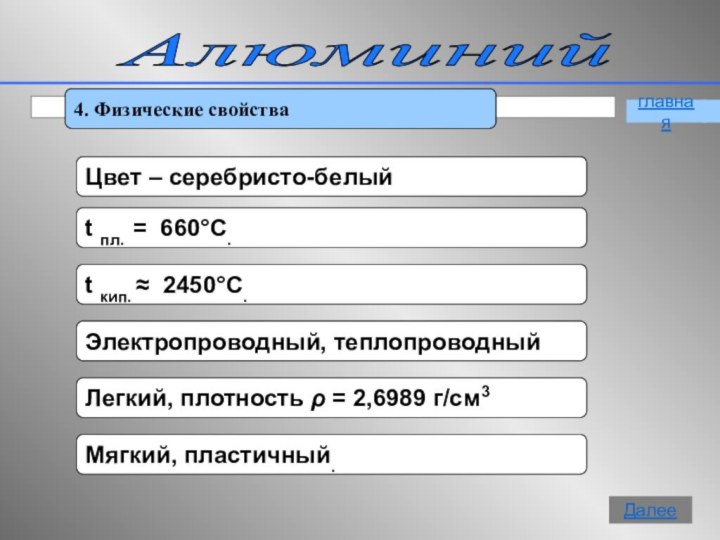
- 10. Алюминий 4. Физические свойстваглавнаяДалее
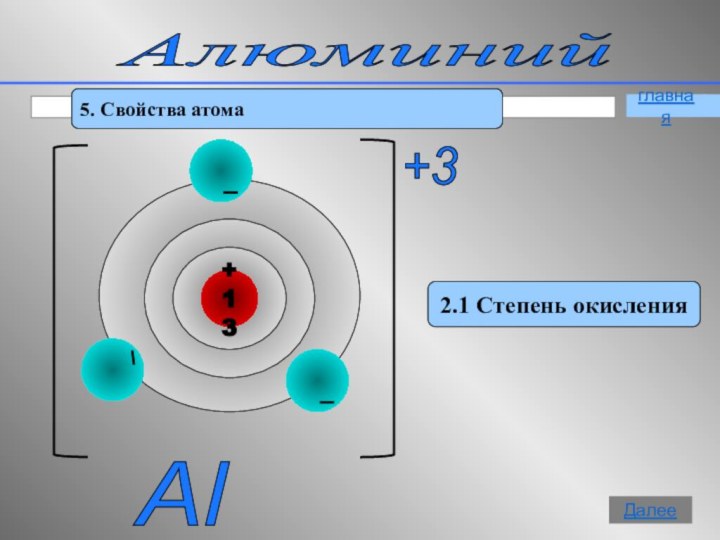
- 11. Алюминий 5. Свойства атома2.1 Степень окисленияAl +3 главнаяДалее
- 12. Алюминий 5. Свойства атома2.2 ВосстановительныеЭлектрохимический ряд напряжений
- 13. Алюминий 6. Химические свойства4Аl + 3O2 =
- 14. Алюминий 7. Содержание в земной кореглавнаяДалее
- 15. Алюминий 7. Нахождение в природеглавнаяДалее
- 16. Алюминий 8. ПолучениеглглаглавнаяДалее
- 17. Скачать презентацию
- 18. Похожие презентации












Слайд 2
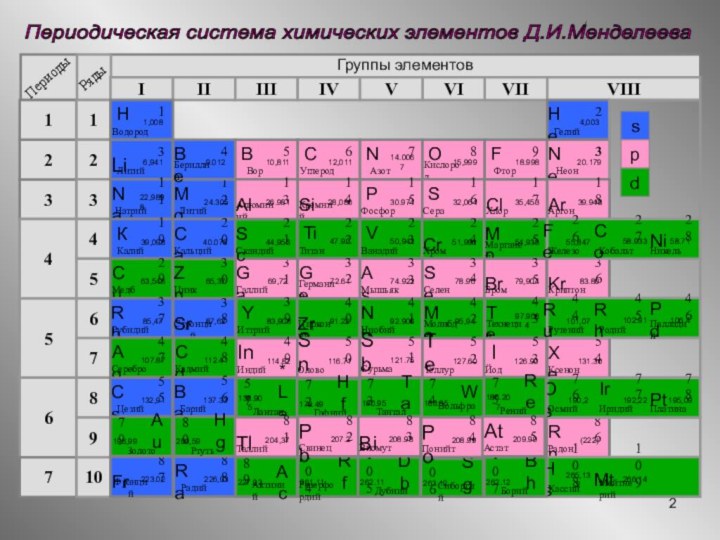
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
II
III
IV
VII
VI
V
VIII
3
2
1
4
5
6
7
1
2
3
4
5
6
7
8
9
10
s
d
p
Слайд 3
Периодическая система химических элементов Д.И.Менделеева
Группы элементов
I
II
III
IV
VII
VI
V
VIII
3
2
1
4
5
6
7
1
2
3
4
5
6
7
8
9
10
Характеристика
Слайд 4
Алюминий
2. Электронное строение
5.
Свойства атома
3. Строение простого вещества
4.
Физические свойства 6. Химические свойства
7. Нахождение в природе
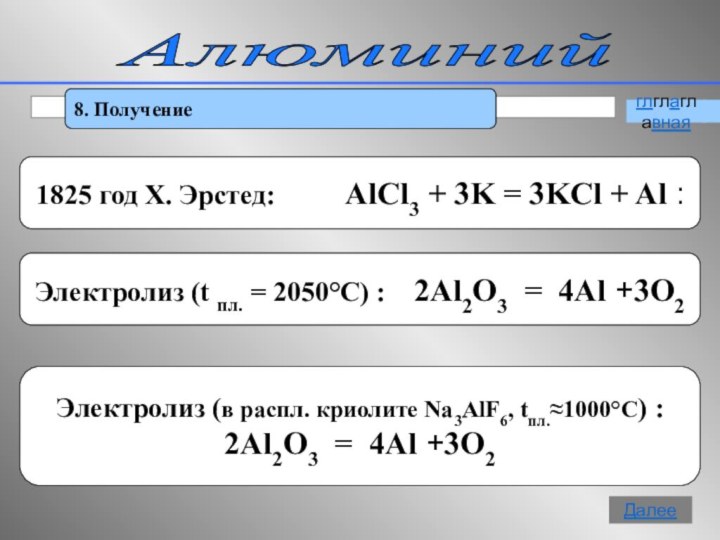
8. Получение
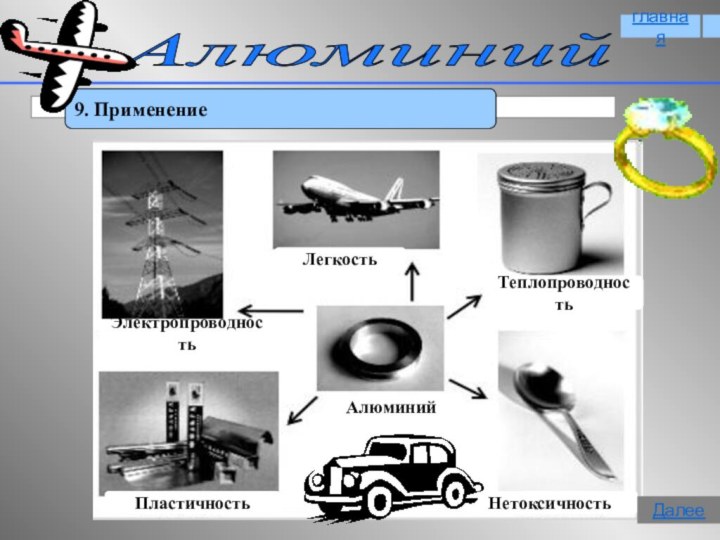
9. Применение
1. Из истории открытия
Слайд 5
Алюминий
1. Из истории открытия
главная
Далее
Впервые Al был
получен датским физиком Эрстедом Х.
в 1825 г. Название
элемента происходит от лат.алюмен, так в древности называли квасцы,
которые использовали для крашения
тканей (KAl(SO4)2 . 12H2O).
Позже в 1827 г. немецкий химик
Фридрих Велер получил алюминий
следующим способом:
Слайд 6
Алюминий
1. Из истории открытия
Главная
Далее
В период открытия алюминия - металл был дороже золота.
Англичане хотели почтить богатым подарком великого русского химика Д.И Менделеева, подарили ему химические весы, в которых одна чашка была изготовлена из золота, другая - из алюминия. Чашка из алюминия стала дороже золотой. Полученное «серебро из глины» заинтересовало не только учёных, но и промышленников и даже императора Франции.
Далее
Слайд 7
Алюминий
главная
Вставьте пропущенные слова
Алюминий - элемент III
группы, главной подгруппы.
Заряд ядра атома алюминия равен +13.
В
ядре атома алюминия 13 протонов.В ядре атома алюминия 14 нейтронов.
В атоме алюминия 13 электронов.
Атом алюминия имеет 3 энергетических уровня.
Электронная оболочка имеет строение 2е, 8е, 3е.
На внешнем уровне в атоме 3 электронов.
Степень окисления атома в соединениях равна +3 .
Простое вещество алюминий является металлом.
Далее
Слайд 8
Алюминий
2. Электронное строение
27
Аl
+13
0
2e
8e
3e
1s2
2s2
2p6
3s2
3p1
Краткая электронная запись
1s2
2s2
2p6
3s2
3p1
Порядок заполнения
главная
Далее
Слайд 9
Алюминий
3.Строение простого вещества
Металл
Связь
- металлическая
Кристаллическая решетка -
металлическая,
кубическая гранецентрированная
главная
Далее
Слайд 12
Алюминий
5. Свойства атома
2.2 Восстановительные
Электрохимический ряд напряжений металлов
Li,
K, Ca, Na, Mg, Al, Cr, Zn, Fe, Co,
Pb,H2,Cu,Hg,AgОслабление восстановительных свойств
главная
Далее
Слайд 13
Алюминий
6. Химические свойства
4Аl + 3O2 = 2Al2O3
t
2Al + 3S = Al2S3
C н
е м е т а л л а м и (c кислородом, с серой)2Аl + 3Cl2 = 2AlCl3
4Al + 3C = Al4C3
C неметаллами (c галогенами, с углеродом)
(Снять оксидную пленку)
2Al + 6H2O = 2Al(OH)2 + H2↑
C в о д о й
2Al + 6HCl = 2AlCl3 + H2↑
2Al + 3H2SO4 = Al2(SO4)3 + H2↑
C к и с л о т а м и
2Al + 6NaOH + 6H2O = 2Na3[Al(OH)6] + 3H2↑
2Al + 2NaOH + 2H2O =2NaAlO2 +3H2↑
Cо щ е л о ч а м и
8Al + 3Fe3O4 = 4Al2O3 + 9Fe
2Al + WO3 = Al2O3 + W
C о к с и д а м и м е т а л л о в
главная
Далее