- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Гидролиз солей 11 класс по Химии
Содержание
- 2. Цели урока:Ознакомиться с понятием гидролиза солей.Рассмотреть типы
- 3. Что такое гидролиз?Гидролиз(от греческого hydro – вода;lysis – разложение)- взаимодействие органических и неорганических веществ с водой
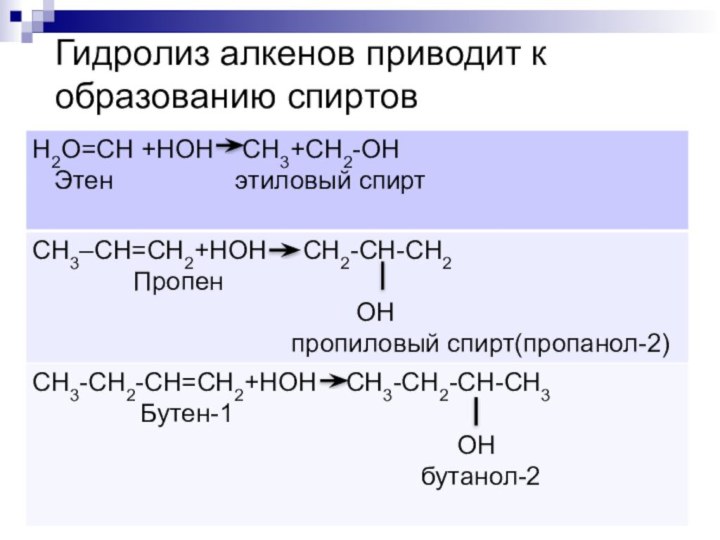
- 4. Гидролиз алкенов приводит к образованию спиртов
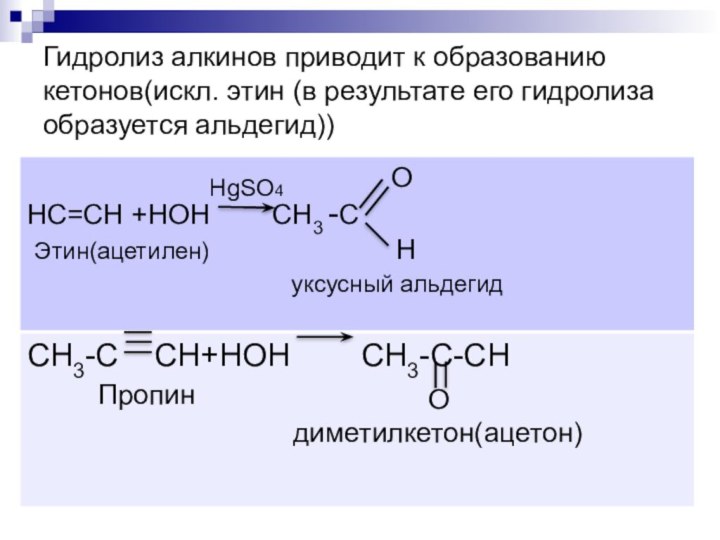
- 5. Гидролиз алкинов приводит к образованию кетонов(искл. этин (в результате его гидролиза образуется альдегид))HgSO4O
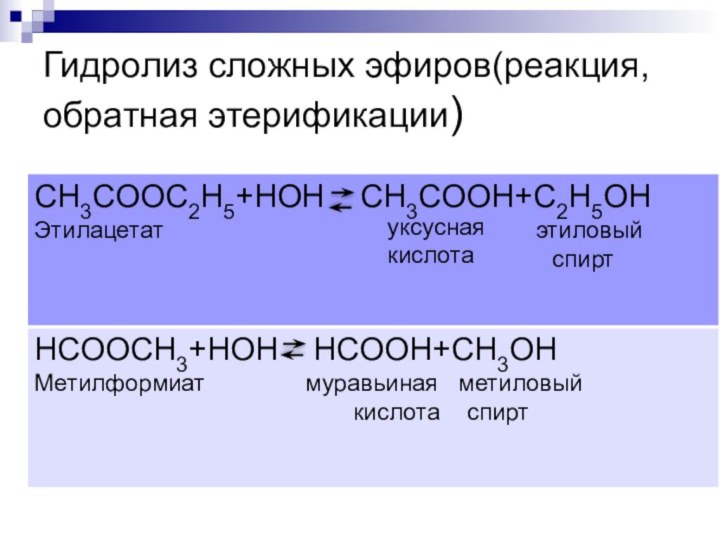
- 6. Гидролиз сложных эфиров(реакция, обратная этерификации)уксусная
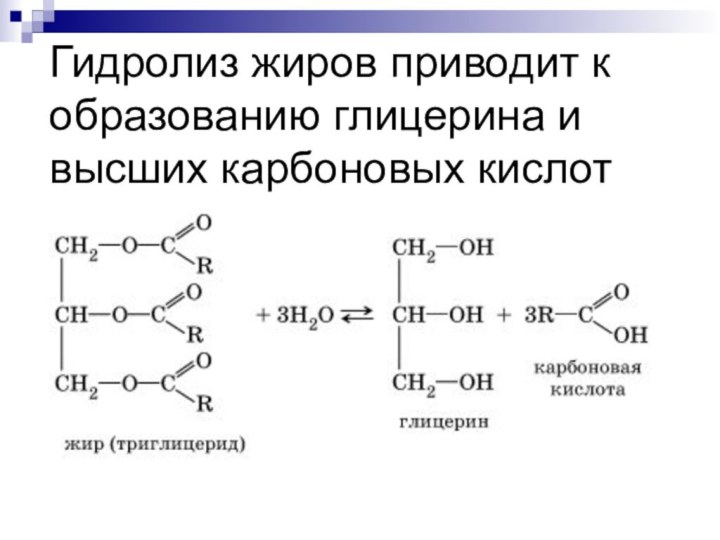
- 7. Гидролиз жиров приводит к образованию глицерина и высших карбоновых кислот
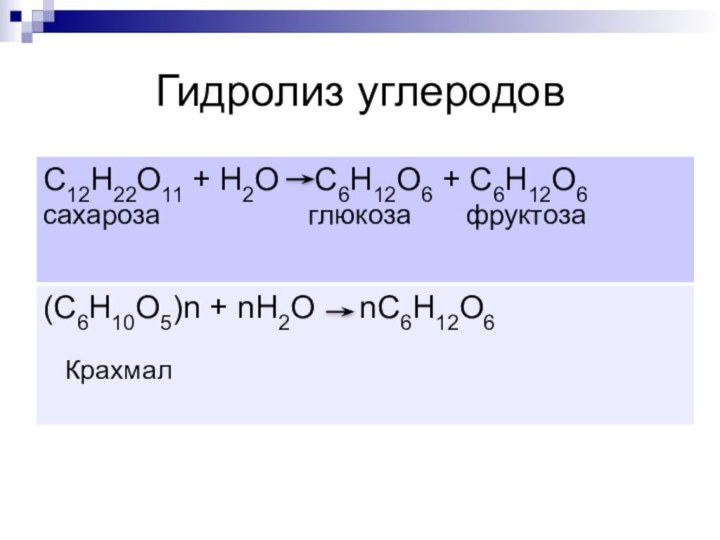
- 8. Гидролиз углеродов
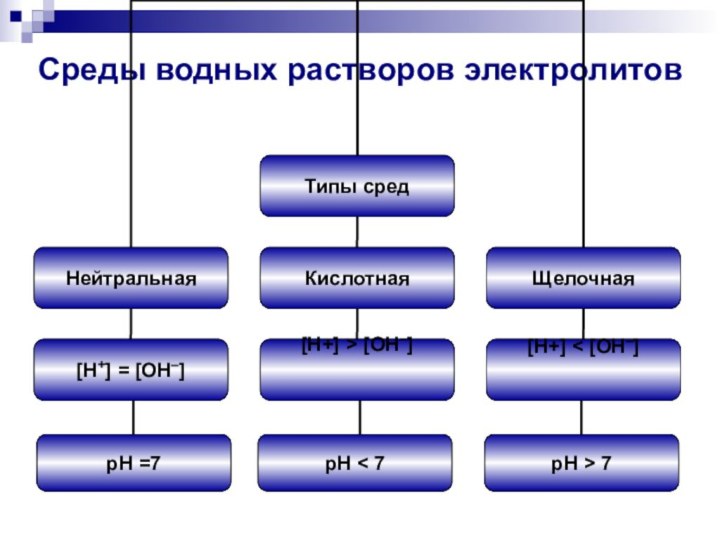
- 9. Среды водных растворов электролитовpH =7pH < 7pH > 7
- 10. Определение гидролизаГидролиз соли – это химическая реакция
- 11. Классификация солейсильным основанием и слабой кислотойслабым
- 12. Гидролиз солей3.2.1.№Реакция среды, pHТип гидролизаСоли, образованныенейтральная среда
- 13. Гидролиз солейА) гидролиз солей, образованных сильным основанием
- 14. Гидролиз солейб) гидролиз солей, образованных сильным основанием
- 15. Гидролиз солейб) гидролиз солей, образованных сильным основанием
- 16. В) гидролиз соли образованной слабым основанием и
- 17. Определение типа среды с помощью индикаторовсиняякраснаяфиолетоваяЛакмусмалиноваябесцветнаябесцветнаяФенол- фталеинжелтаярозоваяоранжеваяМетиловый оранжевыйщелочнойкислотнойнейтральнойОкраска индикатора в средеИндикатор
- 18. Лабораторный опыт Таблица № 1НейтральнаяpH = 7бесцветнаяоранжеваяфиолетоваяNa2SO4КислотнаяpH < 7бесцветнаярозоваякраснаяZnSO4ЩелочнаяpH > 7малиноваяжелтаясиняяNa2CO3Фенол-фталеинМетил-оранжЛакмусСреда,pHОкраска индикатораСоли373246
- 19. Сущность гидролиза1. Na2CO3 →
- 20. Уравнения гидролиза← Na2CO3 → NaOHсильное основаниеH2CO3слабая
- 21. Уравнения гидролиза← ZnSO4 → Zn(ОН)2слабое основаниеH2SO4сильная
- 22. Задание. Определите реакцию среды водных растворов солей.
- 23. Гидролиз солей4.3.2.1.№Реакция средыТип гидролизаСоли, образованные?гидролиз покатиону ианиону
- 24. Готовимся к ЕГЭ 1. Установите соответствие: Формула соли Тип гидролиза 1.
- 25. Готовимся к ЕГЭ 2. Установите соответствие: Формула соли Среда раствора 1.
- 26. Готовимся к ЕГЭ 3. Установите соответствие: Формула соли Значение pH 1.
- 27. Интересные факты
- 28. Скачать презентацию
- 29. Похожие презентации














Слайд 2
Цели урока:
Ознакомиться с понятием гидролиза солей.
Рассмотреть типы гидролиза.
Научиться
составлять ионные уравнения гидролиза солей.
по её формуле.
Слайд 3
Что такое гидролиз?
Гидролиз
(от греческого hydro – вода;
lysis –
разложение)
- взаимодействие органических и неорганических веществ с водой
Слайд 5 Гидролиз алкинов приводит к образованию кетонов(искл. этин (в
результате его гидролиза образуется альдегид))
HgSO4
O
Слайд 10
Определение гидролиза
Гидролиз соли – это химическая реакция обмена
соли с водой,
в результате которой ионы слабого
электролита, входящие в состав соли, соединяются с составными частями воды: H+ и OH- .
Слайд 11
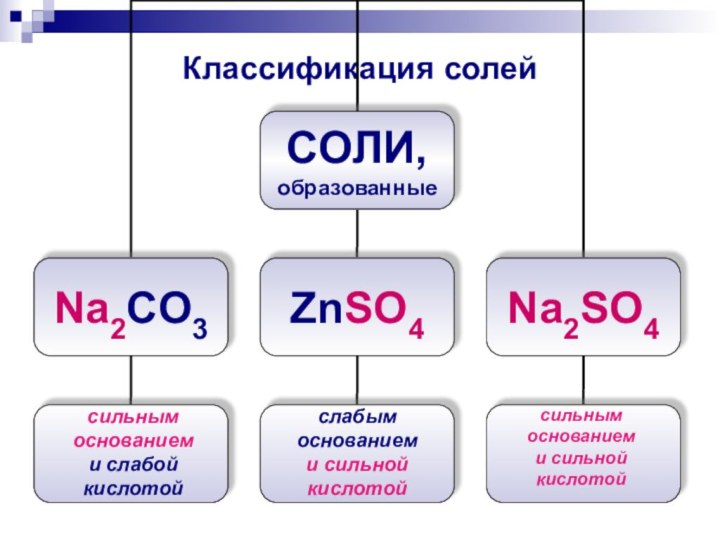
Классификация солей
сильным
основанием
и слабой кислотой
слабым
основанием
и сильной
кислотой
сильным
основанием
и
сильной
кислотой
Слайд 12
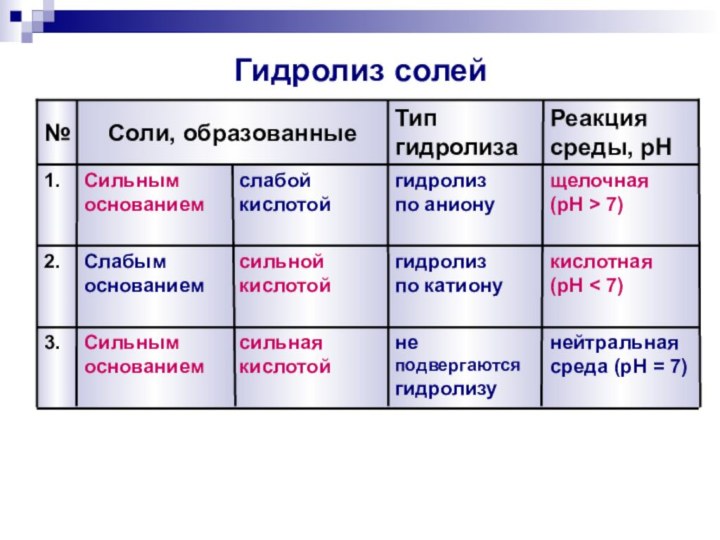
Гидролиз солей
3.
2.
1.
№
Реакция среды, pH
Тип гидролиза
Соли, образованные
нейтральная среда (pH
= 7)
не
подвергаются гидролизу
сильная кислотой
Сильным основанием
кислотная
(pH < 7)
гидролиз
по
катионусильной кислотой
Слабым основанием
щелочная
(pH > 7)
гидролиз
по аниону
слабой кислотой
Сильным основанием
Слайд 13
Гидролиз солей
А) гидролиз солей, образованных сильным основанием и
слабой кислотой.
Na2CO3 2Na+ + CO32 -
CO32 - +
HOH HCO3- + OH- среда щелочная pH >72Na++CO32 -+HOH Na++НCO3- n +Na++OH-
Na2CO3+HOH NaHCO3+NaOH
K2S 2K++S2 –
S2 -+HOH HS-+OH-
2K++S2 -+HOH K+ +HS-+K++OH-
K2S+H2O KHS+KOH
Слайд 14
Гидролиз солей
б) гидролиз солей, образованных сильным основанием и
сильной кислотой
AlCl3 Al3++ 3Cl-
Al3+ + HOH ⇄ AlOH2+ + H+ -
кислая среда pH < 7Al3+ + 3Cl- + HOH ⇄ AlOH2+ + 2Cl- + H+ + Cl-
AlCl3 + HOH ⇄ AlOHCl2 + HCl
Гидрохлорид
алюминия
Слайд 15
Гидролиз солей
б) гидролиз солей, образованных сильным основанием и
сильной кислотой
Zn(NO3)2 Zn2+ 2NO3-
Zn2+ + HOH ⇄ ZnOH+ + H+ -кислая
среда pH < 7Zn2+ + 2NO3- + HOH ⇄ ZnOH+ + NO3- + H++ NO3-
Zn(NO3)2 + HOH ⇄ ZnOHNO3 + HNO3
Гидроксонитрат
цинка
Слайд 16 В) гидролиз соли образованной слабым основанием и слабой
кислотой
CH3COONH4 CH3COO- +NH4+
CH3COO +HOHCH3COOH+OH-
NH4+ +HOH NH4OH+H+
[OH] = [H]
pH=7-среда нейтральная
Слайд 17
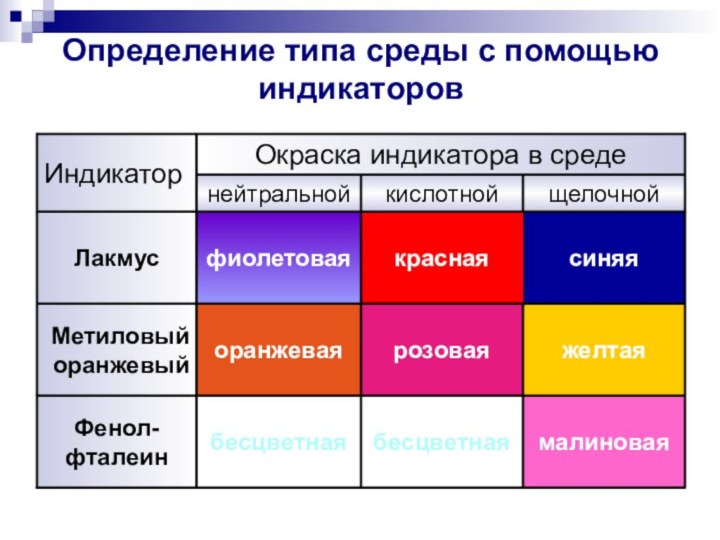
Определение типа среды с помощью индикаторов
синяя
красная
фиолетовая
Лакмус
малиновая
бесцветная
бесцветная
Фенол-
фталеин
желтая
розовая
оранжевая
Метиловый оранжевый
щелочной
кислотной
нейтральной
Окраска индикатора
в среде
Индикатор
Слайд 18
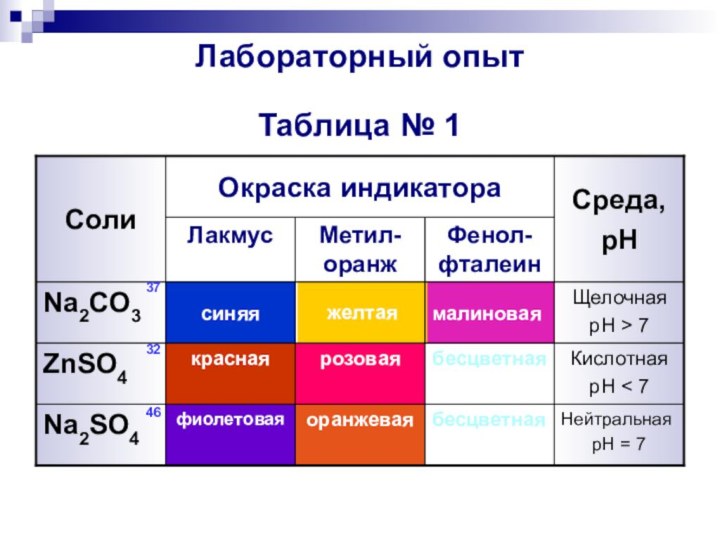
Лабораторный опыт
Таблица № 1
Нейтральная
pH = 7
бесцветная
оранжевая
фиолетовая
Na2SO4
Кислотная
pH < 7
бесцветная
розовая
красная
ZnSO4
Щелочная
pH
> 7
малиновая
желтая
синяя
Na2CO3
Фенол-фталеин
Метил-оранж
Лакмус
Среда,
pH
Окраска индикатора
Соли
37
32
46
Слайд 19
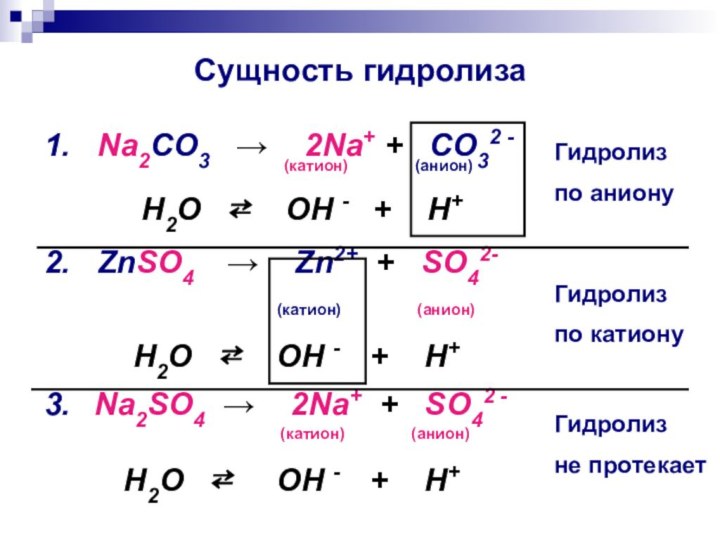
Сущность гидролиза
1. Na2CO3 → 2Na+
+ CO32 -
(катион) (анион)H2O ⇄ OH - + H+
2. ZnSO4 → Zn2+ + SO42-
(катион) (анион)
H2O ⇄ OH - + H+
3. Na2SO4 → 2Na+ + SO42 -
(катион) (анион)
H2O ⇄ OH - + H+
Гидролиз
по аниону
Гидролиз
по катиону
Гидролиз
не протекает
Слайд 20
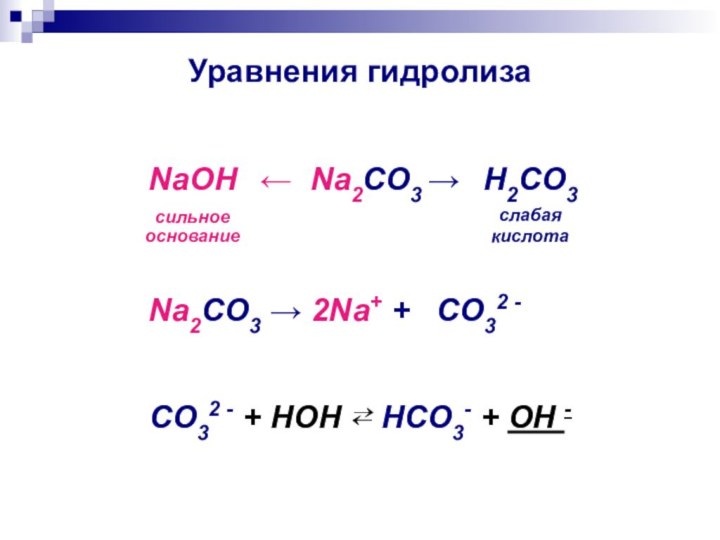
Уравнения гидролиза
← Na2CO3 →
NaOH
сильное
основание
H2CO3
слабая
кислота
Na2CO3 → 2Na+
+ CO32 -
CO32 - + HOH ⇄ HCO3- + OH -
Слайд 21
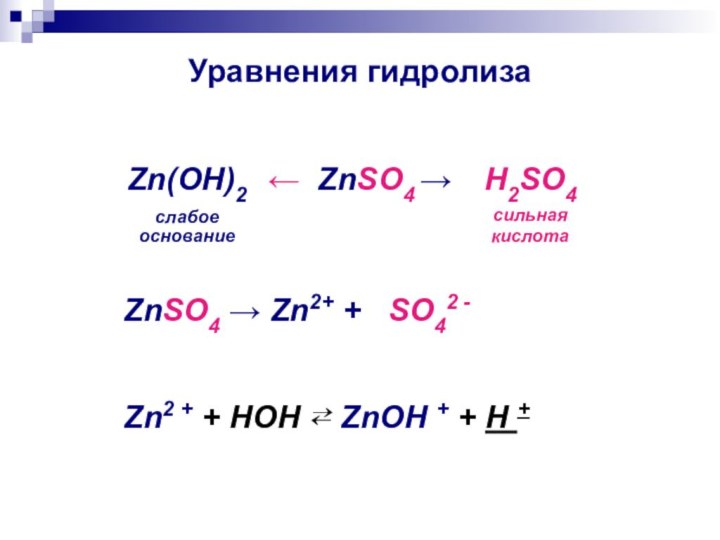
Уравнения гидролиза
← ZnSO4 →
Zn(ОН)2
слабое
основание
H2SO4
сильная
кислота
ZnSO4 → Zn2+
+ SO42 -
Zn2 + + HOH ⇄ ZnOH + + H +
Слайд 22 Задание. Определите реакцию среды водных растворов солей. Таблица №
2
NaNO3
K2S
Na2SiO3
5.
NH4NO3
LiNO3
NaClO4
4.
KMnO4
KI
K3PO 4
3.
Na2SO3
FeCl3
CuSO4
2.
KCl
NaNO2
Li2SO4
1.
III ряд
II ряд
I ряд
№
Н
К
Щ
Н
Щ
Щ
Н
Н
К
Щ
Н
Щ
Н
К
Н
н-нейтральная; к – кислотная; щ - щелочная
Слайд 23
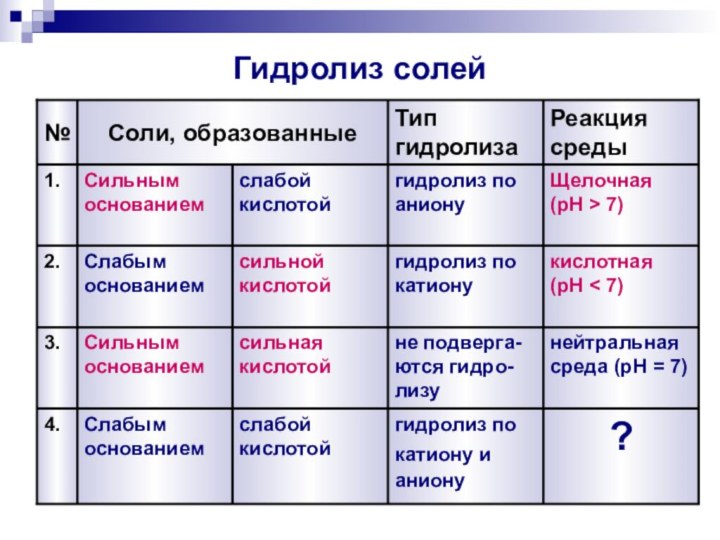
Гидролиз солей
4.
3.
2.
1.
№
Реакция среды
Тип гидролиза
Соли, образованные
?
гидролиз по
катиону и
аниону
слабой кислотой
Слабым
основанием
нейтральная среда (pH = 7)
не подверга-ются гидро-лизу
сильная кислотой
Сильным основанием
кислотная
(pH
< 7)гидролиз по катиону
сильной кислотой
Слабым основанием
Щелочная
(pH > 7)
гидролиз по аниону
слабой кислотой
Сильным основанием
Слайд 24
Готовимся к ЕГЭ
1. Установите соответствие:
Формула соли Тип гидролиза
1. FeCl2 А.
по катиону
2. Ba(NO3)2
Б. по аниону3. KF В. не гидролизуется
4. Na3PO4
Ответ:
1А;
2В;
3Б;
4Б
Слайд 25
Готовимся к ЕГЭ
2. Установите соответствие:
Формула соли Среда раствора
1. K2SO4 А.
кислотная
2. Li2CO3
Б. щелочная3. NH4Br В. нейтральная
4. CrCl3
Ответ:
1В;
2Б;
3А;
4А
Слайд 26
Готовимся к ЕГЭ
3. Установите соответствие:
Формула соли Значение pH
1. K2SiO3 А.
pH < 7
2. LiNO3
Б. pH > 73. CuCl2 В. pH = 7
4. NaCl
Ответ:
1Б;
2В;
3А;
4В