- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Алкины
Содержание
- 2. Цель урока: Продолжить формирование представлений учащихся
- 3. Задачи: Обучающие:- обобщение и систематизация знаний по теме «Алкины»;-
- 4. Сегодня на уроке вы узнаете:Понятие о непредельных
- 5. Понятие об алкинахАлкины – углеводороды, содержащие в
- 6. Характеристика тройной связиВид гибридизации –
- 7. Схема образования sp -гибридных орбиталей
- 8. Схема образования sp -гибридных орбиталей
- 9. Номенклатура алкинов. (Согласно международной номенклатуре названия
- 10. Гомологический ряд алкинов C2H2 C3H4 C4H6 C5H8 C6H10 C7H12Этин ПропинБутинПентинГексинГептин
- 11. Изомерия алкинов Структурная изомерия1. Изомерия положения тройной
- 12. Выполните упражнение:Назовите вещество.Составьте к нему три изомера разных видов изомерии. Назовите изомеры.
- 13. Физические свойстваТемпературы кипения и плавления алкинов, так
- 14. Ацетилен получают в промышленности двумя способами:1. Термический
- 15. Химические свойства алкиновХимические свойства ацетилена и его
- 16. Реакции присоединения1. Галогенирование Обесцвечивание бромной воды является качественной реакцией на все непредельные углеводороды
- 17. 2. Гидрогалогенирование.3. Гидрирование.4. Гидратация.
- 18. ОкислениеАцетилен и его гомологи окисляются перманганатом калия
- 19. Горение ацетиленаПри сгорании (полном окислении) ацетилена выделяется
- 20. Реакции замещенияПри взаимодействии ацетилена (или R−C≡C−H) с
- 21. Реакция полимеризации1. Димеризация под действием водного раствора
- 22. Применение алкинов
- 23. Домашнее заданиеУчебник О.С. Габриелян (10 класс базовый уровень) § 5
- 24. Скачать презентацию
- 25. Похожие презентации
Цель урока: Продолжить формирование представлений учащихся об изомерии и номенклатуре органических веществ, умений составлять структурные формулы веществ, давать им названия на примере алкинов, изучить химические свойства и способы получения алкинов, показать зависимость химических свойств от






















Слайд 3
Задачи:
Обучающие:- обобщение и систематизация знаний по теме «Алкины»;- выявление
уровня усвоения основных понятий, правил; проверка умений решать задачи на вывод
МФ (молекулярной формулы) органических веществ.Развивающие: - развивать умение рационально планировать свою деятельность, продолжить формирование умений применять приемы сравнения, систематизации, составления уравнений химических реакций;- развивать монологическую речь.
Воспитательные:- воспитывать у студентов интерес к учению;- стремление добиваться успехов в учебе за счет добросовестного отношения к своему труду.
Слайд 4
Сегодня на уроке вы узнаете:
Понятие о непредельных углеводородах.
Характеристика
тройной связи.
Изомерия и номенклатура алкинов.
Физические свойства.
Получение алкинов.
Свойства алкинов.
Применение алкинов.
Слайд 5
Понятие об алкинах
Алкины – углеводороды, содержащие в молекуле
одну тройную связь между атомами углерода, а качественный и
количественный состав выражается общей формулойСnН2n - 2, где n ≥ 2.
Алкины относятся к непредельным углеводородам, так как их молекулы содержат меньшее число атомов водорода, чем насыщенные.
Слайд 6
Характеристика
тройной связи
Вид гибридизации –
sp
Валентный угол –
180Длина связи С = С – 0,12 нм
Строение ─ линейное
Вид связи – ковалентная полярная
По типу перекрывания – δ и 2 π
Слайд 9
Номенклатура алкинов.
(Согласно международной номенклатуре названия
ацетиленовых углеводородов
производят от соответствующего алкана с заменой
суффикса –ан на –ин.)
Слайд 10
Гомологический
ряд алкинов
C2H2
C3H4
C4H6
C5H8
C6H10
C7H12
Этин
Пропин
Бутин
Пентин
Гексин
Гептин
Слайд 11
Изомерия алкинов
Структурная изомерия
1. Изомерия положения тройной связи
(начиная с С4Н6):
СН ≡С−СН2−СН3
СН3−С≡С−СН3бутин-1 бутин-2
2. Изомерия углеродного скелета (начиная с С5Н8):
СН ≡С−СН2−СН2−СН3 СН ≡С−СН−СН3
⏐
СН3
пентин-1 3-метилбутин-1
3. Межклассовая изомерия с алкадиенами и циклоалкенами, (начиная с С4Н8):
СН = СН
СН ≡С–СН2–СН3 СН2=СН–СН=СН2 ⏐ ⏐
СН2 –СН2
бутин-1 бутадиен-1,3 циклобутен
Слайд 12
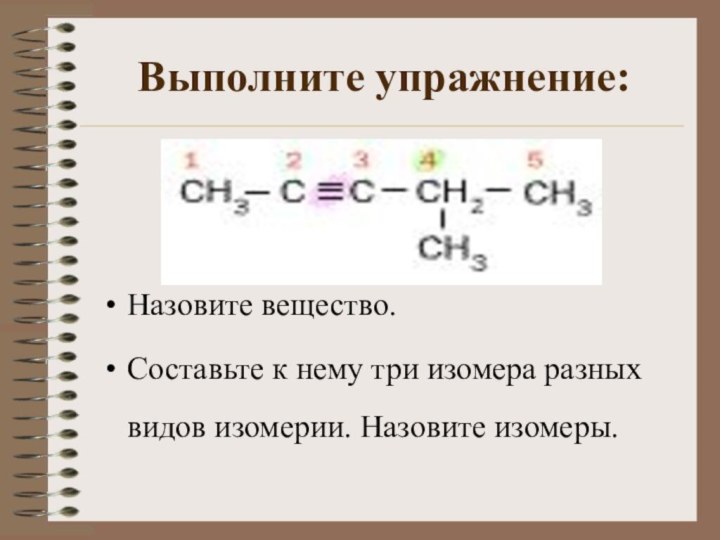
Выполните упражнение:
Назовите вещество.
Составьте к нему три изомера разных
видов изомерии. Назовите изомеры.
Слайд 13
Физические свойства
Температуры кипения и плавления алкинов, так же
как и алкенов, закономерно повышаются при увеличении молекулярной массы
соединений.Алкины имеют специфический запах. Они лучше растворяются в воде, чем алканы и алкены.
Слайд 14
Ацетилен получают в промышленности двумя способами:
1. Термический крекинг
метана:
1500°С
2СН4 ⎯⎯→
С2Н2 + 3Н2 2. Гидролиз карбида кальция:
CaC2 + 2H2O ⎯⎯→ C2H2 + Ca(OH)2
Получение алкинов
Слайд 15
Химические свойства алкинов
Химические свойства ацетилена и его гомологов
в основном определяются наличием в их молекулах тройной связи.
Наиболее характерны для алкинов реакции присоединения.
Слайд 16
Реакции присоединения
1. Галогенирование
Обесцвечивание бромной воды является
качественной реакцией на все непредельные углеводороды
Слайд 17
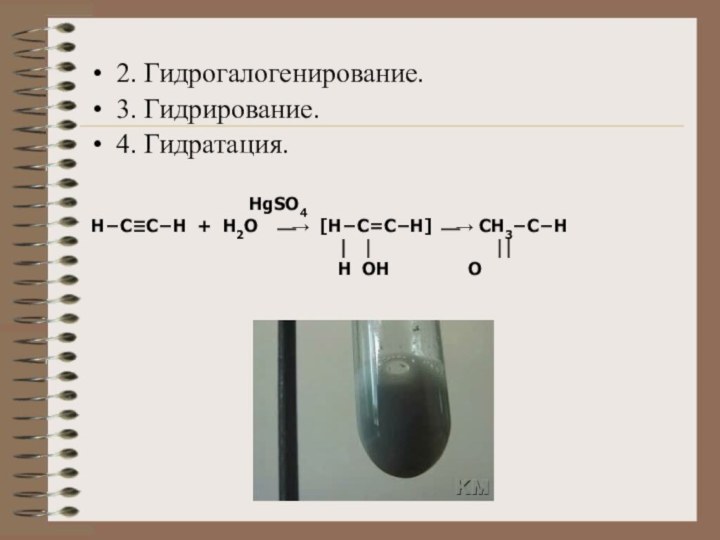
2. Гидрогалогенирование.
3. Гидрирование.
4. Гидратация.
HgSO4
Н−C≡C−H + H2O ⎯→ [H−C=C−H] ⎯→ CH3−C−H
⏐ ⏐ ⏐⏐
H OH O
Слайд 18
Окисление
Ацетилен и его гомологи окисляются перманганатом калия с
расщеплением
тройной связи и образованием карбоновых кислот:
R−C≡C−R’ + 3[O] +
H2O ⎯→ R−COOH + R’−COOHАлкины обесцвечивают раствор KMnO4, что используется
для их качественного определения.
Слайд 19
Горение ацетилена
При сгорании (полном окислении) ацетилена выделяется большое
количества тепла:
HC≡CH + 2О2 ⎯→ 2СО2 + Н2О +
Q
Слайд 20
Реакции замещения
При взаимодействии ацетилена (или R−C≡C−H) с аммиачными
растворами
оксида серебра выпадают осадки нерастворимых ацетиленидов:
HC≡CH + 2[Ag(NH3)2]OH ⎯→
AgC≡CAg ↓ + 4NH3 + 2H2O Качественная реакция на
концевую тройную связь
Слайд 21
Реакция полимеризации
1. Димеризация под действием водного раствора CuCl
и NH4Cl:
НC≡CH + НC≡CH
⎯→ Н2C=CH−C≡CH(винилацетилен)
2. Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского):
С, 600 °С
3НC≡CH ⎯⎯→ С6H6 (бензол)





























