- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Признаки химических реакций
Содержание
- 2. Химические превращения веществ — это явления, в
- 3. Признаки протекания химических реакций
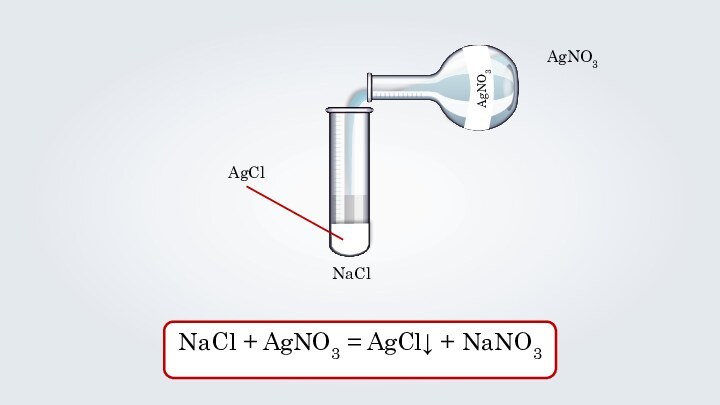
- 4. Образование осадка
- 5. NaClAgNO3AgCl NaCl + AgNO3 = AgCl↓ + NaNO3
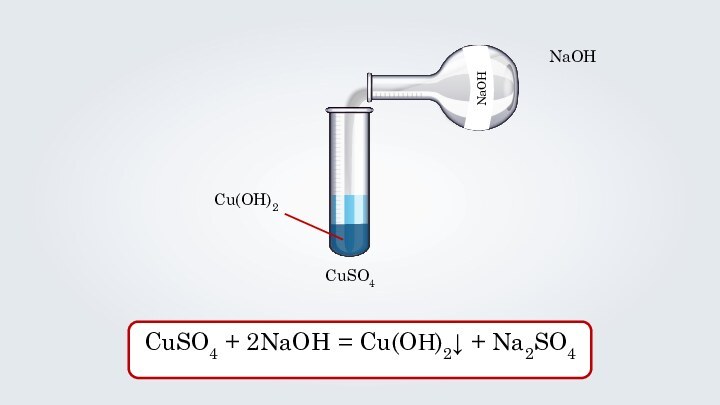
- 6. Растворение осадка
- 7. CuSO4NaOHCu(OH)2CuSO4 + 2NaOH = Cu(OН)2↓ + Na2SO4
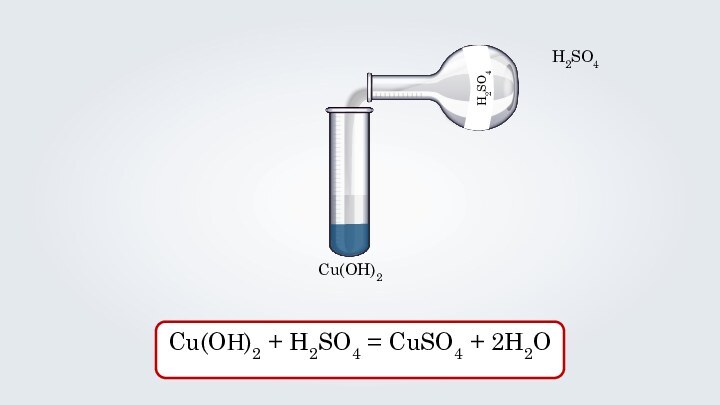
- 8. H2SO4Cu(OH)2Cu(OН)2 + H2SO4 = CuSO4 + 2H2O
- 9. выпадение осадкарастворение осадка
- 10. Изменение цвета и выделение газа
- 11. Этот опыт проводится только учителемс соблюдением правил безопасности!
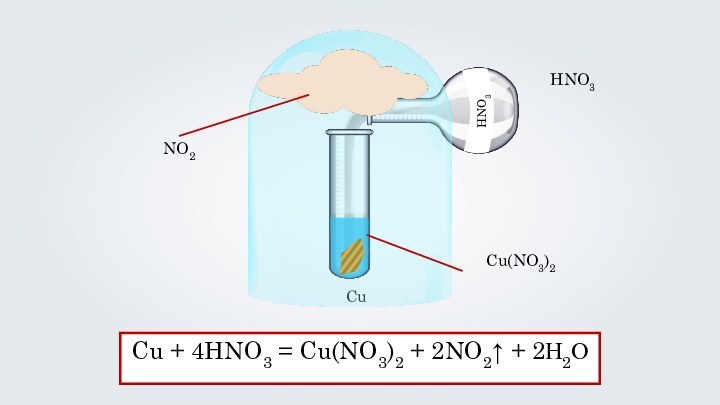
- 12. CuHNO3Cu + 4HNO3 = Cu(NO3)2 + 2NO2↑ + 2Н2ОCu(NO3)2NO2
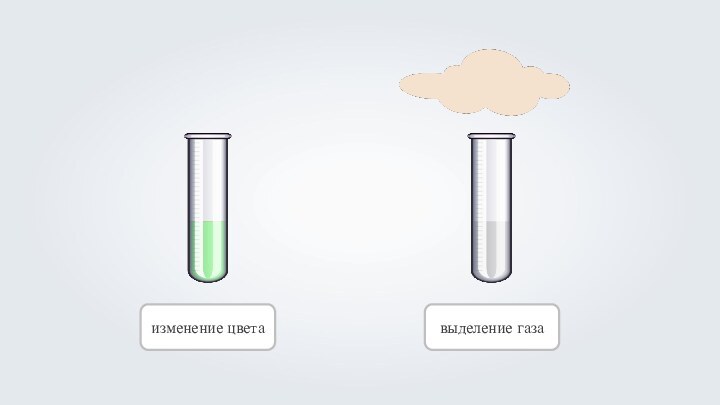
- 13. изменение цветавыделение газа
- 14. Излучение света и выделение теплоты
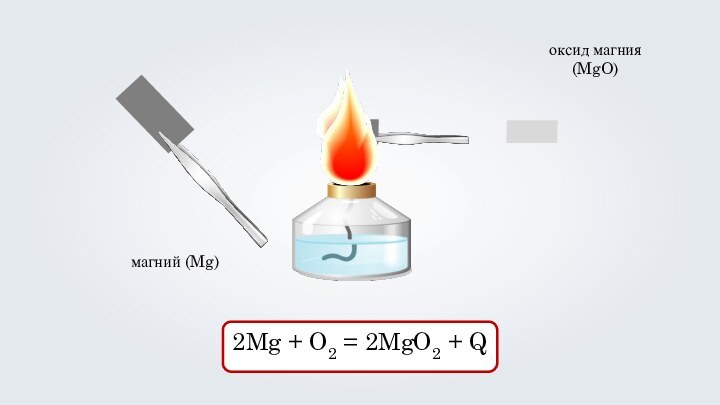
- 15. магний (Mg)оксид магния (MgO)2Mg + O2 = 2MgO2 + Q
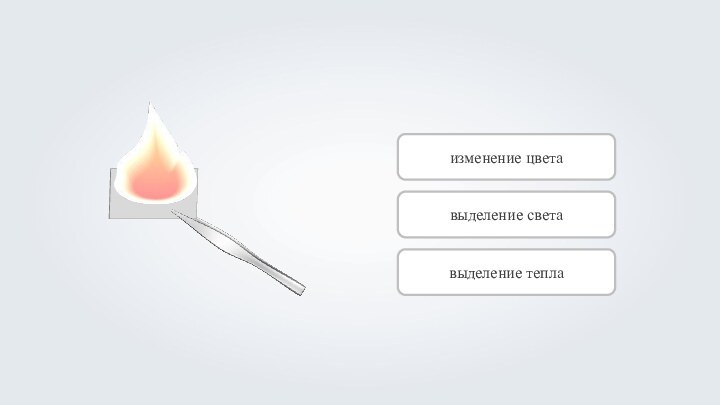
- 16. изменение цветавыделение светавыделение тепла
- 17. Возникновение звука илизвуковой эффект реакции
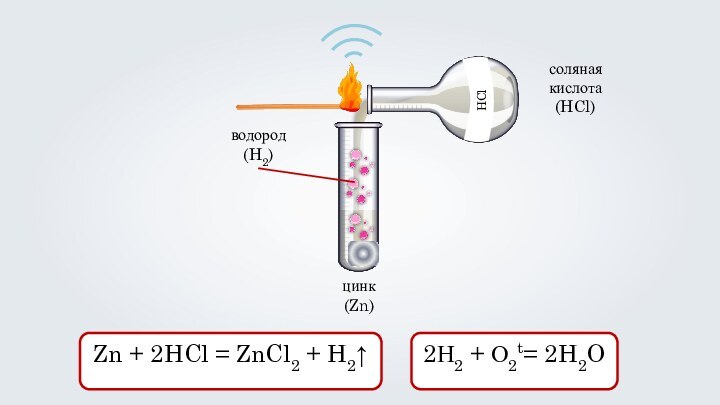
- 18. цинк (Zn)соляная кислота (HCl)водород (H2) Zn + 2HCl = ZnCl2 + H2↑2Н2 + О2t= 2H2O
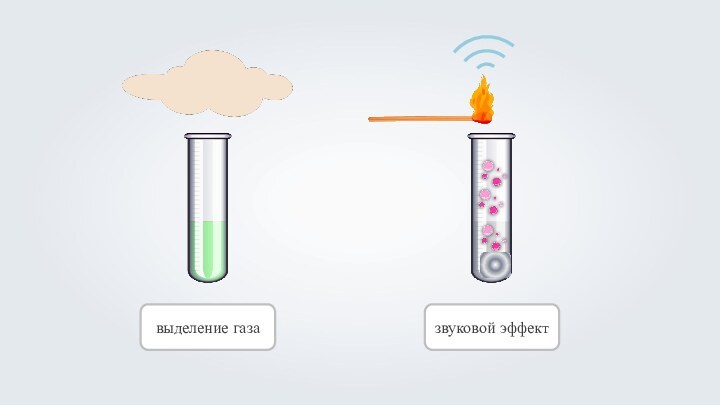
- 19. выделение газазвуковой эффект
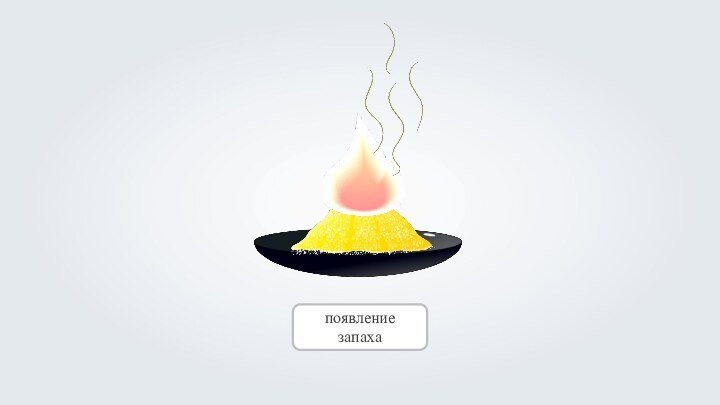
- 20. Появление запаха
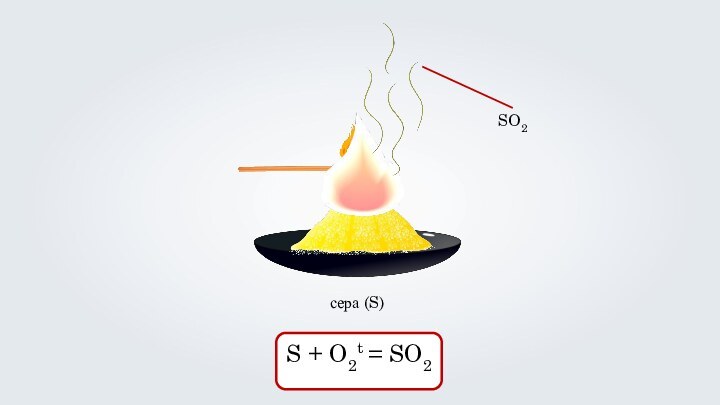
- 21. сера (S)SO2S + O2t = SO2
- 22. появление запаха
- 23. Скачать презентацию
- 24. Похожие презентации
Химические превращения веществ — это явления, в результате которых из одних веществ образуются другие. Они также носят название химических реакций.