- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Сера. Характеристика химического элемента и простого вещества
Содержание
- 2. Сера в природеВ каком виде химический элемент сера встречается в природе?Стр. 132
- 3. Сера в природеСамороднаяСульфидная:СероводородH2SЦинковаяобманкаZnSКиноварь HgSСвинцовый блеск PbSПирит FeS2Cульфатная:Глауберова сольNa2SO4·10H2OГипсCaSO4·2H2O
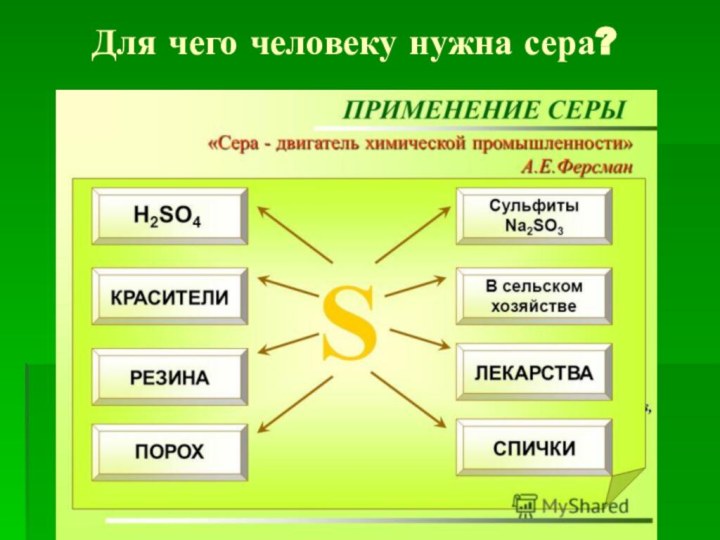
- 4. С. 133Для чего человеку нужна сера?
- 5. ПолучениеВыплавление из природных залежейНеполное сгорание H2S:
- 6. Положение х.э. S в ПСХЭ Д.И. Менделеева: ПериодРядГруппаПодгруппа№
- 7. Положение в ПСХЭПериод – 3 (малый)Ряд –
- 8. Важнейшие характеристики атома S:Валентность: Степени окисления:II, IV, VI-2,
- 9. Строение атома↑↑↑↓↑↓↑↓↑↓↑↓↑↓↑↓n=3n=2n=3**n=1n=3*↑↓↑↑↑↑↑↑↑↑↑↑С.О. -2, 0, +2С.О. +4С.О. +6
- 10. Сера – простое веществоАЛЛОТРОПИЯСпособность атома образовывать несколько простых веществСтр. 130 - 131
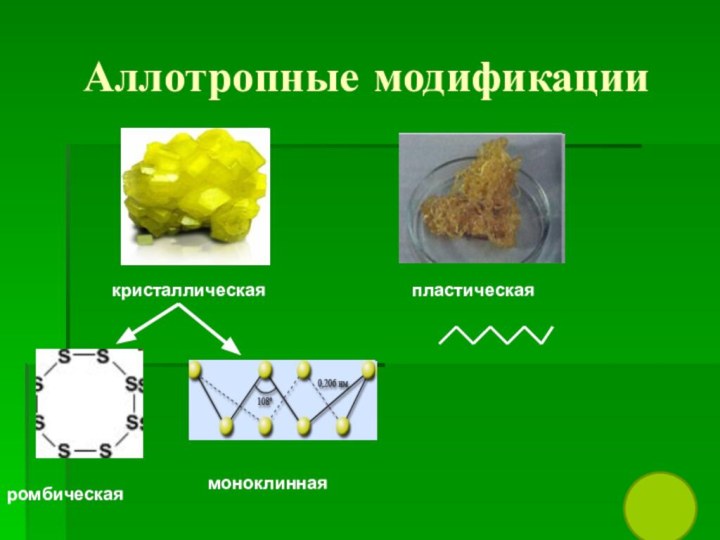
- 11. Аллотропные модификациикристаллическаяпластическаяромбическаямоноклинная
- 12. Химические свойстваОкислитель:S + Hg →S + Zn
- 13. Скачать презентацию
- 14. Похожие презентации
Сера в природеВ каком виде химический элемент сера встречается в природе?Стр. 132











Слайд 3
Сера в природе
Самородная
Сульфидная:
Сероводород
H2S
Цинковая
обманка
ZnS
Киноварь HgS
Свинцовый блеск PbS
Пирит FeS2
Cульфатная:
Глауберова соль
Na2SO4·10H2O
Гипс
CaSO4·2H2O
Слайд 5
Получение
Выплавление из природных залежей
Неполное сгорание H2S:
2H2S + O2 = 2H2O + 2S
Подкисление раствора тиосульфата
натрия:Na2S2O3 + 2HCl = 2NaCl + SO2 + H2O + S
Слайд 8
Важнейшие характеристики атома S:
Валентность:
Степени окисления:
II, IV, VI
-2, 0,
+2, +4, +6
Объясните с позиции строения атома возможность существования
указанных валентностей и степеней окисления атома серы.
Слайд 10
Сера – простое вещество
АЛЛОТРОПИЯ
Способность атома образовывать несколько простых
веществ
Стр. 130 - 131
Слайд 12
Химические свойства
Окислитель:
S + Hg →
S + Zn →
S
+ Al →
S + Fe →
S + H2 →
S
+ C →Восстановитель:
S + Cl2 →
S + O2 →
S + F2 →