бромоводородная, фтороводородная, азотная, азотистая:
1) 5
2) 4 3) 3Кислоты
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть












































Кислоты
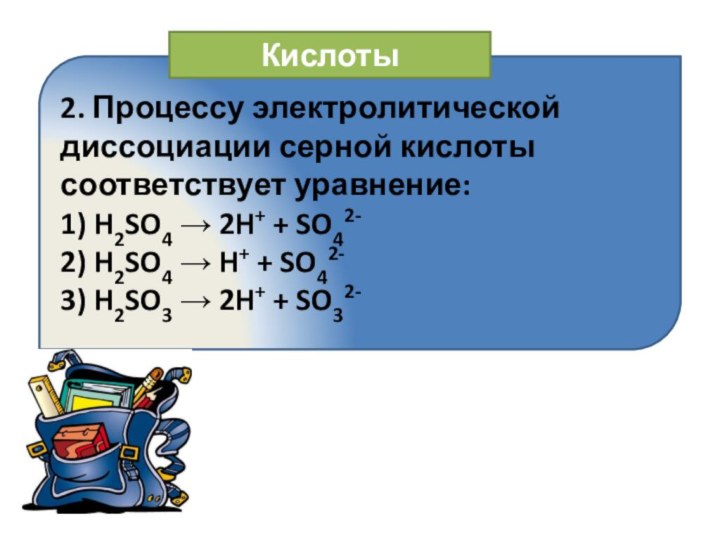
Кислоты
Кислоты
Кислоты
Кислоты
Кислоты
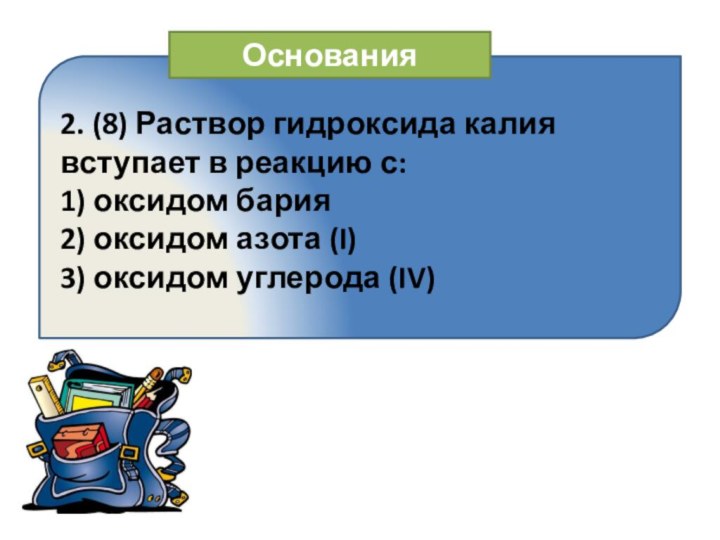
Основания
Основания
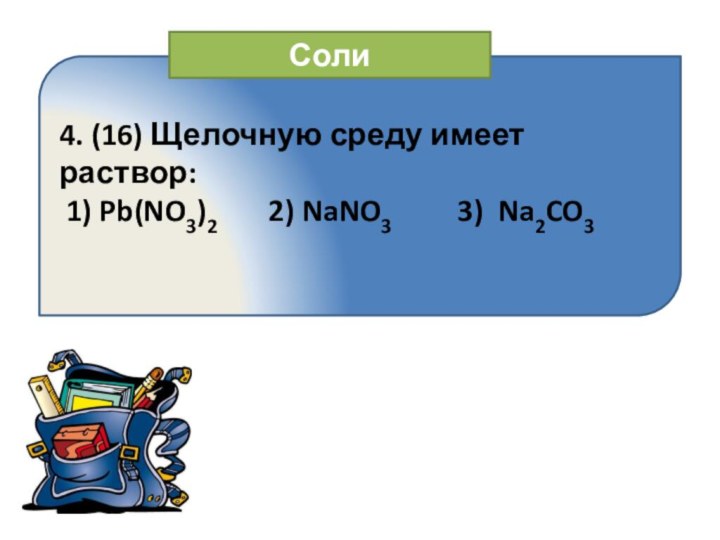
Соли
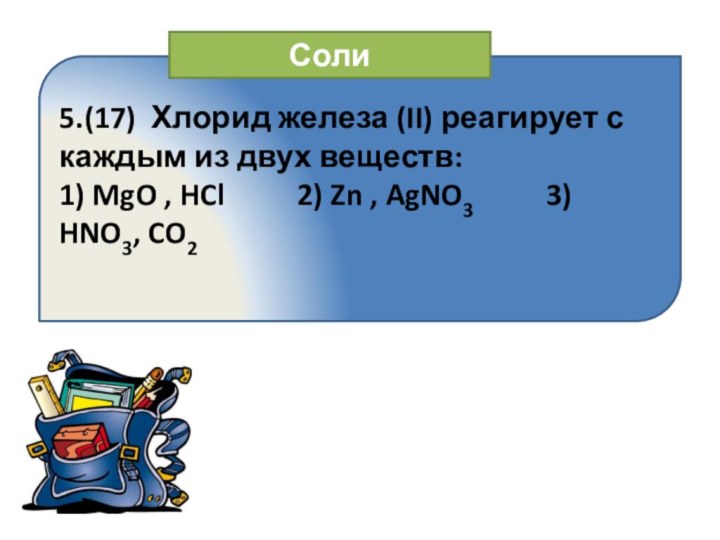
Соли
Соли
Соли
Соли