- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Азотная кислота и ее соли: общие и особенные химические свойства, применение (9 класс)
Содержание
- 2. Характеристика кислотыАзо́тная кислота́ — HNO3: кислородсодержащая, одноосновная, сильная,
- 3. Строение азотной кислоты
- 4. Химические свойства Общие с кислотами1. CuO
- 5. Химические свойстваОсобенные свойства:На свету: 4HNO3→4NO2 + 2H2O
- 6. Химические свойства1. HNO3 + Mg → Mg(NO3)2
- 7. Разложение нитратовMe(NO3)m → Me(NO2)m + O2↑, Ме-
- 8. Скачать презентацию
- 9. Похожие презентации
Характеристика кислотыАзо́тная кислота́ — HNO3: кислородсодержащая, одноосновная, сильная, летучая, стабильная. В водных растворах она практически полностью диссоциирует на ионы.


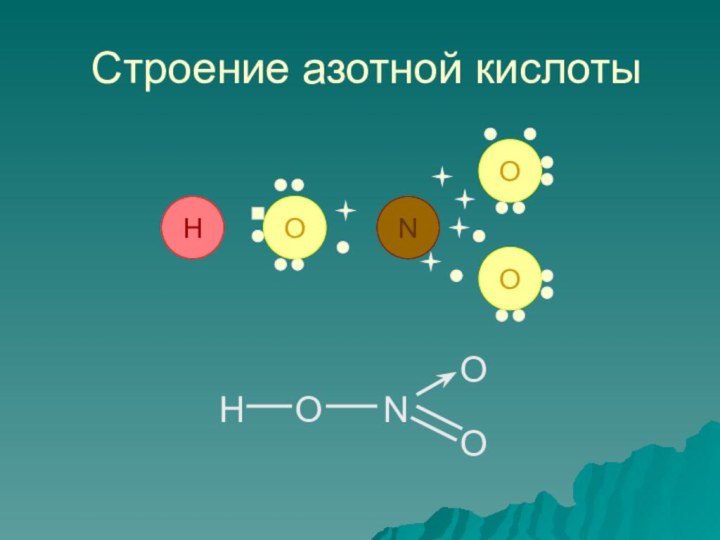





Слайд 2
Характеристика кислоты
Азо́тная кислота́ — HNO3: кислородсодержащая, одноосновная, сильная, летучая,
Слайд 4
Химические свойства
Общие с кислотами
1. CuO +
2HNO3→ Cu(NO3)2 + H2O
2. Cu(OH)2 + 2HNO3→Cu(NO3)2 + 2H2O
NaOH + HNO3→NaNO3 + H2O3. K2CO3+2HNO3→2KNO3+CO2↑+H2O
Слайд 5
Химические свойства
Особенные свойства:
На свету: 4HNO3→4NO2 + 2H2O +
O2↑
Взаимодействие с металлами:
HNO3 + Me → Me(NO3)m + H2O
+ NH3↑ ( N2↑, N2O↑, NO↑, NO2↑) HNO3 + Mg → Mg(NO3)2 +H2O + N2O↑
конц.
HNO3 + Cu → Cu(NO3)2 + H2O + NO2↑
конц.
HNO3 + Al (Fe) –пассивирует
конц.
Слайд 6
Химические свойства
1. HNO3 + Mg → Mg(NO3)2 +NH4NO3
+ H2O
разб.
N2↑HNO3 + Al → Al(NO3)3 +NH4NO3 + H2O
разб. N2↑
HNO3 + Cu → Cu(NO3)2 + NO↑ +H2O
разб.
Слайд 7
Разложение нитратов
Me(NO3)m → Me(NO2)m + O2↑, Ме- до
Mg
Me(NO3)m → Me+m2O-2m + NO2↑ + O2↑, Ме- от
Mg до CuMe(NO3)m → Me + NO2↑ + O2↑, Me – после Cu





























