- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии Основания 8 класс
Содержание
- 2. ОСНОВАНИЯ
- 3. Основания – это сложные вещества, состоящие из атомов металлов и одной или нескольких гидроксогрупп (ОН-).Ме(ОН)n+n
- 4. NaOH - гидроксид натрияZn(OH)2–гидроксид цинкаCu(OH)2-гидроксид меди (II)
- 5. ОСНОВАНИЯрастворимые -щелочинерастворимыеLiOH NaOH KOH RbOH
- 6. Гидроксиды щелочных металлов – при обычных условиях
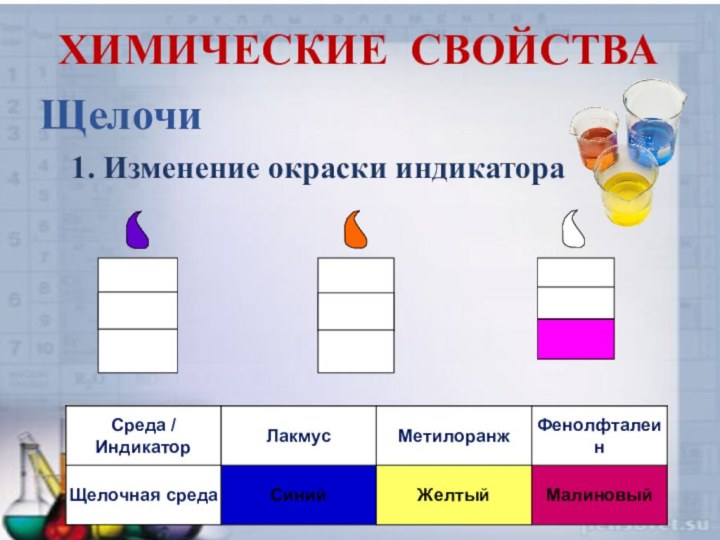
- 7. ХИМИЧЕСКИЕ СВОЙСТВА1. Изменение окраски индикатораЩелочи
- 8. ХИМИЧЕСКИЕ СВОЙСТВАЩелочи2. щелочь + кислотный оксид =
- 9. ХИМИЧЕСКИЕ СВОЙСТВАНерастворимые основания1. нерастворимые основания разлагаются при
- 10. ХИМИЧЕСКИЕ СВОЙСТВААмфотерные основанияZn(OH)2 + 2NaOH → Na2[Zn(OH)4] Аl(ОН)3 + NaOH = NaAlO2 + 2H2O2Al(OH)3 + Na2O → 2NaAlO2 + 3H2Oсплавлениев растворе
- 11. ХИМИЧЕСКИЕ СВОЙСТВААмфотерные основанияZn(OH)2+2HCl = ZnCl2+2H2O2Cr(OH)3 + 3SO3 = Cr2(SO4)3 + 3H2OАмфотерный гидроксидКислотный оксидсольвода++=2Al(OH)3 → Al2O3 + 3H2O
- 12. ПОЛУЧЕНИЕ1. Металл + H2O = ЩЁЛОЧЬ + Н2↑ Здесь, Металл
- 13. CuCl2+2NaOH=Cu(OH)2↓+2NaClНерастворимые основанияСОЛЬ(р-р) + ЩЁЛОЧЬ = ОСНОВАНИЕ↓ + СОЛЬ
- 14. Химические ожоги, причиняемые щелочами, в том числе
- 15. Скачать презентацию
- 16. Похожие презентации
ОСНОВАНИЯ







![Презентация по химии Основания 8 класс ХИМИЧЕСКИЕ СВОЙСТВААмфотерные основанияZn(OH)2 + 2NaOH → Na2[Zn(OH)4] Аl(ОН)3 + NaOH = NaAlO2 + 2H2O2Al(OH)3 + Na2O → 2NaAlO2 + 3H2Oсплавлениев растворе](/img/tmb/7/609072/84adc0e1ddcbbb7f7ed986b8107b1dc4-720x.jpg)





Слайд 3 Основания – это сложные вещества, состоящие из атомов
металлов и одной или нескольких гидроксогрупп (ОН-).
Слайд 4
NaOH - гидроксид натрия
Zn(OH)2–гидроксид цинка
Cu(OH)2-гидроксид меди (II)
Названия
оснований складываются из слова "гидроксид" и названия металла. Если
металл проявляет переменную валентность, то в скобках указывается его валентность.НОМЕНКЛАТУРА
Слайд 5
ОСНОВАНИЯ
растворимые -
щелочи
нерастворимые
LiOH NaOH KOH RbOH CsOH
Ca(OH)2 Sr(OH)2 Ba(OH)2
Cu(OH)2 Zn(OH)2 Fe(OH)3 Fe(OH)2
КЛАССИФИКАЦИЯ
Слайд 6 Гидроксиды щелочных металлов – при обычных условиях представляют
собой твердые белые кристаллические вещества, гигроскопичные, мылкие на ощупь,
очень хорошо растворимы в воде (их растворение – экзотермический процесс), легкоплавки.Гидроксиды щелочноземельных металлов Са(ОН)2, Sr(OH)2, Ва(ОН)2 – белые порошкообразные вещества, гораздо менее растворимы в воде по сравнению с гидроксидами щелочных металлов.
Нерастворимые в воде основания обычно образуются в виде гелеобразных осадков, разлагающихся при хранении.
ФИЗИЧЕСКИЕ СВОЙСТВА
Слайд 8
ХИМИЧЕСКИЕ СВОЙСТВА
Щелочи
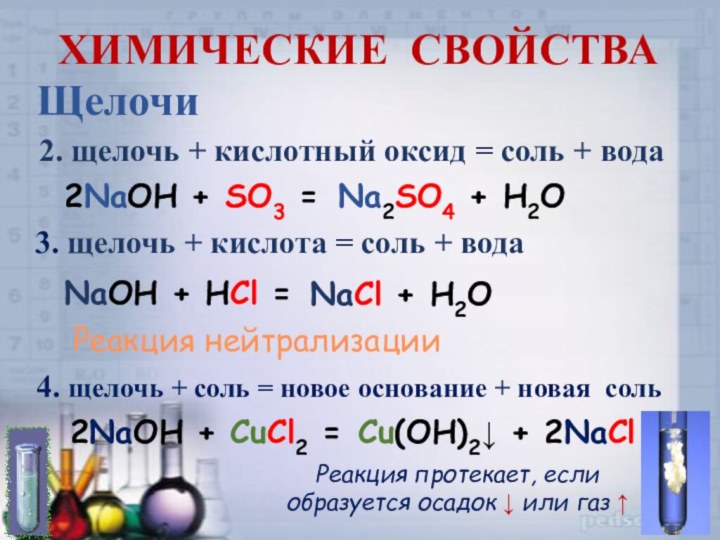
2. щелочь + кислотный оксид = соль
+ вода
2NaOH + SO3 =
Na2SO4 + H2O
3. щелочь +
кислота = соль + водаNaOH + HCl =
NaCl + H2O
Реакция нейтрализации
4. щелочь + соль = новое основание + новая соль
2NaOH + CuCl2 =
Cu(OH)2↓ + 2NaCl
Реакция протекает, если образуется осадок ↓ или газ ↑
Слайд 9
ХИМИЧЕСКИЕ СВОЙСТВА
Нерастворимые основания
1. нерастворимые основания разлагаются при нагревании
Cu(OH)2
→ CuO + H2O
При составлении формулы основного оксида, не
забудьте учесть валентность металла. Какова она в основании, такая же валентность металла будет и в оксиде.ll
2. нерастворимое основание + кислота = соль + вода
Cu(OH)2 + 2HCl =
CuCl2 + 2H2O
Слайд 10
ХИМИЧЕСКИЕ СВОЙСТВА
Амфотерные основания
Zn(OH)2 + 2NaOH → Na2[Zn(OH)4]
Аl(ОН)3 + NaOH = NaAlO2 +
2H2O
2Al(OH)3 + Na2O → 2NaAlO2 + 3H2O
сплавление
в растворе
Слайд 11
ХИМИЧЕСКИЕ СВОЙСТВА
Амфотерные основания
Zn(OH)2+2HCl = ZnCl2+2H2O
2Cr(OH)3 + 3SO3 =
Cr2(SO4)3 + 3H2O
Амфотерный
гидроксид
Кислотный
оксид
соль
вода
+
+
=
2Al(OH)3 → Al2O3 + 3H2O
Слайд 12
ПОЛУЧЕНИЕ
1. Металл + H2O = ЩЁЛОЧЬ + Н2↑
Здесь, Металл –
это щелочной металл (Li, Na, K, Rb, Cs) или щелочноземельный (Ca, Ba, Ra)
2. ОКСИД МЕТАЛЛА + H2O =
ЩЁЛОЧЬ Здесь, ОКСИД МЕТАЛЛА (основный оксид, растворимый в воде) – щелочного металла (Li, Na, K, Rb, Cs) или щелочноземельного (Ca, Ba, Ra)
2Na + 2H2O = 2 NaOH + H2
Слайд 14
Химические ожоги, причиняемые щелочами, в том числе едким
натром и едким кали, намного опаснее, чем химические ожоги
от кислот.Щёлочи способны разъедать много материалов, вызывать серьёзные ожоги на коже и слизистых оболочках, поражать глаза. Поэтому гидроксид натрия называют «едким натром», а гидроксид калия – «едким кали». При работе со щелочами и их растворами, нужно соблюдать осторожность. При попадании раствора щелочи на кожу, нужно сразу смыть его большим количеством воды. Затем обработать это место слабым раствором уксусной или борной кислоты. И опять промыть водой.
Осторожно щелочь !