- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему к уроку химии для 11 класса по теме Марганец
Содержание
- 2. Нахождение в природе Положение в ПСХЭ Физические свойства Химические свойства Получение Применение Соединения Mn?
- 3. MnO2пиролюзитMn2O4гаусманитMnO2 * Mn(OH)2манганитВ земной коре его 0,1 % от массыИндияБразилияАфрикаРоссия
- 4. хрупкий металл твердый т КИП
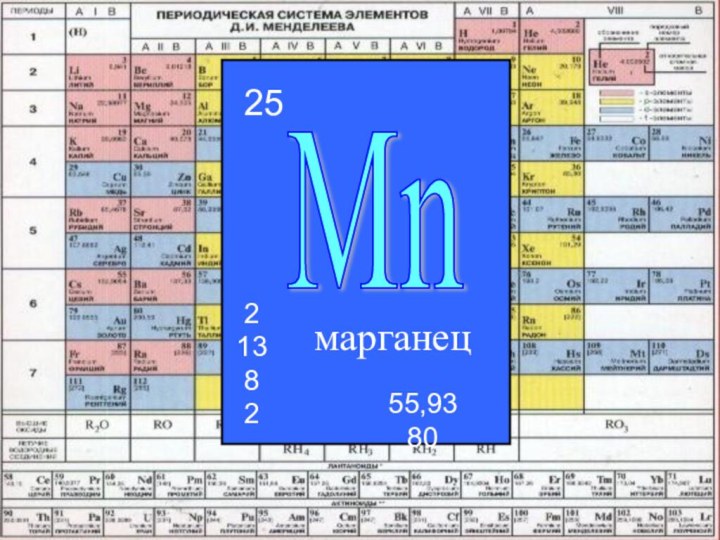
- 5. Mn5525+ 25 ) ) ) )1s²2 8 13 22s²2p3s²3p3d4s²N=1↓↑N=4N=3N=2↑↑↑↓↑↓↑↓↑↓↑↓↑↓↑↓↑↓↑↓↑↑↑4s+2, +3, +4, +6, +7n= 302665
- 6. Mn + O2 =MnO2Mn +S =Mn +
- 7. MnO+2Mn2O3MnO2Mn2O7Mn(OH)2Mn(OH)3, H2MnO3HMnO4ОсновныесвойстваАмфотерныесвойстваКислотныесвойства+3+4+7MnO3+6
- 8. Важнейшие соединенияПерманганаты:2 KMnO4 = K2MnO4 +MnO2 +O2Манганаты t
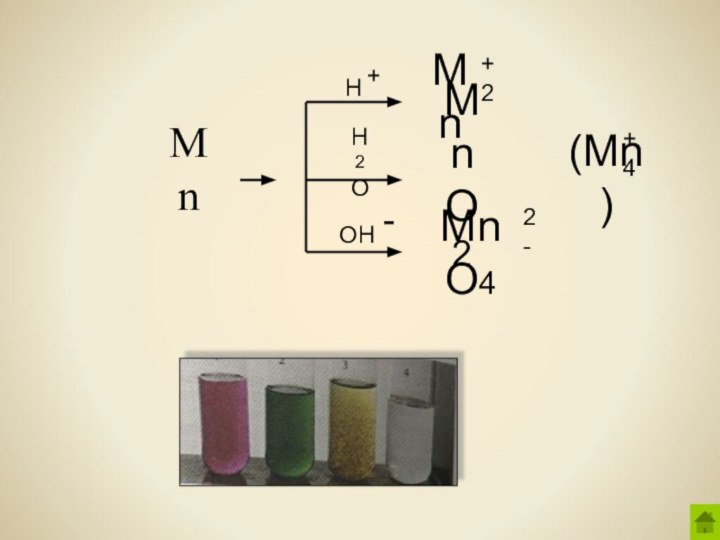
- 9. MnHH2OOHMn+2MnO2(Mn )+4MnO42-+-
- 10. Алюминотермия3MnO2+4AI=2AI2O3+3MnВ промышленности:Электролиз солей
- 12. MnMnOMnCl2Mn(OH)2MnOMnKMnO4O2X1X2X3Осуществите цепочки превращений:+S+O2+H2Ot?????
- 13. 1. БЖЕГ2. В3. В4. ДВГБ5. АВД6 )
- 14. Скачать презентацию
- 15. Похожие презентации
Нахождение в природе Положение в ПСХЭ Физические свойства Химические свойства Получение Применение Соединения Mn?












Слайд 3
MnO2
пиролюзит
Mn2O4
гаусманит
MnO2 * Mn(OH)2
манганит
В земной коре его 0,1 %
от массы
Индия
Бразилия
Африка
Россия
Слайд 4
хрупкий
металл
твердый
т КИП =
2150 º С
плотность = 7,44г/см³
Т ПЛАВ
= 1245 º С cеребристо-
белого цвета
с розовым
отливом
На воздухе покрывается оксидной пленкой
Mn
Слайд 5
Mn
55
25
+ 25
) ) ) )
1s²
2 8 13
2
2s²
2p
3s²
3p
3d
4s²
N=1
↓↑
N=4
N=3
N=2
↑
↑
↑
↓↑
↓↑
↓↑
↓↑
↓↑
↓↑
↓↑
↓↑
↓↑
↑
↑
4s
+2, +3, +4, +6, +7
n= 30
2
6
6
5
Слайд 7
MnO
+2
Mn2O3
MnO2
Mn2O7
Mn(OH)2
Mn(OH)3, H2MnO3
HMnO4
Основные
свойства
Амфотерные
свойства
Кислотные
свойства
+3
+4
+7
MnO3
+6
Слайд 13
1. БЖЕГ
2. В
3. В
4. ДВГБ
5. АВД
6 ) 3
MnCO3 +KClO3 = 3 MnO2 +KCl +3CO2
Mn MnCl Cl
+2
+4
+5
-1
-2e
+6e
3
1
- окисляется, восстановитель
- восстанавливается, окислитель
2KMnO4 +Na2SO3 +2 KOH = Na2SO4 +2 K2MnO4 + H2O
+2
+5
+4
-1
Mn Mn
S S
+7
+6
+4
+6
+1e
-2e
+7
+4
+6
+6
2
1
- восстанавливается, окислитель
- окисляется, восстановитель