кислотных свойств вещества над основными; 2) проявление веществом как кислотных,
так и основных свойств; 3) способность вещества диссоциировать с отщеплением как катиона водорода, так и гидроксид-аниона; 4) способность амфотерных веществ взаимодействовать друг с другом.Амфотерность - проявление веществом как кислотных, так и основных свойств:
Be(OH)2 + 2HCI → BeCI2 + 2H2O (основные свойства)
Be(OH)2 + 2NaOH → Na2[Be(OH)4] (кислотные свойства)
NH2 – CH2 – COOH + HCI → [NH3 – CH2 – COOH ]+CI- (основные свойства)
NH2 – CH2 – COOH + NaOH → NH2 – CH2 – COONa + H2O (кислотные свойства)
Ответ: 2






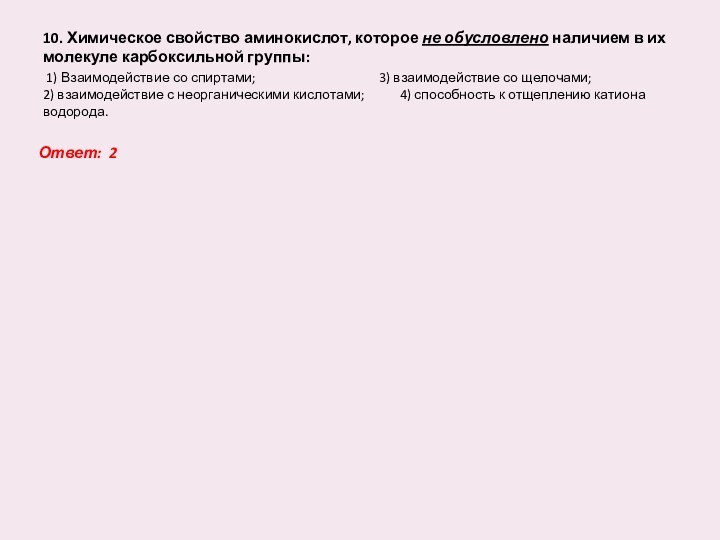
![АМФОРТНЫЕ НЕОРГАНИЧЕСКИЕ И ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ 6. К амфотерным гидроксидам не относят вещество, имеющее формулу: 1) Be(OH)2; 3) K2[Zn(OH)4];](/img/tmb/12/1155540/1571a42f8b16b6b177bad501bed58eb6-720x.jpg)







![АМФОРТНЫЕ НЕОРГАНИЧЕСКИЕ И ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ 15. Ионное уравнение реакции [Zn(OH)4]2- + 2Н+ = Zn(OH)2 + 2Н2О](/img/tmb/12/1155540/6a26ca4b1fef5f29f457de7d90df195d-720x.jpg)