Слайд 2
Цели урока
Образовательная:
Ознакомить обучающихся с природными полимерами – белками.
Изучить их строение, классификацию и свойства. Раскрыть биологическое значение
в жизни человека. Дать характеристику как важнейшим составляющим частям пищи.
Воспитательная:
Воспитывать позитивное отношении к химии.
Развивающая:
Развивать умение работать с постоянно увеличивающимся информационным потоком, развивать логическое мышление, самостоятельность суждений, формировать умение и навыки устной речи, мыслительные навыки, необходимые не только в учёбе, но и в повседневной жизни.
Слайд 3
Закончи предложения
Реакция получения анилина из нитробензола носит имя
………
Основные свойства аминокислот обусловлены
присутствием в молекуле – NH2. Что это?
Кислотные свойства аминокислот обусловлены присутствием в молекуле ……
Определить раствор анилина можно с помощью …….
Метиламин можно рассматривать как производное ……
Зинина
Аминогруппа
СООН
бромной воды
аммиака, в котором атомы водорода замещены углеводородными радикалами
Слайд 4
Белки в природе
Находятся в протоплазме и ядре всех
растительных и животных клеток, являются главными носителями жизни.
Альбумин (в
курином яйце)
Гемоглобин (в крови человека)
Казеин (в коровьем молоке)
Миоглобин и миозин (в мышцах)
– NH – CH – C – NH – CH – C – NH – CH –
│ ║ │ ║ │
R1 О R2 О R3
Слайд 5
Содержание белков в различных тканях человека
Мышцы до 80%
Лёгкие-72%
Кожа-63%
Печень-57%
Мозг-15%
Жировая
и костная ткани, зубы-14-28%
Слайд 6
В состав белков входят:
С – 50 – 52%;
Н – 6,0 – 8,0%;
О
– 19 – 24%;
N – 15 – 18%;
S – 0,5 – 2,0%.
Слайд 7
Классификация белков
Белки
простые
сложные
состоят только содержат белковую
из аминокислот и небелковую части
(альбумин, фибрин) (липиды, углеводы,
ионы металлов –
протеолипиды,
гемоглобин)
Слайд 8
Классификация белков
По растворимости:
1.Растворимые
2.Нерастворимые
По агрегатному состоянию:
1.Жидкие
2.Твердые
Слайд 9
Пептидная теория
В 1903 году немецкий ученый Э.Г.Фишер предложил
пептидную теорию, которая стала ключом к тайне строения белка.
Фишер предположил, что белки представляют собой полимеры из остатков аминокислот, соединенных пептидной связью NH–CO.
Идея о том, что белки – это полимерные образования, высказывалась еще в 1888 году русским ученым А.Я.Данилевским.
Слайд 10
Белок – это высокомолекулярное органическое соединение, представляющее собой
биополимер, состоящий из мономеров, которыми являются
α-аминокислоты соединенные пептидной связью.
Слайд 12
Свойства белков
При обработке хлоридом натрия белки высаливаются из
раствора. Этот процесс обратим.
Слайд 13
Гидратация белков
Водорастворимые белки образуют коллоидные растворы.
Слайд 14
Пенообразование
Процесс пенообразования–это способность белков образовывать высококонцентрированные системы «жидкость–газ»,называемые
пенами.
Белки в качестве пенообразователей широко используются в кондитерской
промышленности(пастила, зефир, суфле).
Структуру пены имеет хлеб, а это влияет на его вкусовые свойства.
Слайд 17
Цветные реакции белков
Ксантопротеиновая реакция
Поместите кусочек прессованного творога
в пробирку и добавьте несколько капель азотной кислоты. Осторожно
нагрейте.
Слайд 18
Биуретовая реакция
Налейте в пробирку
2 миллилитра яичного белка, 2 миллилитра концентрированного раствора гидроксида
натрия и несколько капель раствора сульфата меди (II).
Слайд 19
Горение белка
При горении животных белков ощущается характерный запах
«жжёного рога». В значительной степени этот запах определяется содержанием
серы в белках.
Растительных белков – запахом жженой бумаги.
Слайд 20
Функции белков (немного биологии)
транспортная
защитная
каталитическая
структурная
регуляторная
рецепторная
двигательная
энергетическая
Слайд 21
Транспортная функция
Заключается в связывании и доставке (транспорте) различных
веществ от одного органа к другому.
Гемоглобин соединяется в легких
с кислородом, превращаясь в оксигемоглобин.
Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород.
Слайд 22
Защитная функция
Антитела обезвреживают вещества, поступающие в организм или
появляющиеся в результате жизнедеятельности бактерий и вирусов.
Белок плазмы крови
фибриноген, участвуя в свертывании крови, уменьшает кровопотери
Слайд 23
Каталитическая функция
Заключается в увеличении скорости различных реакций
обмена веществ и энергии в организме.
Модель фермента
Слайд 24
Структурная функция
Гидролизованный коллаген (белок соединительной ткани)
Белки составляют основу
строения клетки.
Слайд 25
Регуляторная функция
Модель белка-регулятора (гормон)
Железы внутренней секреции
Слайд 26
Рецепторная функция
Белки-рецепторы служат для восприятия и преобразования различных
сигналов
(фоторецептор-родопсин).
Слайд 27
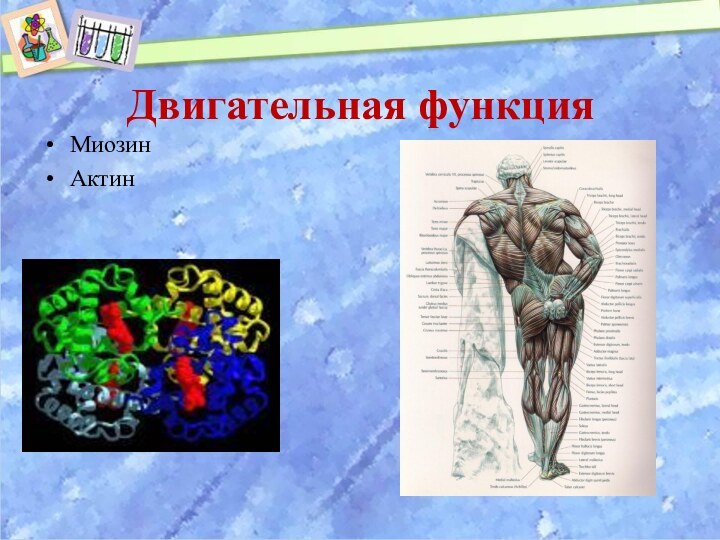
Двигательная функция
Миозин
Актин
Слайд 28
Энергетическая функция
1 г белка эквивалентен 17,6 кДж.
Слайд 30
Суточная норма потребления белка
0,85-1,00 граммов на килограмм
веса для взрослого человека (около 100 граммов в сутки
для среднего мужчины и 70 граммов для женщины).
Детям требуется больше белка - до 1,9 граммов на килограмм веса в сутки.
Слайд 31
Значение белков
Изучение белков важно для выяснения природы заболеваний,
наблюдаемых у человека и животных.
Отдельные белки находят применение
в народном хозяйстве( шерсть, шёлк, кожа , перья, волосы и рога).
Выведения новых высокопродуктивных пород животных и сортов растений.
Развитие направлений современной биоорганической химии - генной инженерии и биотехнологии
Слайд 32
Тест по теме «Белки»
1) Белки это:
а)
искусственные волокна в) природные высокомолекулярные соединения
б)
синтетические волокна г) природные низкомолекулярные соединения
2) Минимальное содержание белка отмечено в:
а) кишечнике б) зубах в) костях г) мышцах
3) Молекулярная масса белков колеблется:
а) от нескольких единиц до нескольких десятков
б) от нескольких десятков до нескольких сотен
в) от нескольких сотен до нескольких тысяч
г) от нескольких тысяч до нескольких миллионов
Слайд 33
Тест по теме «Белки»
4) В состав белков НЕ
входит:
а) азот б) стронций в) фосфор г) сера
5)
Защитная роль белков в организме выражается в:
а) осуществлении всех жизненных процессов
б) доставке кислорода из легких в ткани
в) ускорении многих химических реакций
г) обезвреживании чужеродных веществ
Слайд 34
Тест по теме «Белки»
6) В результате гидролиза природных
белков получается:
а) смесь 20 аминокислот
б) смесь бета-аминокислот
в) смесь различных альфа-аминокислот
г) смесь альфа- и бета-аминокислот
7) Первичная структура белка отражает:
а) последовательность соединения аминокислотных звеньев в полипептидной цепи
б) пространственную конфигурацию полипептидной цепи
в) объем, форму и взаимное расположение участков полипептидной цепи
г) ассоциацию белковых молекул
Слайд 35
Тест по теме «Белки»
8) Вторичная структура белка
поддерживается:
а) ковалентными полярными связями
б) водородными связями между >C=O
и >NH группами
в) водородными связями и дисульфидными мостиками
г) ионными связями
9) Биологическую активность белковой молекулы обуславливает структура:
а) первичная б) вторичная в) третичная г) четверичная
10) Гидролиз белков в организме человека происходит под влиянием:
а) ферментов б) температуры тела
в) температуры окружающей среды г) давления крови
Слайд 36
Проверь себя
В
Б
Г
Б
Г
В
А
Б
В
А
Критерии оценки:
нет ошибок - 5
2 ошибки
- 4
3 - 4 ошибки - 3
более 4 ошибок
- 2
Слайд 37
Ответьте на вопросы:
В чем причина несовместимости тканей
при пересадке органов от одного организма к другому?
Научное
название белков.
Из чего построены молекулы белков?
Сколько структур белка существует?
Структура белка, свернутая в спираль?
Как называется четвертичная структура белка?
Как называется связь - NH – CO - ?
Разрушение структуры белка.
Реакции, определяющие наличие белка?
Пищевые продукты с большим содержанием белка.
Самая неустойчивая структура белка?
Для каждого организма характерен свой
индивидуальный набор белков
протеины
Из остатков аминокислот
4
вторичная
глобула
пептидная
денатурация
Ксантопротеиновая, биуретовая
четвертичная