и неэлектролиты.
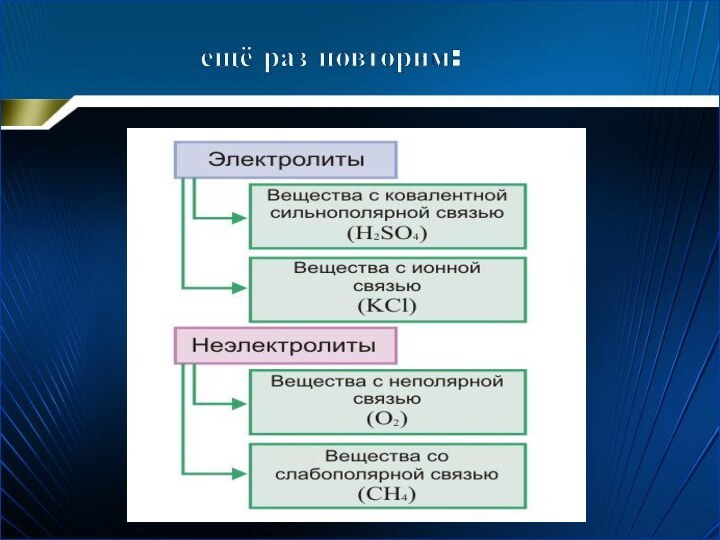
Электролитами называют вещества, растворы или расплавы которых проводят
электрический ток. К ним относится большинство неорганических веществ, например, кислоты, основания, соли, оксиды металлов. Для электролитов характерны ионные или ковалентные полярные связи.Неэлектролитами называются вещества, которые не проводят электрический ток ни в растворах, ни в расплавах. Сюда относится большинство органических веществ (спирт, ацетон, бензин, сахар, масло и другие) и некоторые неорганические вещества (дистиллированная вода, углекислый газ, кислород). Для неэлектролитов характерны ковалентные неполярные или малополярные химические связи.
Электролиты и неэлектролиты