- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Электролиз. Электролит
Содержание
- 2. Электролизом называют совокупность окислительно-восстановительных процессов, происходящих на электродах под действием постоянного электрического тока.
- 3. ЭЛЕКТРОЛИЗЕР – электрохимическая ячейка, в которой проводят электролиз растворов или расплавов веществ.
- 4. СОСТАВ ЭЛЕКТРОЛИЗЕРА ЭЛЕКТРОЛИТ – раствор или расплав
- 5. АНОД – электрод, который подключен к
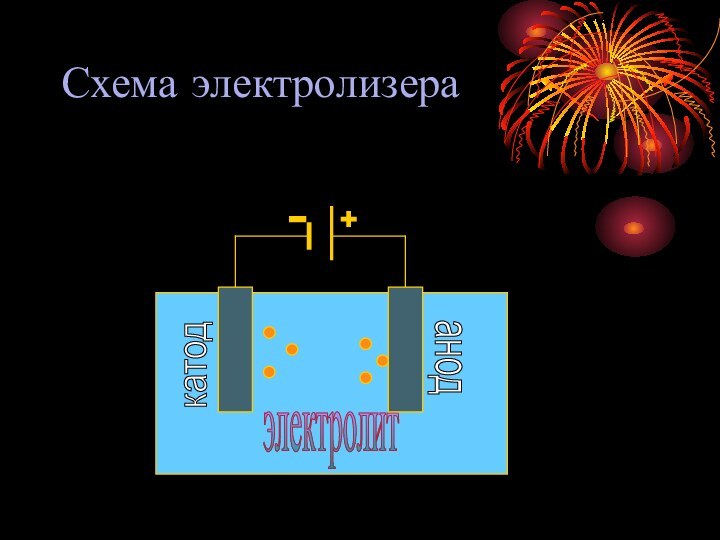
- 6. Схема электролизераанодкатодэлектролит
- 7. ЭЛЕКТРОЛИЗ РАСПЛАВОВПРИМЕР: схема электролиза расплава хлорида магния
- 8. КАТОД (-) : процесс восстановленияMg +
- 9. ЭЛЕКТРОЛИЗ РАСТВОРОВ В данном случае в
- 10. Возможные процессы на катодеЕсли металл расположен в
- 11. 2. Если металл расположен от начала ряда
- 12. 3. Если металл расположен в ряду напряжений
- 14. Возможные процессы на анодеЕсли анод растворимый (Fe,
- 15. 2. Если анод не растворяется (инертный –
- 16. ПРИМЕР: схема электролиза раствора сульфата магния MgSO4В
- 17. Скачать презентацию
- 18. Похожие презентации
Электролизом называют совокупность окислительно-восстановительных процессов, происходящих на электродах под действием постоянного электрического тока.
















Слайд 2 Электролизом называют совокупность окислительно-восстановительных процессов, происходящих на электродах
под действием постоянного электрического тока.
Слайд 3 ЭЛЕКТРОЛИЗЕР – электрохимическая ячейка, в которой проводят
электролиз растворов или расплавов веществ.
Слайд 4
СОСТАВ ЭЛЕКТРОЛИЗЕРА
ЭЛЕКТРОЛИТ – раствор или расплав вещества,
который проводит электрический ток вследствие распада молекул данного вещества
на ионы (катионы и анионы)Слайд 5 АНОД – электрод, который подключен к положительному
полюсу источника питания (ПРОЦЕСС ОКСИЛЕНИЯ)
КАТОД - электрод, который
подключен отрицательному полюсу источника питания (ПРОЦЕСС ВОССТАНОВЛЕНИЯ)
Слайд 7
ЭЛЕКТРОЛИЗ РАСПЛАВОВ
ПРИМЕР: схема электролиза расплава хлорида магния MgCl2
В
расплаве данного электролита
содержатся ионы: Mg и
Сl.Катионы Mg движутся к катоду, а
анионы Сl - к аноду
2+
-
2+
-
Слайд 8
КАТОД (-) : процесс восстановления
Mg + 2e
Mg
АНОД (+) : процесс
окисления2Сl - 2e Cl2
MgCl2 Mg + Cl2
2+
-
Слайд 9
ЭЛЕКТРОЛИЗ РАСТВОРОВ
В данном случае в окислительно-восстановительных
процессах, происходящих на электродах возможно участие молекул ВОДЫ (Н2О)
Слайд 10
Возможные процессы на катоде
Если металл расположен в ряду
напряжений после водорода (Cu, Hg, Ag, Pt, Au), то
восстанавливаются катионы данного металлаСu + 2e Cu
2+
Слайд 11 2. Если металл расположен от начала ряда напряжений
до Al включительно (Li, Na, K, Mg и др.),
то на катоде происходит процесс восстановления молекул Н2О:2Н2О + 2е H2 + 2OH
Слайд 12 3. Если металл расположен в ряду напряжений между
Al и водородом (Zn, Fe, Ni, Mn и др.),
то на катоде происходят процессы восстановления молекул Н2О и ионов данного металла:2Н2О + 2е H2 + 2OH
Zn + 2e Zn
2+
Слайд 14
Возможные процессы на аноде
Если анод растворимый (Fe, Zn,
Al, Сu и др.), то окисляется металл анода, несмотря
на природу аниона:Сu - 2e Cu
2+
Слайд 15 2. Если анод не растворяется (инертный – графит,
Au, Pt и др.), то:
анионы, не содержащие кислород (F
, Cl , S и др.), окисляются на аноде2Cl - 2e Cl2
анионы, содержащие кислород
(SO4 , NO3 и др.) не окисляются на аноде, а окисляются молекулы воды
2Н2О - 4е O2 + 4H
-
-
2-
-
2-
-
+
Слайд 16
ПРИМЕР: схема электролиза раствора сульфата магния MgSO4
В растворе
существуют ионы Mg и SO4
КАТОД (-) : процесс
восстановления2Н2О + 2е H2 + 2OH 2
АНОД (+) : процесс окисления
2Н2О - 4е O2 + 4H 1
2MgSO4 + 6Н2О 2 H2 + O2 + 2Mg(OH)2 + 2H2SO4
2+
2-
-
+