- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Электронное строение атомов элементов
Содержание
- 2. ПовторениеЧисло электронов в атоме элемента = числу
- 3. ПовторениеЧисло электронов в наружном слое атомов элементов
- 4. Распределение электронов по уровнямN=2n2 формула для вычисления
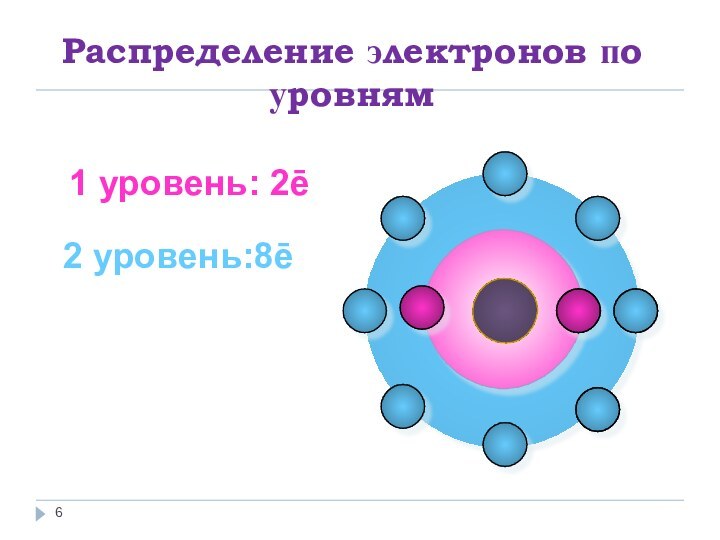
- 5. Распределение электронов по уровням1 уровень:2ē
- 6. Распределение электронов по уровням1 уровень: 2ē2 уровень:8ē
- 7. Распределение электронов по уровням1 уровень-22 уровень-83 уровень-18
- 8. Распределение электронов по уровням281832
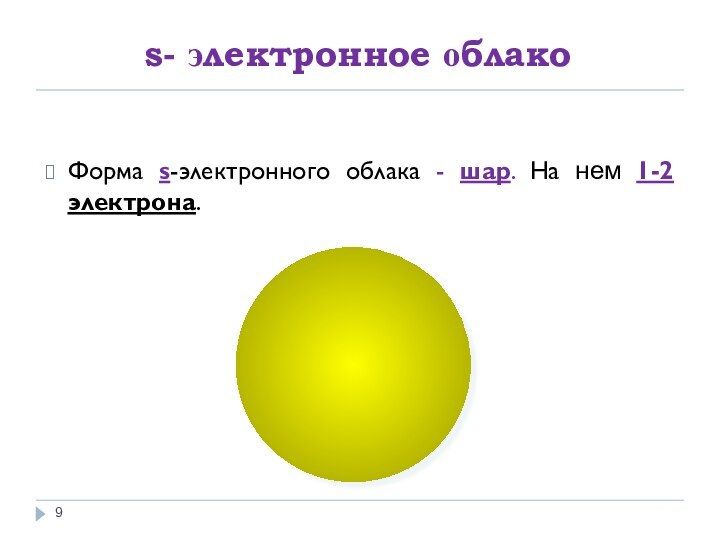
- 9. s- электронное облакоФорма s-электронного облака - шар. На нем 1-2 электрона.
- 10. p- электронное облакоФорма p-электронного облака - объёмная восьмёрка. На нем от 1 до 6 электронов.
- 11. d- электронное облакоФорма d-электронных облаков - две объемные восьмёрки. На нем от 1 до 10 электронов.
- 12. f- электронное облакоФорма f-электронных облаков сложная и
- 13. Атом водородаЭлектрон этого атома при вращении образует
- 14. Атом гелия+2 Не )2 это схема
- 15. Атом лития+3 Li )2)1 это схема строения
- 16. Атом бериллия+4 Be )2 )2 это схема
- 17. Атом углерода+6 С ) 2 ) 4
- 18. Атом хлора+17 Cl )2 )8 )7 схема
- 19. ЗаключениеСуществуют s, p, d, f электроны. Электроны
- 20. Скачать презентацию
- 21. Похожие презентации
ПовторениеЧисло электронов в атоме элемента = числу протонов = заряду ядра атома = порядковому номеру элемента.Электроны в атомах располагаются слоями; число слоёв (энергетических уровней) = номеру периода, в котором находится элемент.














Слайд 2
Повторение
Число электронов в атоме элемента = числу протонов
= заряду ядра атома = порядковому номеру элемента.
атомах располагаются слоями; число слоёв (энергетических уровней) = номеру периода, в котором находится элемент.
Слайд 3
Повторение
Число электронов в наружном слое атомов элементов =
номеру группы, в котором находится элемент. (Для элементов главных
подгрупп)Электроны движутся вокруг ядра с огромной скоростью по орбиталям. Часть пространства, где наиболее вероятно нахождение электрона, называют электронным облаком.
Слайд 4
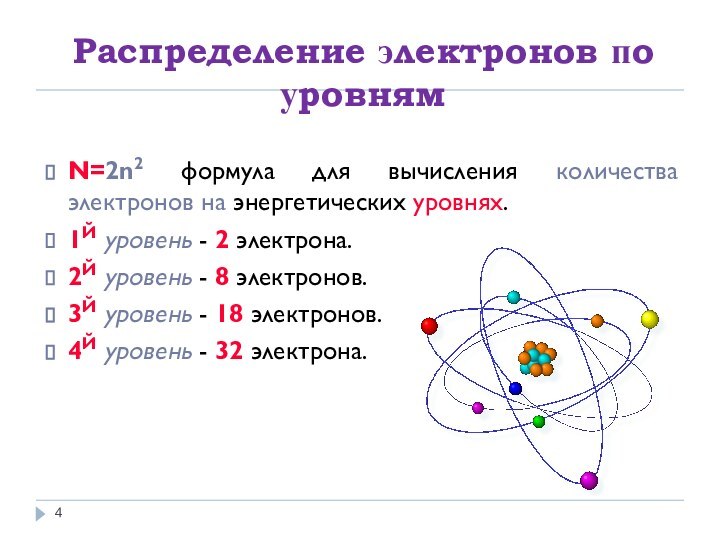
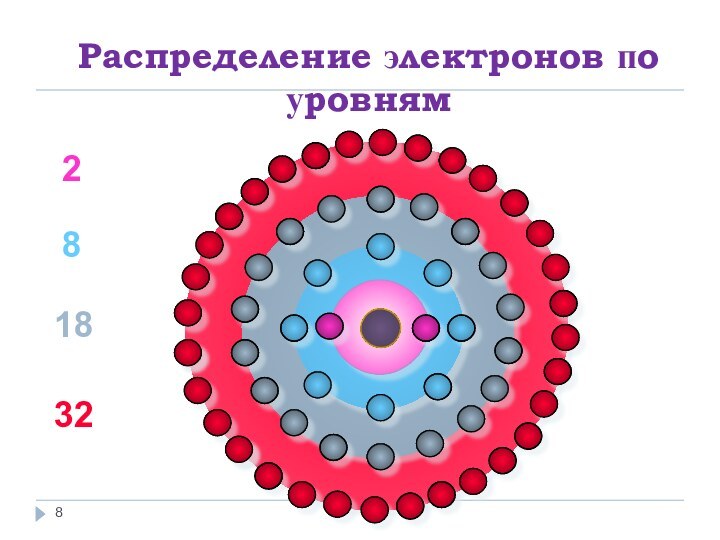
Распределение электронов по уровням
N=2n2 формула для вычисления количества
электронов на энергетических уровнях.
1Й уровень - 2 электрона.
2Й уровень
- 8 электронов.3Й уровень - 18 электронов.
4Й уровень - 32 электрона.
Слайд 10
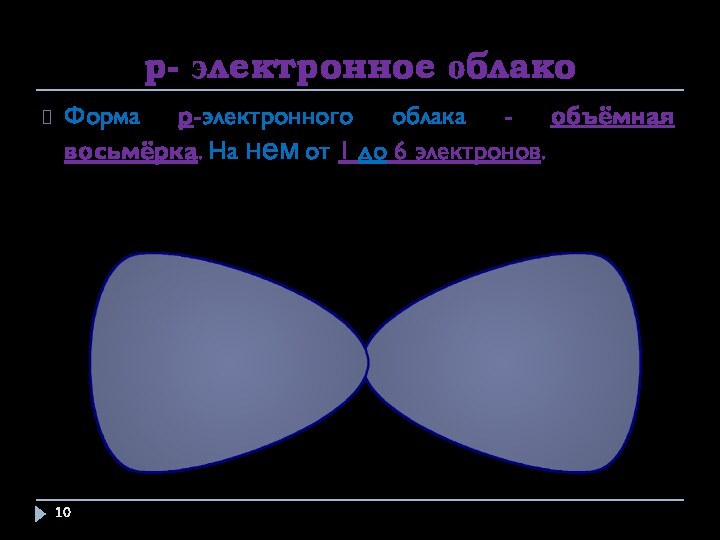
p- электронное облако
Форма p-электронного облака - объёмная восьмёрка.
На нем от 1 до 6 электронов.
Слайд 11
d- электронное облако
Форма d-электронных облаков - две объемные
восьмёрки. На нем от 1 до 10 электронов.
Слайд 12
f- электронное облако
Форма f-электронных облаков сложная и в
школьных учебниках не приводится. На них от 1 до
14 электронов.
Слайд 13
Атом водорода
Электрон этого атома при вращении образует сферическое
облако.
+1 Н )1 это схема строения атома. Здесь на
первом месте - заряд ядра, на втором месте - химическое обозначение, далее - одна орбиталь и электроны на ней.1s1 это электронная формула атома.
Слайд 14
Атом гелия
+2 Не )2 это схема строения
атома.
1s2 это электронная формула атома.
Здесь два s-электрона. Облака их
одинаковой формы и при совмещении образуют общее двухэлектронное облако.Про такие электроны говорят, что они спарены.
Слайд 15
Атом лития
+3 Li )2)1 это схема строения атома.
1s2
2s1 это электронная формула.
Элемент располагается во втором периоде,
имеет два электронных слоя.
Слайд 16
Атом бериллия
+4 Be )2 )2 это схема строения
атома.
1s2 2s2 это электронная формула.
В этом атоме имеется
два спаренных s-электрона во внутреннем слое и два спаренных s-электрона в наружном.
Слайд 17
Атом углерода
+6 С ) 2 ) 4 схема
строения атома.
1s2 2s 2 2p2 электронная формула.
В обычном состоянии
атом углерода двухвалентен. 1s2 2s 1 2p3
В возбужденном состоянии (получил дополнительное количество энергии) атом углерода четырёхвалентен.
Слайд 18
Атом хлора
+17 Cl )2 )8 )7 схема строения
атома.
1s2 2s2 2p6 3s2 3p5 это электронная формула.
Атом располагается
в III периоде, и имеет три энергетических уровня.Атом располагается в VII группе, главной подгруппе - на внешнем энергетическом уровне 7 электронов.