- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Признаки реакций
Содержание
- 2. Девиз урока: “Химик не такой должен быть, который
- 3. ПРОБЛЕМА: Реакцию можно увидеть, что она произошла, по различным признакам. Какие Признаки реакции?
- 4. ПОВТОРЕНИЕ!
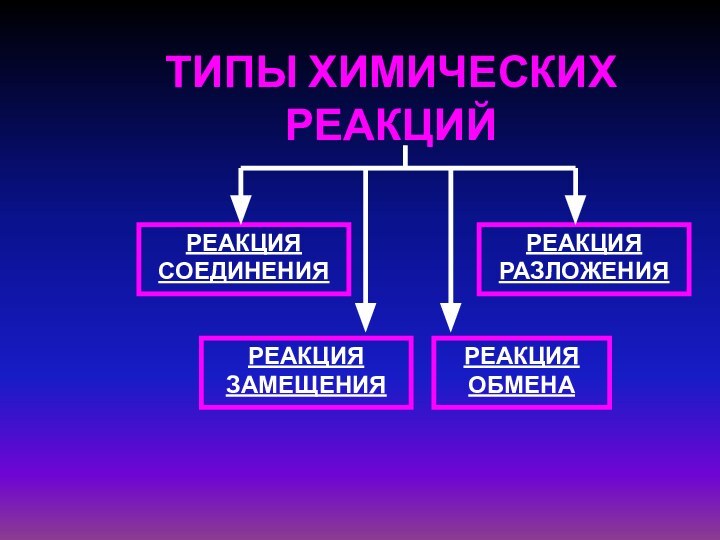
- 5. ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙРЕАКЦИЯ СОЕДИНЕНИЯРЕАКЦИЯ РАЗЛОЖЕНИЯРЕАКЦИЯ ЗАМЕЩЕНИЯРЕАКЦИЯ ОБМЕНА
- 6. CaO + CO2 = CaCO3CO2 + 2NaOH
- 7. CaO + CO2 = CaCO3CO2 + 2NaOH
- 8. 2HgO = 2Hg + O2CaCO3 = CaO
- 9. 2H2O2 = 2H2O + O2H2SO4+Fe(OH)2=FeSO4+2H2OBaO + SO2 = BaSO32HNO3+СuO=Cu(NO3)2+H2OH2SO4+2KOH=K2SO4+2H2O2Na + H2SO4 =Na2SO4+H2↑CaCO3 = CaO + CO2
- 10. ВНИМАНИЕ!Помни! Об этом Знает любая кроха: Безопасность- хорошо, А халатность- плохо!
- 11. Не спеши хватать прибор ты,А инструкцию читай.Убедись,
- 12. Пусть в пробирке пахнет воблой,В колбе- будто
- 13. Скажи мне – и я забуду,Покажи мне
- 14. Скачать презентацию
- 15. Похожие презентации
Девиз урока: “Химик не такой должен быть, который дальше дыму и пеплу ничего не видит, а такой, который на основании опытных данных может делать теоретические выводы” М.В.Ломоносов













Слайд 3
ПРОБЛЕМА:
Реакцию можно увидеть, что она произошла, по различным
признакам.
Какие
Признаки
реакции?
Слайд 6
CaO + CO2 = CaCO3
CO2 + 2NaOH =
Na2CO3 + H2O
Fe + S = FeS
2H2O = 2H2
+ O2CuO + H2 = Cu + H2O
Zn + 2HCl = ZnCl2 + H2↑
ZnO + H2SO4 = ZnSO4 + H2O
Cu(OH)2 = CuO + H2O
Слайд 7
CaO + CO2 = CaCO3
CO2 + 2NaOH =
Na2CO3 + H2O
Fe + S = FeS
2H2O = 2H2
+ O2↑CuO + H2 = Cu + H2O
Zn + 2HCl = ZnCl2 + H2↑
ZnO + H2SO4 = ZnSO4 + H2O
Cu(OH)2 = CuO + H2O
Слайд 8
2HgO = 2Hg + O2
CaCO3 = CaO +
CO2
CuSO4 + Fe = Cu + FeSO4
CuO + H2
= Cu + H2O2H2 + O2 = 2H2O
H2SO4 + 2KOH = K2SO4 + 2H2O
BaO + SO2 = BaSO3
Слайд 9
2H2O2 = 2H2O + O2
H2SO4+Fe(OH)2=FeSO4+2H2O
BaO + SO2 =
BaSO3
2HNO3+СuO=Cu(NO3)2+H2O
H2SO4+2KOH=K2SO4+2H2O
2Na + H2SO4 =Na2SO4+H2↑
CaCO3 = CaO + CO2
Слайд 11
Не спеши хватать прибор ты,
А инструкцию читай.
Убедись, что
ты все понял,
Вот тогда и начинай.
Если хочешь долго жить,
Надо
медленно спешить.Помни: щелочь,кислота
Вмиг прожгут одежду всем.
Надевай халат, как я,
И работай без проблем.
Слайд 12
Пусть в пробирке пахнет воблой,
В колбе- будто мармелад.
Вещества
на вкус не пробуй!
Сладко пахнет даже яд.
Как же нюхать
вещества?В колбу нос совать нельзя!
Что может случиться?
Ты можешь отравиться!





























