- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Реакции ароматического нуклеофильного замещения
Содержание
- 2. Реакции ароматического нуклеофильного замещения
- 3. Реакции SNArAr-B + C- ArC + B-
- 4. Ароматические соединения Характерны реакции замещения, в первую
- 5. Нуклеофильное замещение в ароматических и гетероароматических системах
- 6. SNArнуклеофуги - уходящие частицы: Hal-, RO-, NO2-
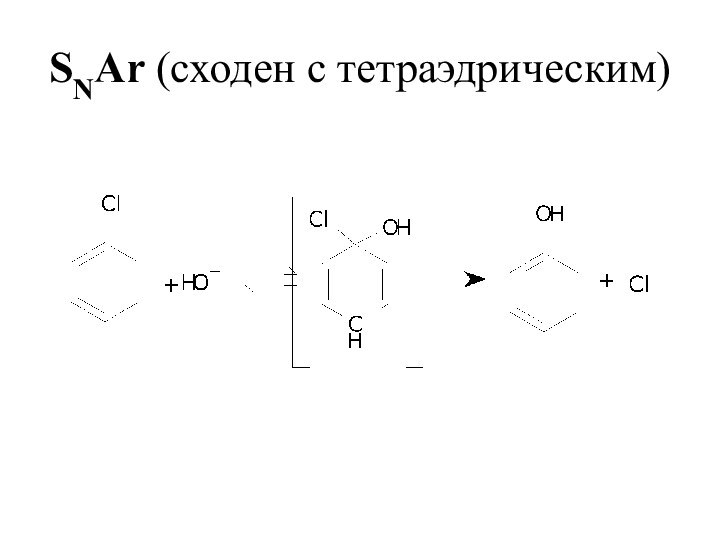
- 7. SNAr (сходен с тетраэдрическим)
- 8. SNArУскоряется в присутствии электроноакцепторных заместителей (особенно в
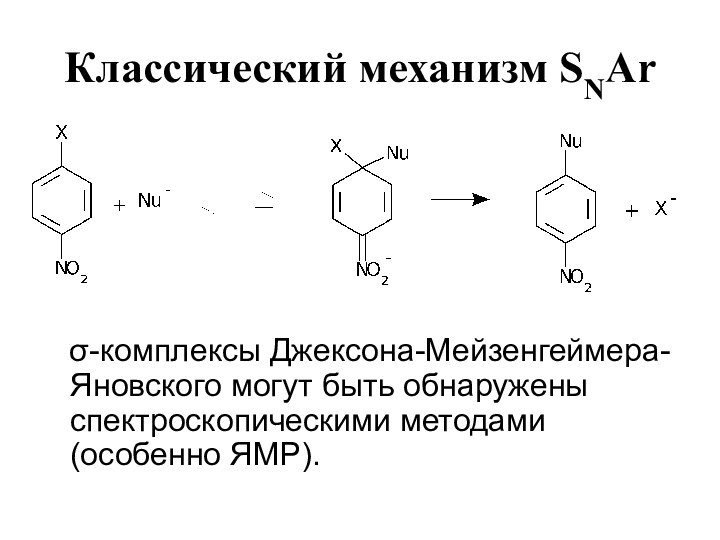
- 9. Классический механизм SNAr -комплексы Джексона-Мейзенгеймера-Яновского могут быть обнаружены спектроскопическими методами (особенно ЯМР).
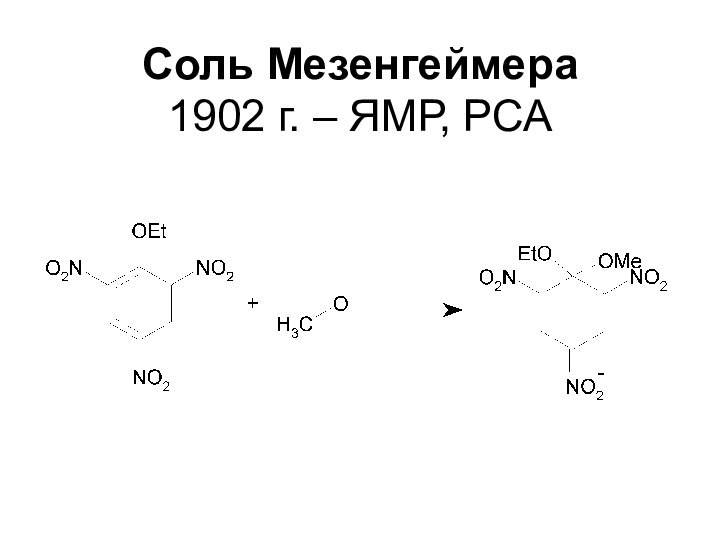
- 10. Соль Мезенгеймера 1902 г. – ЯМР, РСА
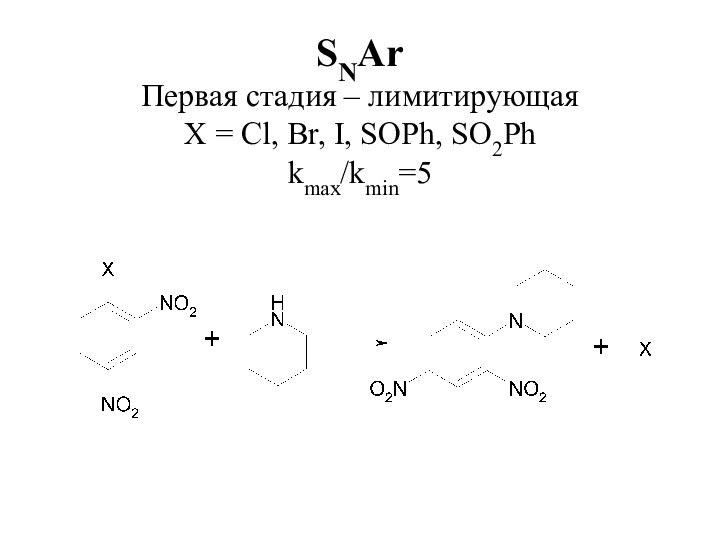
- 11. SNAr Первая стадия – лимитирующая X = Cl, Br, I, SOPh, SO2Ph kmax/kmin=5
- 12. SNAr Реакционная способность уходящих групп F,
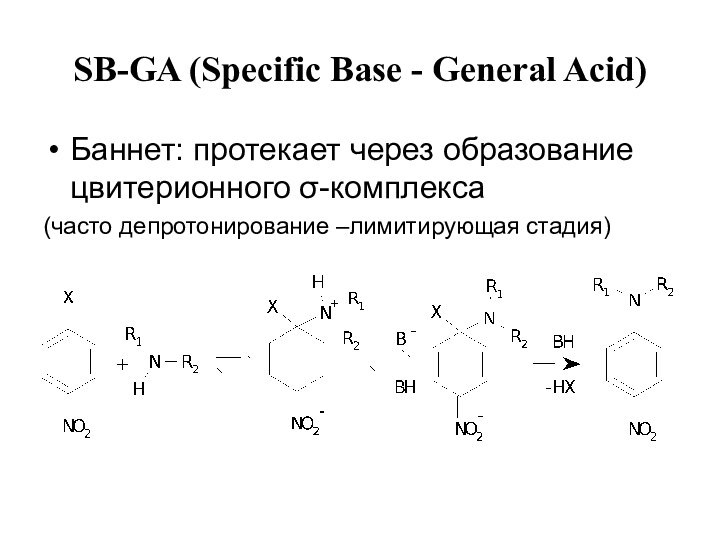
- 13. SB-GA (Specific Base - General Acid) Баннет: протекает через образование цвитерионного -комплекса (часто депротонирование –лимитирующая стадия)
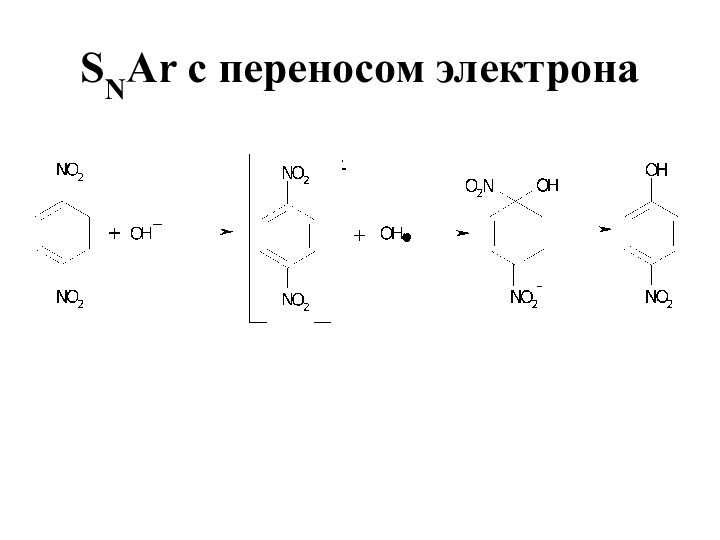
- 14. SNAr с переносом электрона Присутствие радикалов было доказано методом ЭПР
- 15. SNAr с переносом электрона
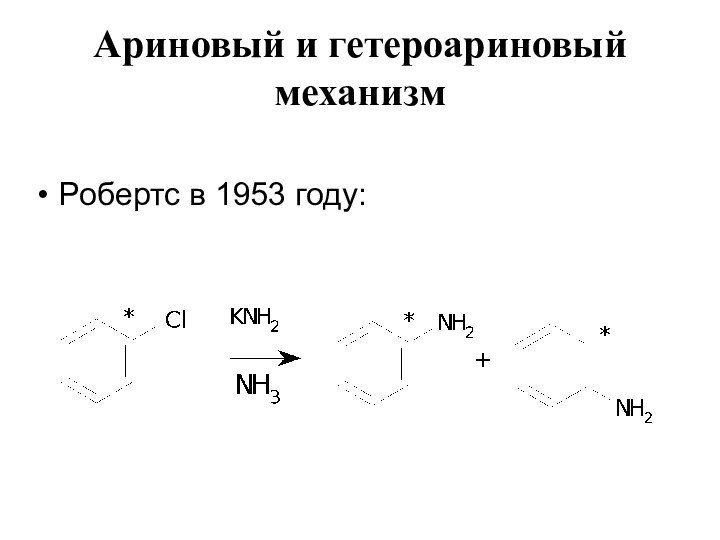
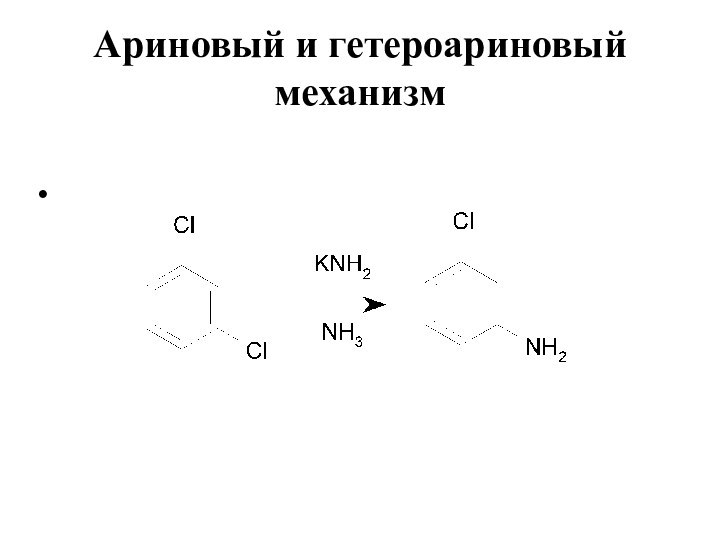
- 16. Ариновый и гетероариновый механизм Робертс в 1953 году:
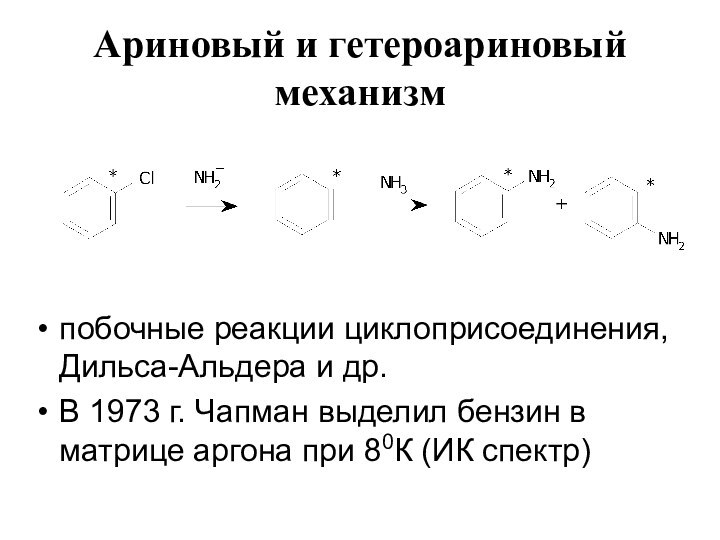
- 17. Ариновый и гетероариновый механизм побочные реакции циклоприсоединения,
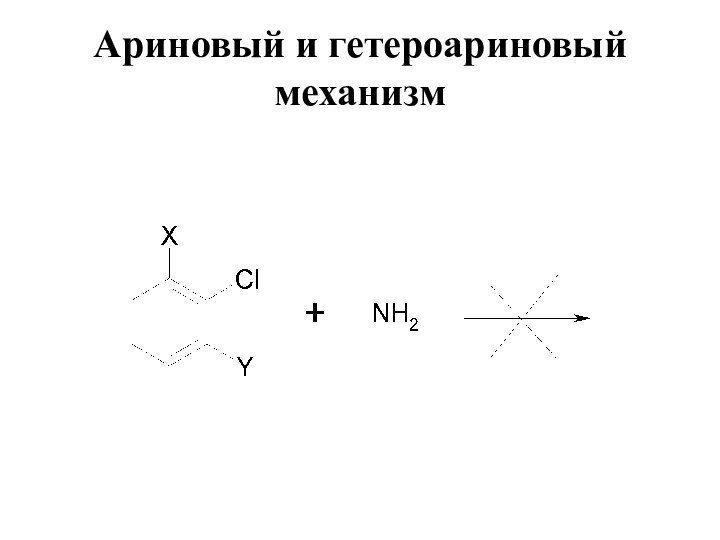
- 18. Ариновый и гетероариновый механизм
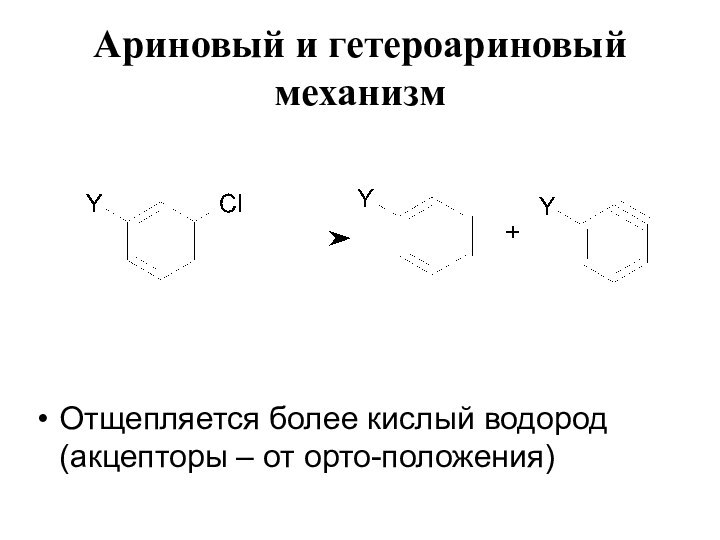
- 19. Ариновый и гетероариновый механизм Отщепляется более кислый водород (акцепторы – от орто-положения)
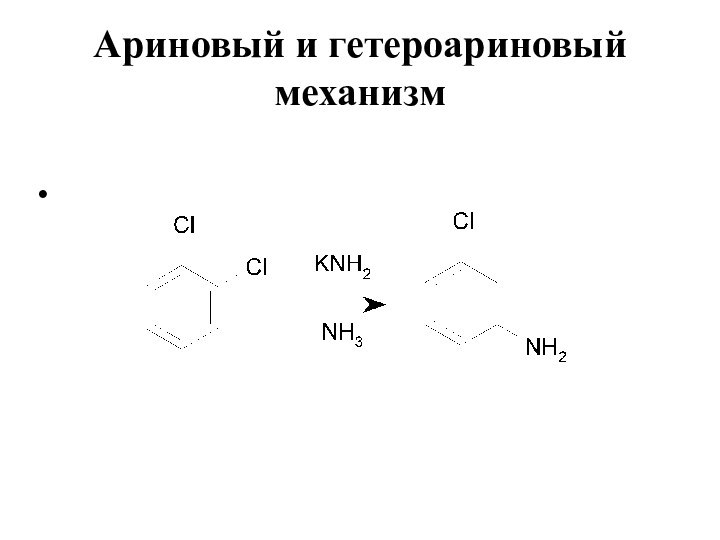
- 20. Ариновый и гетероариновый механизм
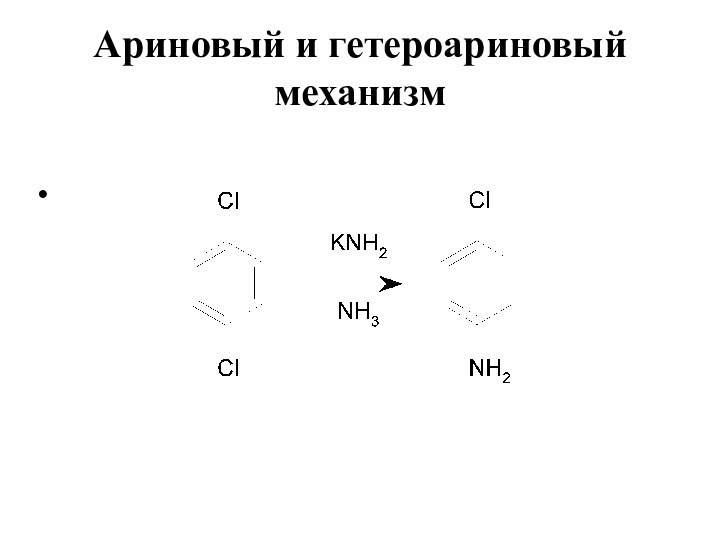
- 21. Ариновый и гетероариновый механизм
- 22. Ариновый и гетероариновый механизм
- 23. Механизм SRN1Баннет и Ким1970 г.
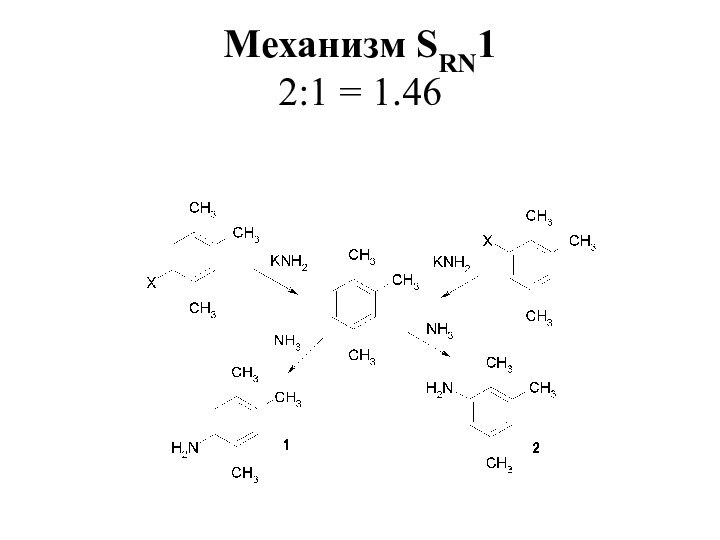
- 24. Механизм SRN1 2:1 = 1.46
- 25. Механизм SRN1Для йода2:1 = 0.63 или 2:1
- 26. SRN1ArX + e [ArX]-.[ArX]-. Ar.
- 27. SRN1Не нужна активация сильно электроноакцепторными группамиОтсутствует чувствительность к стерическим препятствиямЭффективно фотостимулирование или электрохимическое инициирование
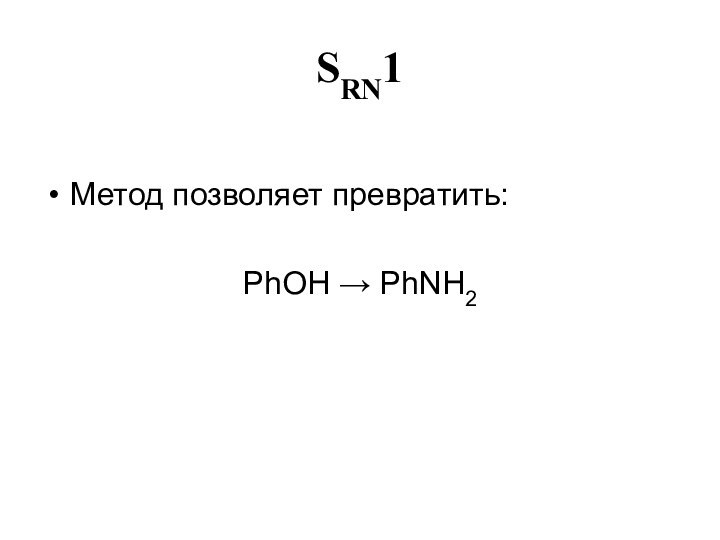
- 28. SRN1Метод позволяет превратить:PhOH PhNH2
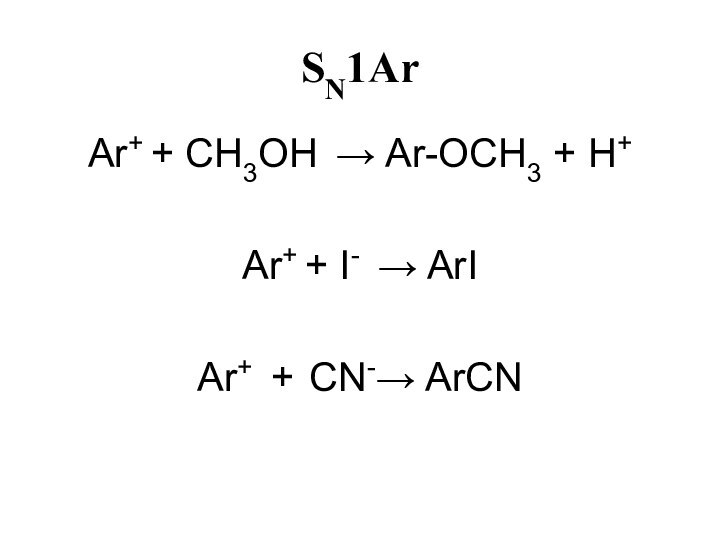
- 29. SN1Ar ArN2+ N2 +
- 30. SN1Ar Ar+ + CH3OH Ar-OCH3 + H+Ar+ + I- ArIAr+ + CN- ArCN
- 31. SN1Ar1) Скорость не зависит от [Nu]2) Влияние
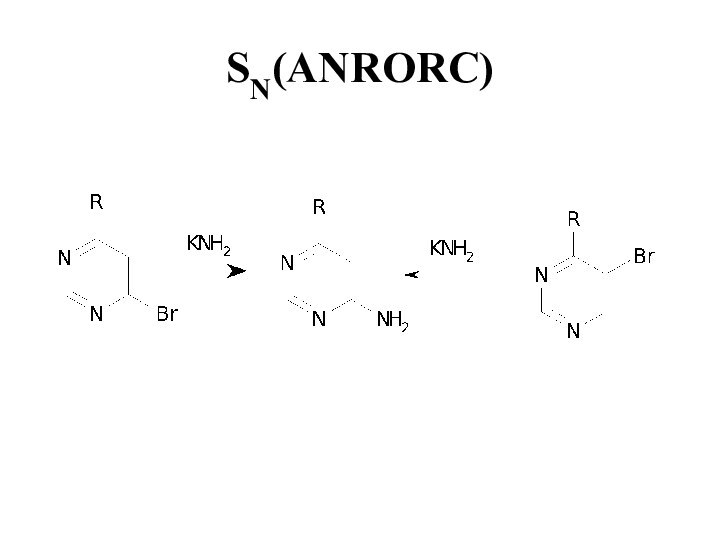
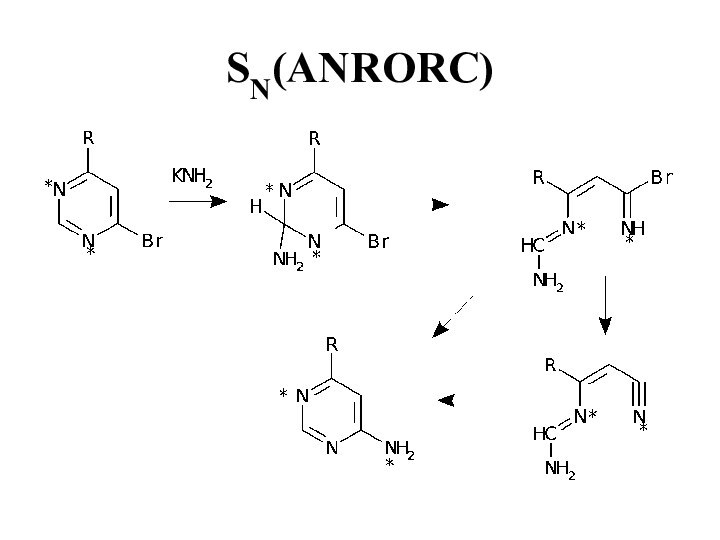
- 32. SN(ANRORC) Этот механизм был открыт Ван-дер-Плассом в
- 33. SN(ANRORC)
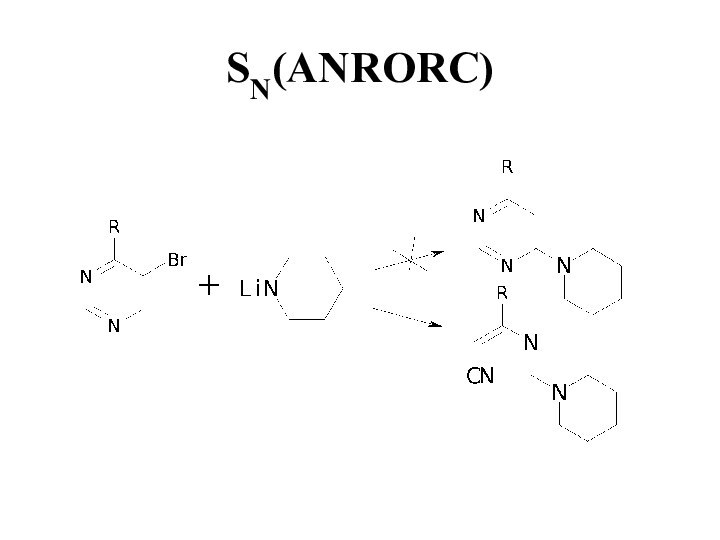
- 34. SN(ANRORC)
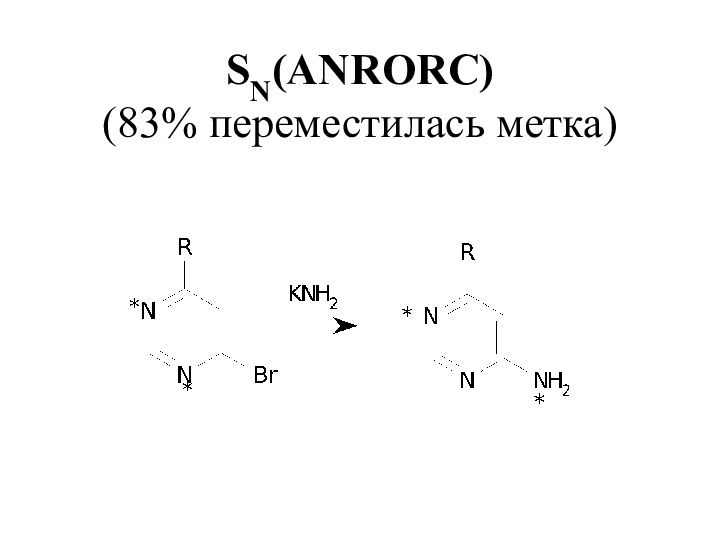
- 35. SN(ANRORC) (83% переместилась метка)
- 36. SN(ANRORC)
- 37. Замещение гидроксигруппы
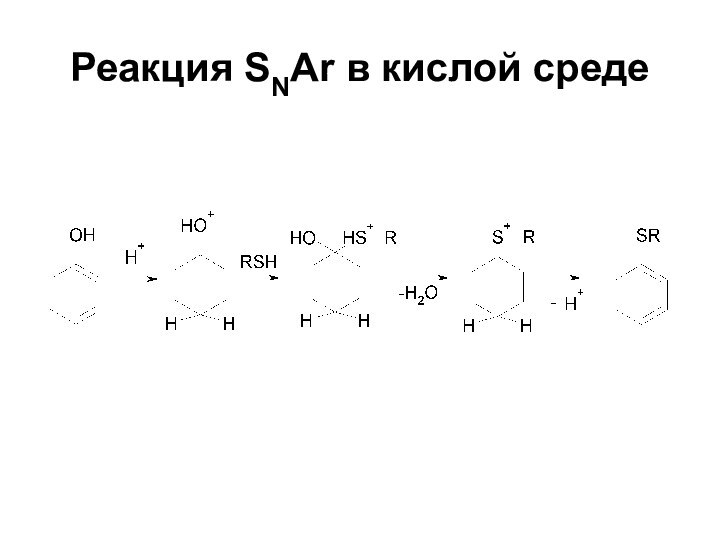
- 38. Реакция SNAr в кислой среде
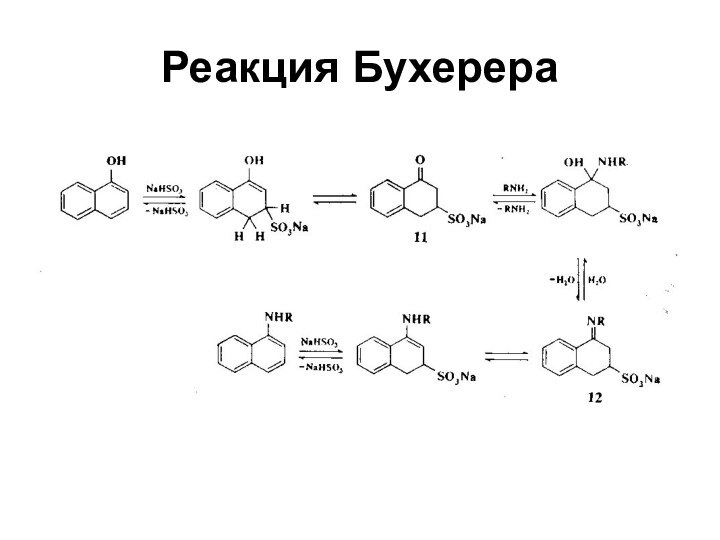
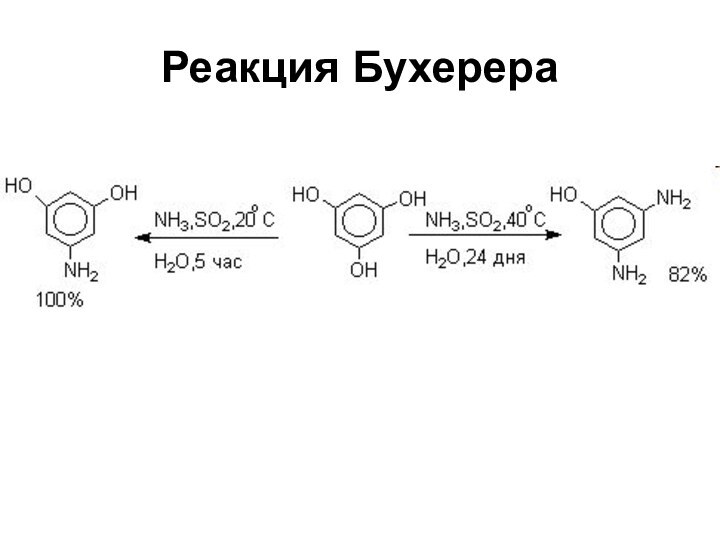
- 39. Реакция Бухерера
- 40. Реакция Бухерера
- 41. Реакция УльманаArI + Cu ArCuArCu + ArI ArAr
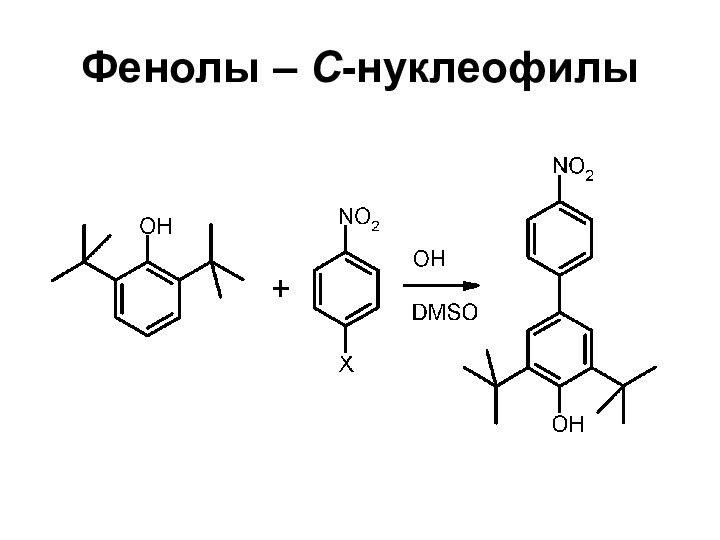
- 42. Фенолы – С-нуклеофилы
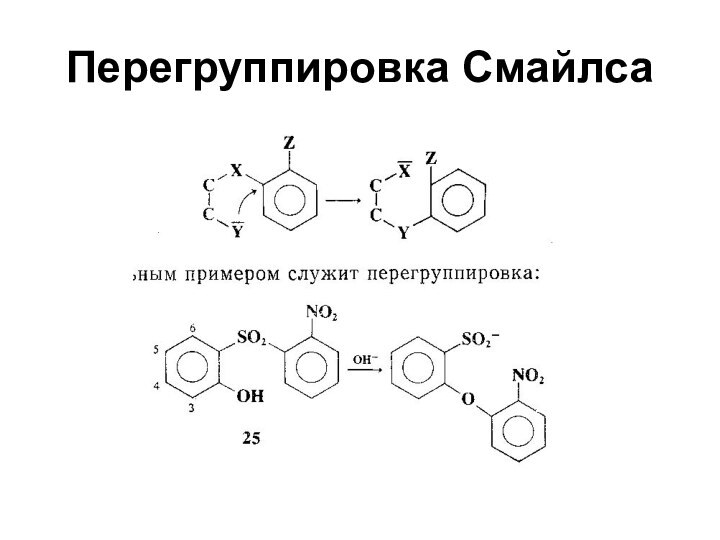
- 43. Перегруппировка Смайлса
- 44. Реакция УльманаAr-I + Cu ArCuArCu + Ar-I Ar-Ar
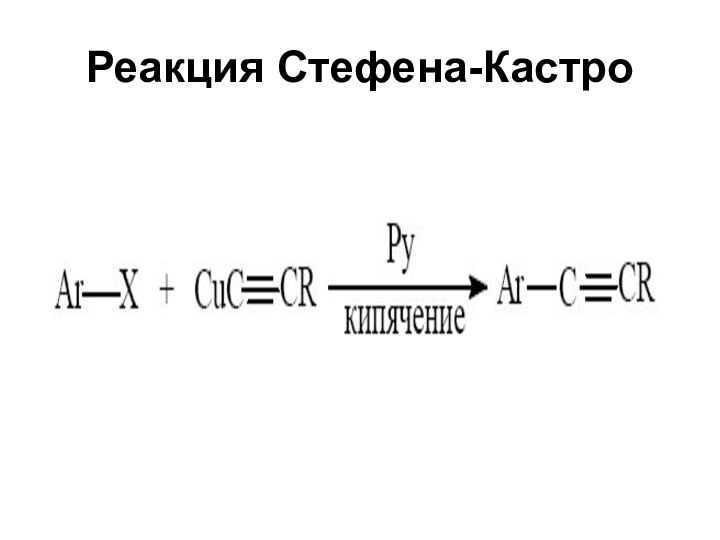
- 45. Реакция Стефена-Кастро
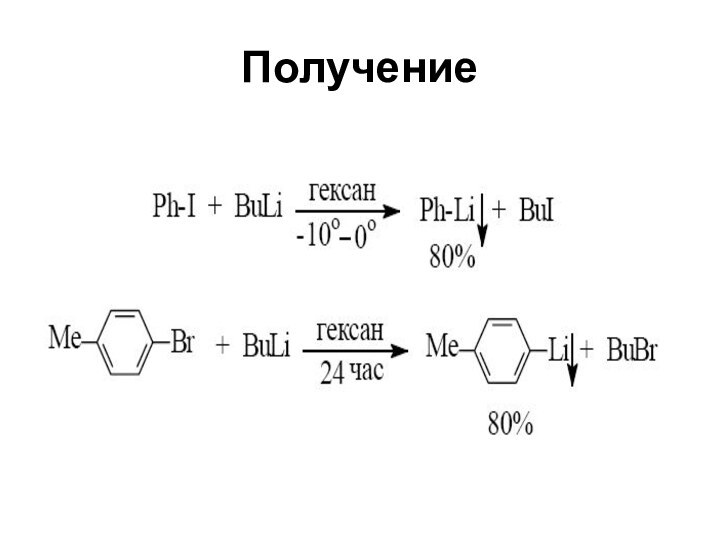
- 46. Получение
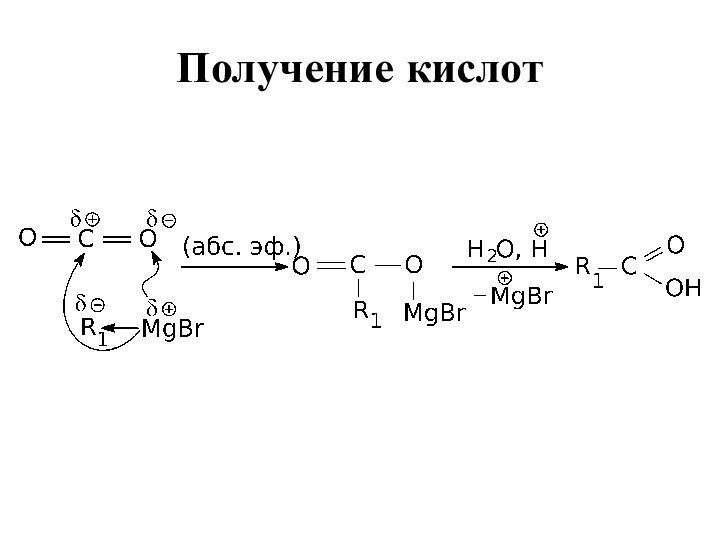
- 47. Получение кислот
- 48. Скачать презентацию
- 49. Похожие презентации
Реакции ароматического нуклеофильного замещения











![Реакции ароматического нуклеофильного замещения SRN1ArX + e [ArX]-.[ArX]-. Ar. + X-Ar. + Y- ](/img/tmb/13/1268684/5dfec501d6f1354e90de77c4f7349aac-720x.jpg)

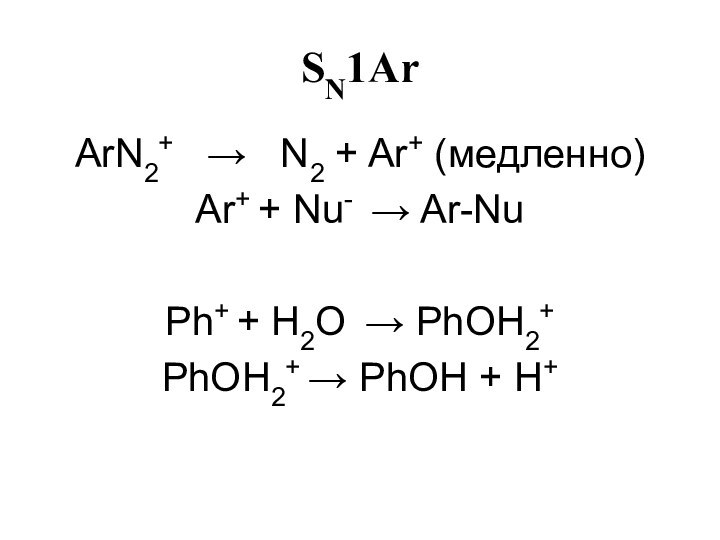
![Реакции ароматического нуклеофильного замещения SN1Ar1) Скорость не зависит от [Nu]2) Влияние заместителей в ароматическом](/img/tmb/13/1268684/00b30c4aa5bb0fcc1afec508c415fcd2-720x.jpg)





Слайд 5
Нуклеофильное замещение в ароматических и гетероароматических системах
1)
реакции, активируемые электроноакцепторными группами в орто- и пара-положениях к
уходящей группе;2) реакции, катализируемые очень сильными основаниями и протекающие через образование ариновых интермедиатов;
3) реакции, инициируемые донорами электронов;
4) реакции, в которых азот в соли диазония замещается нуклеофилом
Слайд 6
SNAr
нуклеофуги - уходящие частицы:
Hal-, RO-, NO2- и
др., в том числе и водород.
Эта область органической
химии в последние десятилетия особенно интенсивно развивается, в ней было открыто несколько новых механизмов.
Слайд 8
SNAr
Ускоряется в присутствии электроноакцепторных заместителей (особенно в орто-
и пара-положениях), катализаторов, -коплексованием, в гетероциклах атомом азота (
и -положения), N-оксидной функциейТормозится в присутствии электронодонорных заместителей





























