- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Щелочноземельные металлы
Содержание
- 2. Цель:Изучение строения атомов щелочноземельных металлов, физических и химических свойств.
- 3. Положение в периодической таблицеBe Mg
- 4. Строение атома+4 ) )+12 ) ) )+20
- 5. Распишите электронные формулы всех элементов63SВеMg
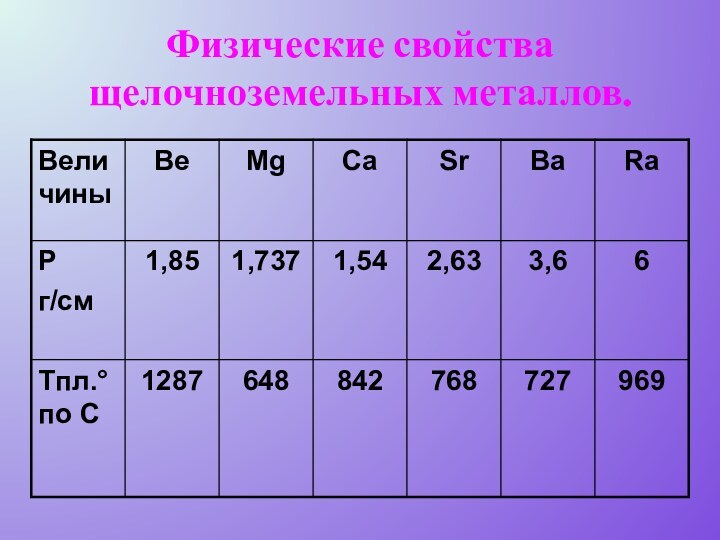
- 6. Физические свойства щелочноземельных металлов.
- 7. Химические свойства1.Взаимодйествие с простыми веществами:А) с кислородом2Са+
- 8. Химические свойства2. Взаимодействие со сложными веществами.а) с
- 9. Mg +2HCl = MgCl2 +H2Са с разбавленными кислотами не реагируетВзаимодействие с кислотами
- 10. Соединения щелочноземельных металлов
- 11. Выполните следующее задание:Решить задачу №1после §12Осуществить превращения:Ca → CaO→ CaCl2→ Ca(OH)2 →CaCO3 →CaO
- 12. Скачать презентацию
- 13. Похожие презентации
Цель:Изучение строения атомов щелочноземельных металлов, физических и химических свойств.









Слайд 7
Химические свойства
1.Взаимодйествие с простыми веществами:
А) с кислородом
2Са+ О2=
2СаО
Б) с галогенами
Са +Сl2= CaCl2
В) с водородом
Са +Н2 =
СаН2Г) с азотом
3Са + N2 = Ca3N2
Слайд 8
Химические свойства
2. Взаимодействие со сложными веществами.
а) с водой
Са
+ 2Н2О = Са(ОН)2 + Н2
б) с солями менее
активных металловMg +CuSO4 =Cu +MgSO4
в) с оксидами металлов
FeO + Mg = MgO +Fe
Его используют для получения чистых металлов из оксидов. Этот способ получил название магниотермия.





























