Слайд 2
Цели:
1.Добиться усвоения понятия «спирты»; сформировать знания о составе,
строении, номенклатуре спиртов, физиологическом воздействии на организм, физических и
химических свойствах, способах получения, областях применения.
2. Формировать умение делать выводы, сравнивать, работать с источниками информации (учебник, таблица, схема), высказывать суждения по изучаемым вопросам. Подтвердить прогноз экспериментально.
3. Формировать умение находить пути решения проблемных ситуаций, обосновывать свое решение адекватно поставленной проблеме.
Слайд 3
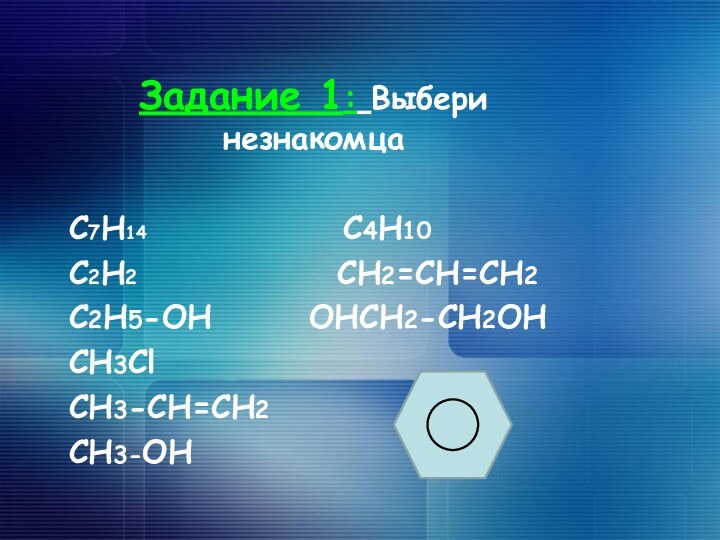
Задание 1: Выбери незнакомца
C7H14
C4H10
C2H2 CH2=CH=CH2
C2H5-OH OHCH2-CH2OH
CH3Cl
CH3-CH=CH2
CH3-OH
Слайд 4
Задание 2
Напишите структурную формулу этана и пропана в
которых один атом водорода замените на -ОН группу.
СН3
–СН2- ОН
СН3 – СН2 –СН2- ОН
Напишите структурную формулу пропана и замените около каждого атома углерода один атом водорода на -ОН группу.
СН2ОН-СНОН-СН2ОН
Слайд 5
Как назвать класс получившихся веществ?
2. Как можно отличить
спирты от других классов органических веществ?
3. Какое определение спиртов
вы можете предложить?
Слайд 6
Спирты (алканолы)– органические вещества, в молекулах которых содержится
одна или несколько гидроксильных групп (-ОН) соединенных с углеводородным
радикалом.
Слайд 7
Содержание
Из истории.
Классификация,
Изомерия,номенклатура спиртов.
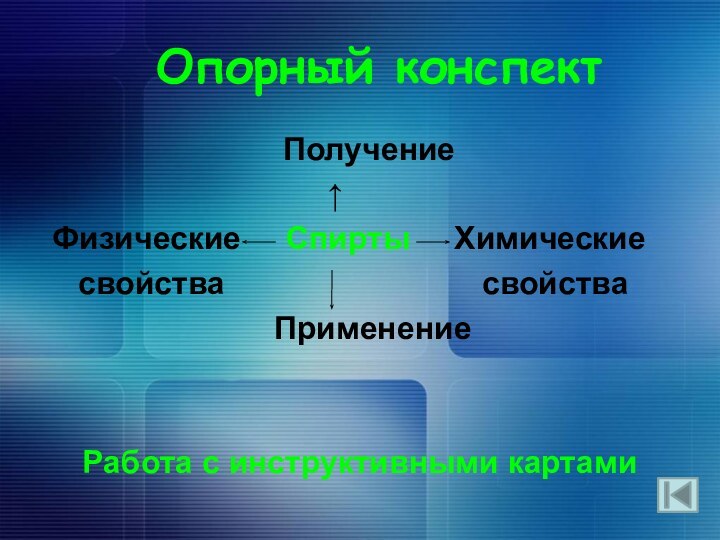
Опорный конспект
Физические свойства.
Получение спиртов.
Химические
свойства.
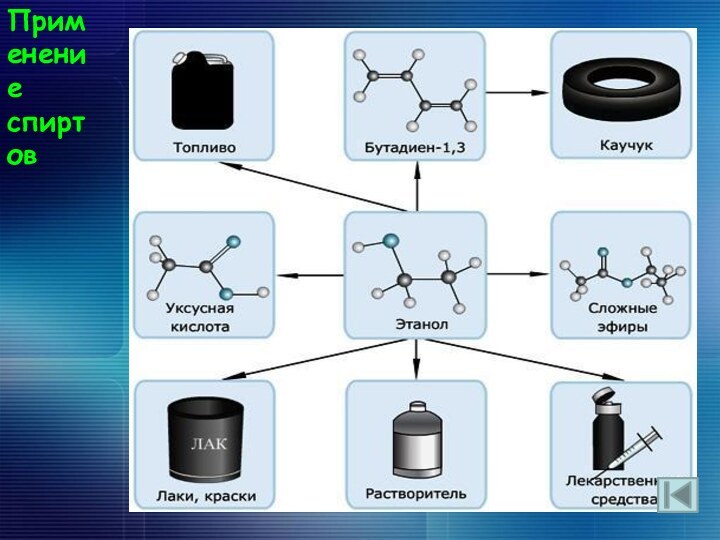
Применение спиртов.
Дружить или не дружить со спиртами
Слайд 8
Из истории возникновения алкоголя
Похититель рассудка — так именуют
алкоголь с давних времен. Чистый спирт начали получать в
5-7 веках арабы и назвали « аль коголь», что означает « одурманивающий». Об опьяняющих свойствах спиртных напитков люди узнали не менее чем за 8000 лет до нашей эры – с появлением керамической посуды, давшей возможность изготовления алкогольных напитков из меда, плодовых соков и дикорастущего винограда. Возможно, виноделие возникло еще до начала культурного земледелия. Так, известный путешественник Н.Н. Миклухо-Маклай наблюдал папуасов Новой Гвинеи, не умевших еще добывать огонь, но знавших уже приемы приготовления хмельных напитков.
Слайд 10
Спирты в России
В
дохристианскую эпоху на Руси потребление алкоголя имело место главным
образом на языческих пиршествах (народный и княжеский пиры, игрища, тризны).
Известно, что в Древней Руси пьянства не было вовсе. Население Древней Руси невыращивало виноград, и вино для Причастного таинства привозилось из Византии. Хмельными напитками были бродивший мёд и пиво. С этих далеких времен сохранился назаменитый рефрен многих народных сказок: “И я там был. Мед, пиво пил. По усам текло, а в рот не попало”.
Слайд 11
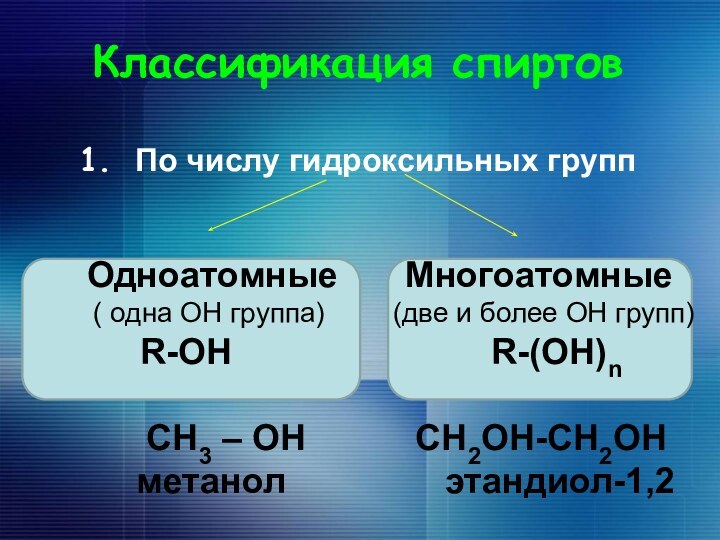
Классификация спиртов
1. По числу гидроксильных групп
Одноатомные Многоатомные
( одна ОН группа) (две и более ОН групп)
R-OH R-(OH)n
СН3 – ОН СН2ОН-СН2ОН
метанол этандиол-1,2
Слайд 12
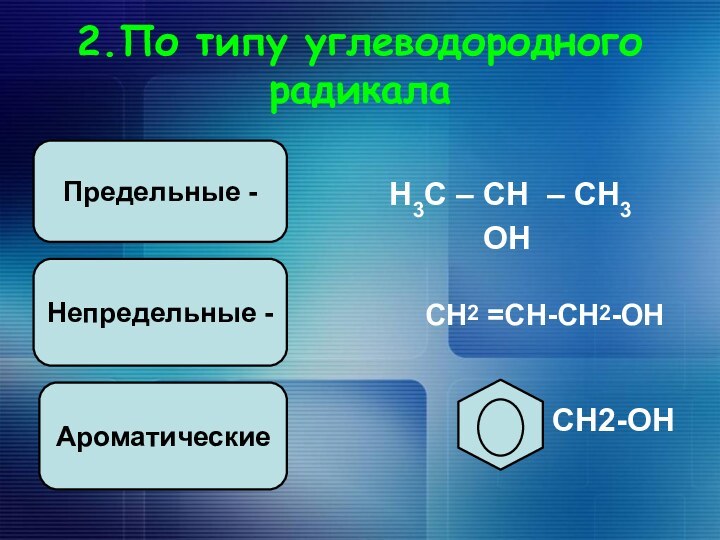
2.По типу углеводородного радикала
Н3С – СН – СН3
ОН
СН2 =СН-СН2-ОН
СН2-ОН
Предельные -
Непредельные -
Ароматические
Слайд 13
3. По типу атома углерода, связанного с группой
- ОН
СН3-СН2-СН2-ОН
СН3-СН-СН3
ОН
СН3
СН3-С-СН3
ОН
Первичные -
Вторичные -
Третичные -
Слайд 14
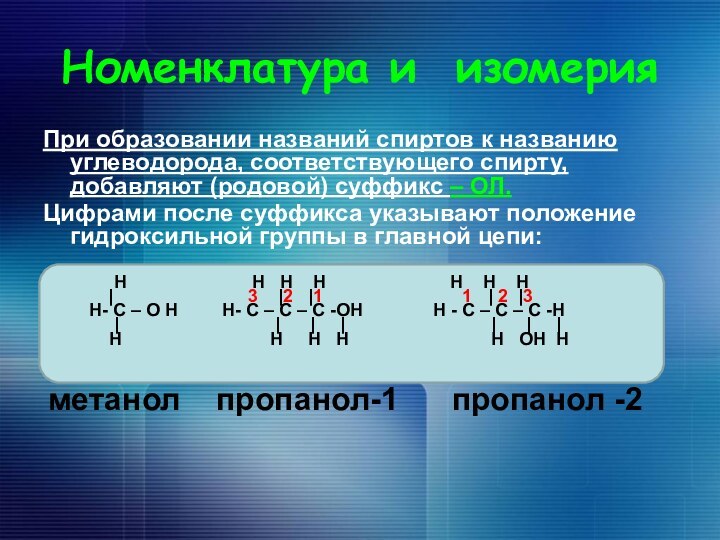
Номенклатура и изомерия
При образовании названий спиртов к
названию углеводорода, соответствующего спирту, добавляют (родовой) суффикс – ОЛ.
Цифрами
после суффикса указывают положение гидроксильной группы в главной цепи:
H H H H H H H
| 3 |2 |1 1 | 2 |3
H- C – O H H- C – C – C -OH H - C – C – C -H
| | | | | | |
H H H H H OH H
метанол пропанол-1 пропанол -2
Слайд 15
ВИДЫ ИЗОМЕРИИ:
1. Изомерия положения функциональной группы (пропанол–1 и
пропанол–2)
2.Изомерия углеродного скелета
CH3-CH2-CH2-CH2-OH
CH3-CH-CH2-OH
CH3
бутанол-1 2-метилпропанол-1
3.Изомерия межклассовая – спирты изомерны простым эфирам:
СН3-СН2-ОН СН3-О-СН3
этанол диметиловый эфир
Получение
↑
Физические Спирты Химические
свойства свойства
Применение
Работа с инструктивными картами
Опорный конспект
Слайд 17
Физические свойства
Низшие и средние спирты (С1-C11)-летучие, бесцветные жидкости
с резким, характерным алкогольным запахом, жгучим вкусом. Растворимы в
воде до актонола.
Высшие спирты (C12- и выше)- твердые вещества с приятным запахом. Нерастворимы в воде.
Слайд 18
Способы получения
Лабораторные:
Гидролиз галогеналканов:
R-CL+NaOH
R-OH+NaCL
Гидратация алкенов: CH2=CH2+H2O C2H5OH
Гидрирование карбонильных соединений
Промышленные:
Синтез
метанола из синтез-газа
CO+2H2 CH3-OH (при повышенном давлении, высокой температуре и катализатора оксида цинка)
Гидратация алкенов
Брожение глюкозы: C6H12O6 2C2H5OH+2CO2
Слайд 19
Химические свойства
1. Спирты реагируют с щелочными
и щелочноземельными металлами, образуя солеобразные соединения – алкоголяты.
2СH3CH2CH2OH
+ 2Na 2СH3CH2CH2ONa + H2
При этом атом водорода гидроксильной группы замещается на металл. Похоже на кислоту.
2СH3CH2OH + Сa (СH3CH2O)2Ca + H2
Но кислотные свойства спиртов слишком слабы, слабы настолько, что спирты не действуют на индикаторы.
Слайд 20
Химические свойства
2. Спирты горят:
2С3H7ОH
+ 9O2 6СO2 + 8H2O
Дегидратация
CH3–CH2–OH CH2=CH2 +
H2O
Слайд 22
Дружить или не дружить со спиртом.
Спирт относится к ксенобиотикам – веществам, не содержащимся
в человеческом организме, но влияющим на его жизнедеятельность. Все зависит от дозы.
Спирт – это питательное вещество, которое обеспечивает организм энергией. В средние века за счет потребления алкоголя организм получал около 25% энергии.
Спирт – это лекарственное средство, имеющее дезинфицирующее и антибактериальное действие.
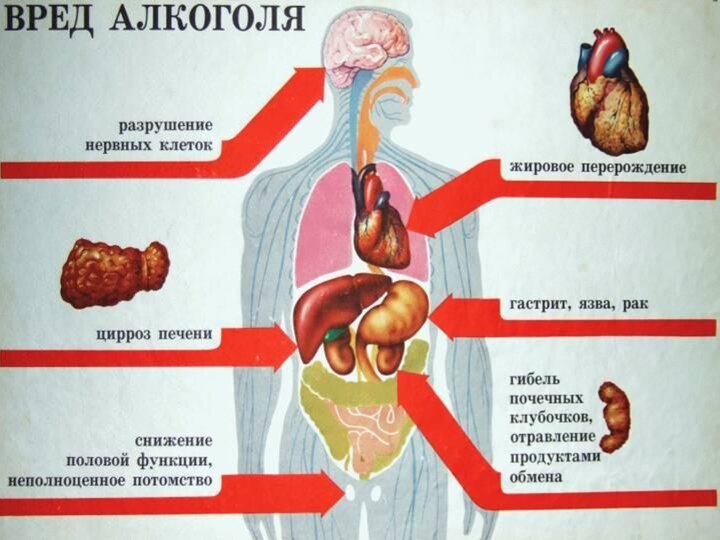
Спирт – это яд, нарушающий естественные биологические процессы, разрушающий внутренние органы и психику и при чрезмерном употреблении влекущий смерть.
Слайд 23
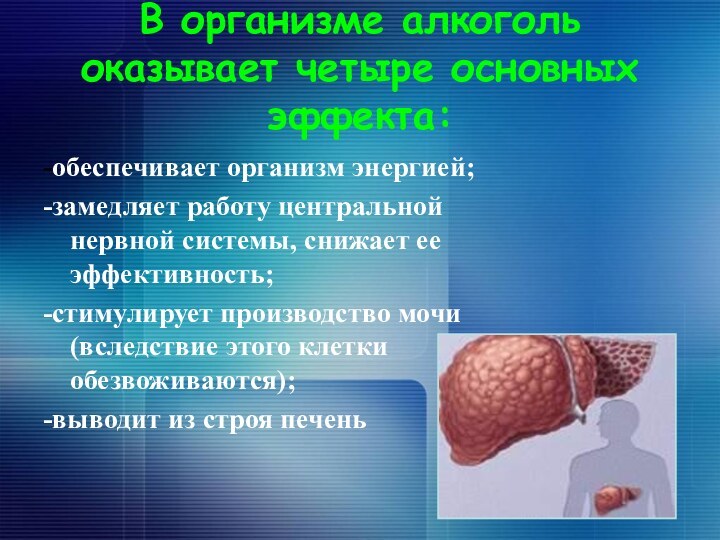
В организме алкоголь оказывает четыре основных эффекта:
-обеспечивает организм
энергией;
-замедляет работу центральной нервной системы, снижает ее эффективность;
-стимулирует
производство мочи (вследствие этого клетки обезвоживаются);
-выводит из строя печень
Слайд 25
ВОПРОСЫ ДЛЯ ЗАКРЕПЛЕНИЯ
В одном сосуде без подписи находится
вода, а в другом – спирт. Можно ли воспользоваться
индикатором, чтобы их распознать?
Кому принадлежит честь получения чистого спирта?
Может ли спирт быть твердым веществом?
Молекулярная масса метанола 32, а углекислого газа 44. Сделайте вывод об агрегатном состоянии спирта.
Как провести инспектора ГАИ?