- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Алюминий (9 класс)
Содержание
- 2. «Нахождение алюминия в природе, его свойства, получение и применение»Тема урока:3.03.11
- 3. Цель урокаРассмотреть природные соединения алюминия, важнейшие свойства, получение и изучить практическое значение
- 4. ЗадачиОбразовательная: на основе знания общих свойств металлов
- 5. Осуществить цепочку превращенияCO2 → СaCO3→ Са(HCO3 )2→ СaCO3→CaO→ Са(ОH)2
- 6. Ответы на тестыВариант-11-г2-б3-в4-в5-б6-в7-в8-в9-а10-бВариант-21-а2-г3-б4-б5-б6-б7-г8-в9-а10-в
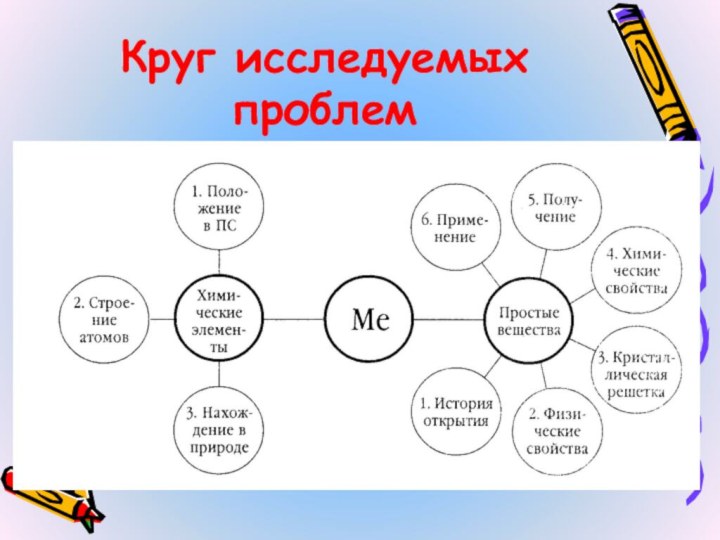
- 7. Круг исследуемых проблемALХимическийэлементПростое вещество
- 8. Характеристика алюминия как химического элементаПоложение в периодической
- 9. Алюминий как химический элемент: 3) нахождение в
- 10. Всего известно 250 минералов . В состав
- 12. Это полудрагоценные камни , содержащие алюминий.
- 14. Нахождение в природе.Алюминий в природе встречается
- 15. Алюминий- простое веществоАлюминий впервые был получен датским химиком Эрстедом в 1825 г
- 16. Самые древние изделия из алюминия датированы III
- 17. Древние римляне использовали квасцы для подавления секреции потовых желез
- 18. Племянник Наполеона III приказал изготовить сервиз и
- 19. В 1889 году в Лондоне Д.И. Менделееву
- 20. В 1955 г.в Венгрии выпустили почтовую марку на алюминиевой фольге толщиной 0,09мм/
- 21. Каков будет выход продукта продукта реакции, если из 800г глинозема (Аl2О3) получено 400г алюминия.
- 22. Тайны физических свойств алюминия
- 23. План исследования1.Сравнительный анализ физических свойств алюминия.2.Особенности строения алюминия, как простого вещества.3.Выводы.
- 24. Кристаллическая решетка
- 25. 1.Исследовать диаграмму физических свойств алюминия;Эталоном твёрдости принят
- 26. Согласно диаграмме, алюминий занимает 4место
- 27. Плотность Al составляет 2,7 г/см3 ( менее
- 28. Температура плавления Al- 660 0С в сравнении
- 29. В чём причины физических свойств алюминия?В строении!
- 31. Вывод Характерные физические свойства алюминия находятся
- 32. Химические свойства От чего зависят химические свойства?Какова
- 33. ALСложные веществаПростыевеществаO2H2OI2кислотаS?Щёлочьсоль
- 34. Составьте уравнения реакций алюминия с кислородом, йодом
- 35. выводАлюминий –очень активный металл.В ряду напряжений он
- 36. Получение1.Кто впервые получил алюминий? Почему этот способ
- 37. Алюминий как простое вещество: получение.
- 38. Какие же свойства алюминия позволяют ему найти широкое применение в технике ,быту промышленности?Применение
- 39. Применение алюминия
- 40. Люстры из алюминиевых пластинок, зеркала, прожектораСпособность отражать световые лучиСпособность гореть ослепительным пламенем
- 43. Найти соответствие:
- 44. Почему алюминий так нужен человеку?Запишите
- 45. Скачать презентацию
- 46. Похожие презентации
«Нахождение алюминия в природе, его свойства, получение и применение»Тема урока:3.03.11










































Слайд 3
Цель урока
Рассмотреть природные соединения алюминия, важнейшие свойства, получение
и изучить практическое значение
Слайд 4
Задачи
Образовательная: на основе знания общих свойств металлов охарактеризовать
свойства алюминия как химического элемента и простого вещества, сформировать
представление о природных источниках, свойствах и применении алюминия.Развивающая: умение работать с различными источниками информации, прививать навыки самостоятельной работы, учить четко и грамотно выражать свои мысли, развивать умения выделять главное, сравнивать и обобщать.
Воспитывающая: формирование коммуникативных качеств и чувства ответственности, аккуратности.
Слайд 6
Ответы на тесты
Вариант-1
1-г
2-б
3-в
4-в
5-б
6-в
7-в
8-в
9-а
10-б
Вариант-2
1-а
2-г
3-б
4-б
5-б
6-б
7-г
8-в
9-а
10-в
Слайд 8
Характеристика алюминия
как химического элемента
Положение в периодической системе
: ___период, ___ ряд ,
__ группа , _____ подгруппа
Порядковый
номер №___Строение атома
е- =__, р+ =__, n 0= __
З.я. +____ ) ) )
_ _ _
Алюминий – _________ металл
Формулы
высшего оксида_________,
его гидроксида ________.
Слайд 9
Алюминий как химический элемент:
3) нахождение в природе.
Li,K,Ba,Ca,Na,Mg,Al,Mn,Cr,Zn,Fe,Co,Sn,Pb,H2,Cu,Hg,Au
Рассмотрите
диаграмму.
Сделайте вывод о распространенности алюминия в земной коре
по сравнению с другими металлами. Рассмотрите электрохимический ряд металлов.
В каком виде (в свободном или в соединении) находится алюминий в природе?
Слайд 10 Всего известно 250 минералов . В состав которых
алюминий
Важнейший минерал алюминия – боксит , смесь основного оксида
AlO(OH) . Al(OH)3
Слайд 14
Нахождение в природе.
Алюминий в природе встречается в
виде алюмосиликатов,боксита, корунда и криолита.
Алюмосиликаты составляют основную массу земной
коры. Продукт их выветривания – глина и полевые шпаты.Слайд 16 Самые древние изделия из алюминия датированы III веком
н.э. в трудах Плиния старшего. Римскому императору Тиберию ремесленник
принес кубок из серебристо-белого металла, утверждая, что его он сделал из глины. Опасаясь за обесценивание золота и серебра, император велел казнить мастера.Слайд 18 Племянник Наполеона III приказал изготовить сервиз и столовые
приборы для торжеств, во время которых важные персоны ели
алюминиевыми приборами, а менее важные золотыми и серебрянымиСлайд 19 В 1889 году в Лондоне Д.И. Менделееву за
заслуги в химии вручили драгоценные весы из золота и
алюминияСлайд 21 Каков будет выход продукта продукта реакции, если из
800г глинозема (Аl2О3) получено 400г алюминия.
Слайд 22
Тайны физических свойств
алюминия
Цели:
1.Исследовать важнейшие
физические свойства алюминия в сравнении со свойствами других металлов.2.Выявить причины, обуславливающие эти признаки.
Гипотеза:
Свойства металлов возможно прогнозировать.
Слайд 23
План исследования
1.Сравнительный анализ физических свойств алюминия.
2.Особенности строения алюминия,
как простого вещества.
3.Выводы.
Слайд 25
1.Исследовать диаграмму физических свойств алюминия;
Эталоном твёрдости принят алмаз-10
единиц.
Твёрдость алюминия 2,9 единиц, что составляет 30% от
твёрдости алмаза, 96% от твёрдости Cu , 67.5% от твёрдости Fe , значит Al-мягкий металл.Слайд 26 Согласно диаграмме, алюминий занимает 4место после
Ag, Cu, Au .
Электропроводность составляет 65% от Cu и
теплопроводность -50% от Cu .Слайд 27 Плотность Al составляет 2,7 г/см3 ( менее 5
г/см3), значит
Al- лёгкий металл,
он
уступает по плотности Ag, Cu и Fe,но тяжелее Mg, K, Na.
Al в 4 раза легче Аg ,3.5 легче Cu и в 3 раза легче Fe .
Слайд 28
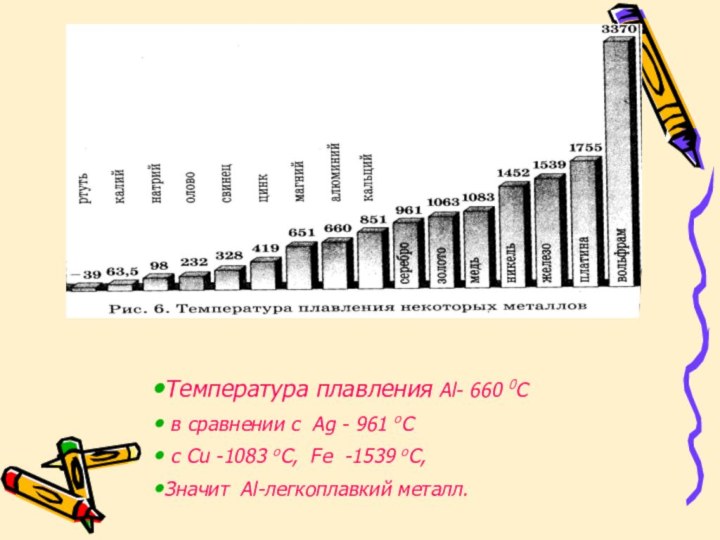
Температура плавления Al- 660 0С
в сравнении с
Ag - 961 оС
с Cu -1083 оC, Fe
-1539 оC,Значит Al-легкоплавкий металл.
Слайд 29
В чём причины физических свойств алюминия?
В строении!
Кристаллическая
решётка Al.Она подобна кубу с плотноупакованными шарами. Это металлическая
кубическая гранецентрированная решётка. В узлах решётки находятся ионы, а в промежутках между ними легкоподвижные электроны. Веществам с металлической кристаллической решёткой присуща металлическая связь. Попробуем установить зависимость между строением Al и его физическими свойствами.
Слайд 31
Вывод
Характерные физические свойства алюминия находятся в
зависимости от его внутренней структуры. Зная строение, можно прогнозировать
свойства металлов.
Слайд 32
Химические свойства
От чего зависят химические свойства?
Какова химическая
активность алюминия ?
Какие свойства проявляет алюминий , вступая в
химические реакции ?Напишите уравнения реакции характерные для алюминия.
Слайд 34
Составьте уравнения реакций алюминия с кислородом, йодом
Al+ O2 =
Al + I2
= Al+ H2O=
Al + HCl=
Al + NaOH+ H2O=
Методом электронного баланса подберите коэффициенты
Al+ CuCl2 =
Составьте уравнения реакций алюминия с водой, кислотой . щёлочью и солью
Слайд 35
вывод
Алюминий –очень активный металл.
В ряду напряжений он стоит
после щелочных и щелочноземельных металлов .
«Пассивность» алюминия связана с
наличием оксидной плёнки.Алюминий проявляет переходные свойства.
В реакциях он проявляет восстановительные свойства.
Слайд 36
Получение
1.Кто впервые получил алюминий? Почему этот способ не
используют для промышленного получения. Напишите уравнение реакции.
2.Какой метод получения
используют в настоящее время. Почему? Напишите уравнение реакции получения алюминия.Слайд 38 Какие же свойства алюминия позволяют ему найти широкое
применение в технике ,быту промышленности?
Применение
Слайд 40
Люстры из алюминиевых пластинок, зеркала, прожектора
Способность отражать
световые
лучи
Способность гореть
ослепительным
пламенем
Слайд 44
Почему алюминий так нужен человеку?
Запишите три характерных свойства
алюминия, благодаря которым металл широко применяется в быту и
производстве:А)
Б)
В)





























