Слайд 3
Цели урока
Общая характеристика фосфора. Углубить
и расширить знания о причинах возникновения разных видах аллотропных
модификаций фосфора. Изучить химические свойства фосфора.
Слайд 4
Фосфор был открыт в 1669 году. Один из алхимиков
пытался отыскать философский камень, а получил светящееся вещество…
Слайд 5
Исторические сведения
Фосфор, вероятно, был впервые выделен
еще в XII веке арабским алхимиком Алхид Бехилом. Документированное
открытие фосфора, возможно, было повторным и состоялось в 1669 г., когда это сделал немецкий алхимик Хённиг Бранд (1630–1710), за ним и был закреплен приоритет открытия фосфора. Оба ученых наблюдали свечение фосфора и его самовоспламенение.
… Отставной солдат Хённиг Бранд из Гамбурга, подобно другим алхимикам, упорно пытался отыскать волшебный философский камень, который возвращал бы больным старикам молодость и здоровье, а все металлы обращал в золото.
Слайд 7
Как и другие алхимики, Бранд действовал вслепую, подвергая
разнообразные вещества химическим операциям – перегонке, выпариванию, прокаливанию. Однажды
ему пришло в голову выпарить воду из мочи, которая в большом количестве скапливалась в ямах около солдатских казарм. И вот получен сухой остаток от выпаривания. Бранд смешивает его с углем и песком, прокаливает и... в реторте оказывается удивительное светящееся в темноте вещество, которое он назвал «холодным огнем».
Слайд 8
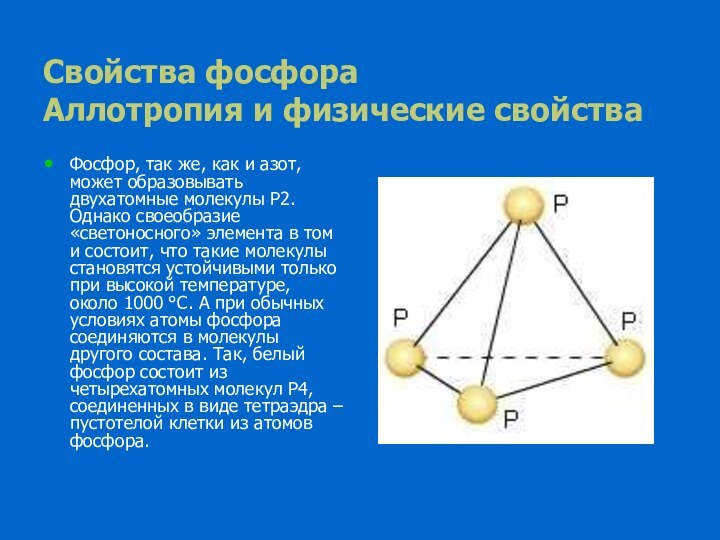
Свойства фосфора
Аллотропия и физические свойства
Фосфор, так же, как
и азот, может образовывать двухатомные молекулы P2. Однако своеобразие
«светоносного» элемента в том и состоит, что такие молекулы становятся устойчивыми только при высокой температуре, около 1000 °С. А при обычных условиях атомы фосфора соединяются в молекулы другого состава. Так, белый фосфор состоит из четырехатомных молекул P4, соединенных в виде тетраэдра – пустотелой клетки из атомов фосфора.
Слайд 10
Белый фосфор — желтовато-белое вещество (из-за примесей), по мягкости
напоминает воск.
Очень активное вещество; а светится, потому что уже
при комнатной температуре окисляется кислородом из воздуха:
Формула белого фосфора - P4, т.е. у него молекулярная кристаллическая решетка.
В книге «Собака Баскервиллей» описывается именно такой фосфор, проблема только в том, что он чрезвычайно ядовит и огнеопасен!
Слайд 12
Желтый фосфор
Это просто
неочищенный белый фосфор. Цвет — от желтого до коричневого. Так же
активен, так же, как и белый фософр, на воздухе самовоспламеняется
Слайд 13
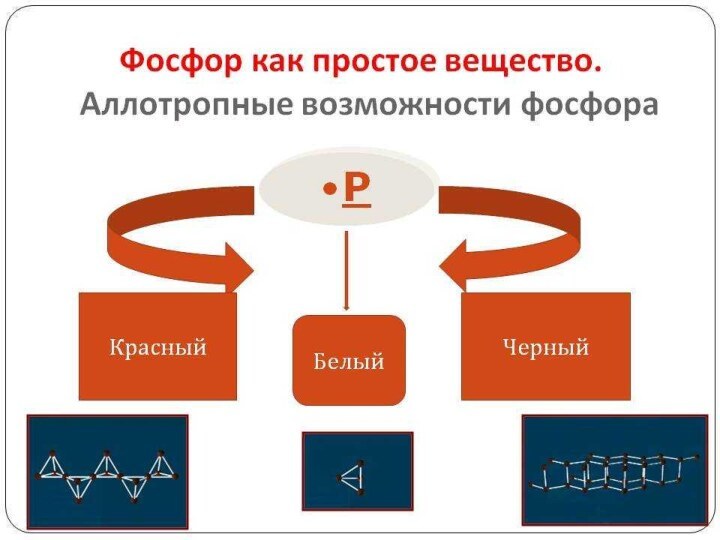
Красный фосфор
Менее активное вещество, чем белый или желтый
фосфор , меньше растворим в воде, на воздухе не самовоспламеняется и не
светится. Менее ядовит. Его формула — Pn - буква n означает, что у вещества полимерная структура. Атомная кристаллическая решетка. Именно из-за его устойчивости и безвредности это основная аллотропия фосфора, применяемая в промышленности и в быту.
Красный фосфор активно применяют при производстве спичек.
Слайд 14
Чёрный фосфор
Чёрное вещество с металлическим блеском, на ощупь
— жирный, внешне очень похож на графит. Чёрный фосфор
даже проводит электрический ток, что обычно характерно для металлов. При определенном давлении он может переходить в модификацию, которую так и называют — металлический фосфор.
Слайд 16
Химические свойства
Белый фосфор Р4 значительно активнее полимерного красного фосфора:
так, температура вспышки белого фосфора 34 °С (часто самовозгорается на
воздухе), а красного фосфора – 240 °С. В уравнениях реакций фосфор для упрощения записывают как P. Красный фосфор на воздухе загорается только при нагревании, реагирует с фтором, хлором и серой.
Свечение на воздухе характерно только для белого фосфора P4. Белый фосфор светится за счет того, что при медленном окислении из Р4 получается оксид фосфора(III) состава P4O6. Уравнение реакции окисления белого фосфора при свечении:
P4 + 3O2 = P4O6.
Слайд 17
Взаимодействует со многими простыми веществами — галогенами, серой,
некоторыми металлами, проявляя окислительные и восстановительные свойства:
Слайд 19
Химические свойства фосфора.
1. Взаимодействие с металлами.
3Ca +2 P (красн)
Ca3P2 (фосфид кальция)
2. Взаимодействие с неметаллами.
4P+5O2 =2P2O5
4P+3O2 =2P2O3
2P+ 5S P2S5
4P+ 3Cl2 =2 P2Cl3
3.
Фосфор - восстановитель.
5KClO3 +6P = 5KCl + 3P2O5
Слайд 25
Биологическая роль фосфора
фосфор входит в состав многих веществ
организма (фосфолипиды, фосфопротеиды, нуклеотиды, коферменты, ферменты и пр.)
фосфолипиды являются
основным компонентом мембран всех клеток в организме человека
в костях фосфор находится в виде гидроксилапатита, в зубах в виде фторапатит, выполняя структурную функцию
остатки фосфорной кислоты входят в состав нуклеиновых кислот и нуклеотидов, а также в состав аденозинтрифосфорной кислоты (АТФ) и креатинфосфата – важнейшие аккумуляторы и переносчики энергии
остатки фосфорной кислоты входят в состав буферной системы крови, регулируя ее значение рН
Слайд 26
Тест по теме «Фосфор»
Какое из
утверждений неверно: «Атом фосфора по сравнению с атомом азота
имеет:
а) больший радиус;
б) меньшее значение электроотрицательности;
в) более ярко выраженные окислительные свойства;
г) больший заряд ядра»
Слайд 27
При горении фосфора образуется:
а) оксид фосфора (III)
б) оксид
фосфора (V)
в) фосфин
г) фосфорная кислота
Слайд 28
. В организме человека больше всего фосфора содержится
в:
а) мышцах
б) головном мозге
в) крови
г) печени
Слайд 29
Какие для фосфора характерны степени окисления:
а) -3, +2,
+5
б) -3, +3, +5
в) +1, +3, +5
г) -2, +3,
+5
Слайд 30
Какой аллотропной модификации фосфора не существует:
а) черный
б) белый
в)
синий
г) красный
Слайд 31
Интересные факты
Фосфор — у древних
греков название утренней звезды. По Гесиоду, Ф. был сын
титанида Астрея и богини Эос и считался любимой звездой Афродиты, которая сделала его стражем своего святилища. Некоторые отождествляли Ф. с Геспером (вечерней звездой) или представляли их в образе братской четы, как Диоскуров. Символически Ф. обозначал собой восток, Геспер — запад, у восточных локров (опунтских и эпикнемидских) была печать с изображением Ф., у западных локров — печать с изображением Геспера.
Слайд 32
Закрепление:
1 Перечислите основные отличия белого от красного фосфора.
2
Как хранят белый фосфор?
3 Укажите в каких случаях фосфор
является окислителем, а когда восстановитель.
ваши главные результаты, что вы поняли, чему научились?
Какие задания
вызвали наибольший интерес и почему?
С какими трудностями вы столкнулись и как вы их преодолевали?
Каковы замечания и предложения на будущее (себе, преподавателям, организаторам)?