- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Генно-инженерные лекарственные препараты
Содержание
- 2. Генно-инженерные лекарственные препаратыЛекция
- 3. ЦЕЛЬ ЛЕКЦИИ:изучение технологии производства и ассортимента лекарственных препаратов, выпускаемых с помощью рекомбинантной ДНК-биотехнологии (генной инженерии).
- 4. П Л А Н Л Е
- 5. I. Получение инсулина генно-инженерными способами. Препараты инсулина
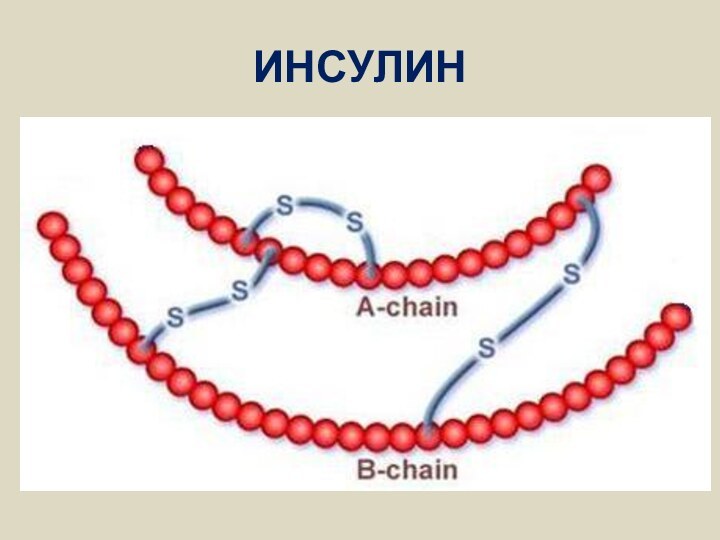
- 6. ИНСУЛИН
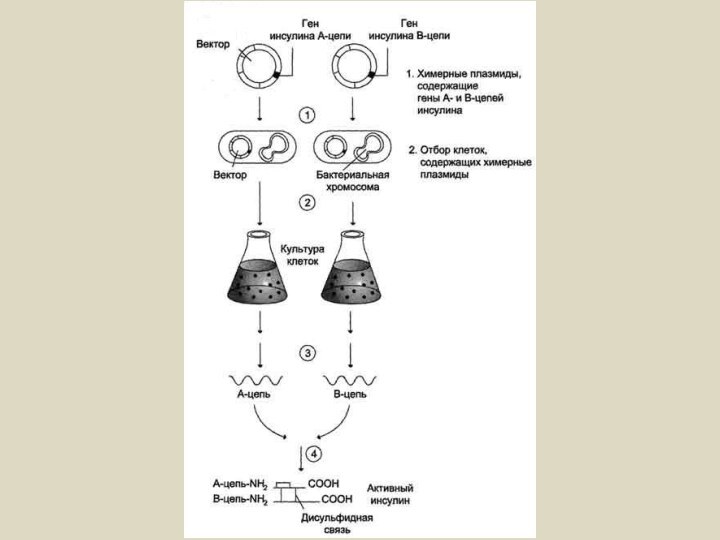
- 7. 1. Генно-инженерный метод через синтез цепей А
- 9. 2. Генно-инженерный метод через проинсулинИмитирует природный процесс
- 10. 3. Комбинация генноинженерного и ферментативного методаВключает: Получение
- 11. 4. Культивирование гибридомных клеток Этим методом, разработанным
- 12. Фирмы-производители:«Eli Lilly» (США)«Genentech» (США)«Novo nordisk» (Дания)«Sanofi -
- 13. Отечественные производители инсулина, использующие импортную субстанциюОАО «Биотон-Восток»,
- 14. История создания препаратов инсулинаСвиной и говяжий инсулины
- 15. Пролонгированные препараты инсулина1. Суспензии цинк-инсулин аморфная, кристаллическая
- 16. Классификация препаратов инсулина1. По составу:Монокомпонентные (свиной, говяжий,
- 17. Классификация препаратов инсулина3. По продолжительности действия:Инсулины короткого
- 18. II. ГОРМОН РОСТА (СОМАТОТРОПИН)
- 19. В
- 20. Фирмы-производители:США - «Хуматроп»
- 21. III. ЭРИТРОПОЭТИН
- 22. Американская
- 23. IV. ПОЛИПЕПТИДНЫЕ ФАКТОРЫ РОСТА
- 24. Пептидные
- 25. Ранозаживляющие факторыЭпидермальный фактор роста (ранозаживляющее действие при
- 26. Ранозаживляющие факторы3. Тромбоцитарный фактор роста (стимулятор
- 27. Колониестимулирующие факторыМакрофагальныйГранулоцитарный Гранулоцитарно-макрофагальныйПример. Препарат «Нейпоген» содержит филграстим,
- 28. Колониестимулирующие факторы являются противоопухолевыми средствами.Ранозаживляющие и колониестимулирущие
- 29. V. ЦИТОКИНЫ
- 30. Цитокины - большая гетерогенная группа белков, синтезируемая
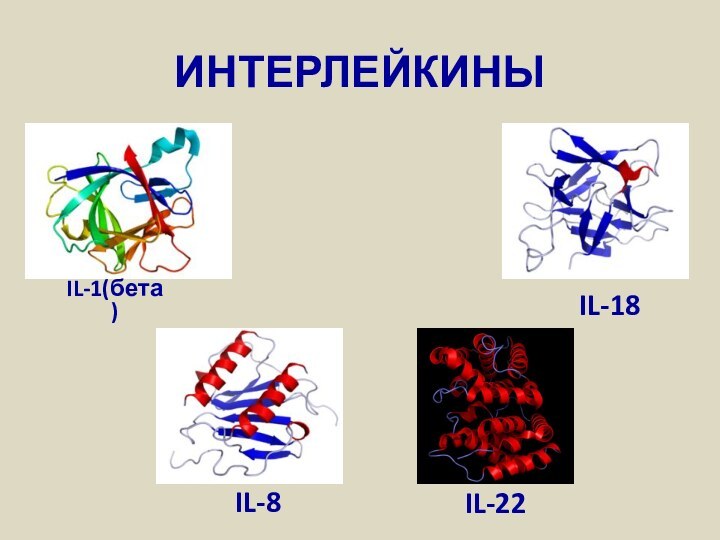
- 31. ИНТЕРЛЕЙКИНЫIL-1(бета)IL-18IL-22IL-8
- 32. Интерлейкины
- 33. Схема получения интерлейкиновАктивация клеток-продуцентов.Выделение интерлейкинов из культуральной среды.Концентрирование.Очистка.IL-10
- 34. Клетки-продуценты интерлейкиновкультуры нормальных лимфоцитов или макрофагов;
- 35. Для увеличения
- 36. ИНТЕРФЕРОНЫИнтерферон бета
- 37. Интерфероны
- 38. Биологическая роль интерфероновактивация интерфероногенеза и защита организма
- 39. Классификация интерферонов в зависимости от химической природы
- 40. Классификация интерферонов по способу получения Природные,
- 41. Традиционная технология получения α-интерферонаПолучение лейкоцитов из свежей
- 42. Традиционная технология получения β-интерферонаКультивирование фибробластов поверхностным методом
- 43. Традиционная технология получения γ-интерферонаКультивирование лимфобластов глубинным методом
- 44. Рекомбинантные микробы-продуценты интерферонов
- 45. Т е х н о л о
- 46. Фирмы-производители:«Генферон», «Интерферон β-1b»ООО «Ферон»«Виферон»«Гриппферон»«Интерферон лейкоцитарный»
- 47. Скачать презентацию
- 48. Похожие презентации





































Слайд 3
ЦЕЛЬ ЛЕКЦИИ:
изучение технологии производства и ассортимента лекарственных препаратов,
выпускаемых с помощью рекомбинантной ДНК-биотехнологии (генной инженерии).
Слайд 4 П Л А Н Л Е К
Ц И И
Получение инсулина генно-инженерными способами. Препараты инсулина.
Гормон роста
(соматотропин).Эритропоэтин.
Пептидные факторы роста.
Цитокины: интерлейкины и интерфероны.
Слайд 7 1. Генно-инженерный метод через синтез цепей А и
В человеческого инсулина
1. Химический синтез генов, кодирующих цепи А
и В человеческого инсулина.2. Введение синтетических генов с помощью плазмиды в структуру E.coli.
3. Продуцирование двух цепей белка инсулина.
4. Отрезание метиониновых остатков бромицианом.
5. Соединение цепей А и В дисульфидными мостиками через образование S-сульфоната
Выход составляет 50%.
Недостаток метода: необходимость химического синтеза генов, большое число подготовительных операций, высокие затраты.
Слайд 9
2. Генно-инженерный метод через проинсулин
Имитирует природный процесс и
включает в себя:
Введение в E.coli или S. сerevisiae
гена одноцепочечного проинсулина.Экспрессию гена с получением проинсулина.
Выделение белка с последующим окислением трипсином или карбоксипептидазой для перевода проинсулин в инсулин.
Этот метод упрощает технологический процесс, снижает производственные затраты.
Получаемые человеческие инсулины по данной технологии носят название «Хумулин».
Слайд 10
3. Комбинация генноинженерного и ферментативного метода
Включает:
Получение свиного
инсулина в E.coli по рДНК технологии.
Ферментативное превращение свиного
инсулина в инсулин человека.При данной технологии исключается зависимость от сырьевой базы (животного сырья).
Слайд 11
4. Культивирование гибридомных клеток
Этим методом, разработанным в
США и Японии, человеческий инсулин получают из ферментативной жидкости
при крупно-масштабном культивировании гибридомных клеток, продуцирующих инсулин.Из хомяков, зараженных раком поджелудочной железы, выделяют клетки островков Лангерганса и после слияния их с клетками, продуцирующими человеческий инсулин, культивируют полученные гибридные клетки в бессывороточной среде.
Слайд 12
Фирмы-производители:
«Eli Lilly» (США)
«Genentech» (США)
«Novo nordisk» (Дания)
«Sanofi - Aventis»
(Франция – Германия)
Инсулин, полученный по выше перечисленным технологиям, обязательно
подвергают очистке (хроматографическими методами), что дает возможность получить инсулин высокой чистоты и природной активности.
Слайд 13
Отечественные производители инсулина, использующие импортную субстанцию
ОАО «Биотон-Восток», г.
Орел – совместное российско-польское производство;
ОАО «Уфа-Вита» – одно из
подразделений «Фармстандарта»;ОАО «Национальные биотехнологии», г. Оболенск, Московская обл. – экспериментальные разработки инсулина на основе собственного генно-инженерного штамма.
Слайд 14
История создания препаратов инсулина
Свиной и говяжий инсулины аморфные
Инсулины
кристаллические (цинк-инсулин водные растворы с рН 2,8-3,5)
Высокоочищенные кристаллические свиной,
говяжий и человеческий (биосинтетический) инсулины (нейтральные растворы для инъекций – подкожно и внутривенно – непродолжительное действие)
Слайд 15
Пролонгированные препараты инсулина
1. Суспензии цинк-инсулин аморфная, кристаллическая и
смешанная (3:7)
2. Суспензия протамин-цинк-инсулин кристаллическая (изофан-инсулин) (протамин – белок,
получаемый из молок осетровых рыб)3. Суспензия инсулин аминохинурид - свиной инсулин, модифицированный аминохинуридом гидрохлоридом.
Слайд 16
Классификация препаратов инсулина
1. По составу:
Монокомпонентные (свиной, говяжий, человеческий)
Смешанные
(свино-говяжий, кристаллический и аморфный).
2. По степени загрязненности проинсулином:
Обычные инсулины
(более 1% проинсулина)Монопиковые (менее 0,3%)
Улучшенные монопиковые (менее 0,005%)
Монокомпонентные (менее 0,001%)
Слайд 17
Классификация препаратов инсулина
3. По продолжительности действия:
Инсулины короткого действия
(инсулин раствор для инъекций человеческий – Хумулин, Актрапид НМ;
свиной – Актрапид, Илетин II)Инсулины средней продолжительности действия – Хумулин НПХ, Депо-инсулин-С, Инсулин
Ленте
Инсулины длительного действия – Инсулин суперленте (суспензия цинк-инсулин кристаллическая монокомпонентная)
Слайд 19 В 1979
г американскими учеными был разработан генно-инженерный метод получения гормона
роста человека. Рекомбинантный соматотропин отличается от нативного дополнительным остатком метионина на NH2 конце молекулы.В настоящее время ведется разработка способов получения гормона роста человека при культивировании клеток млекопитающих, измененных методами генной инженерии.
Слайд 22 Американская фирма
«Amgen» первой клонировала ген человеческого эритропоэтина и добилась его
экспрессии в бактериях, дрожжах и животных клетках.В настоящее время эритропоэтин получают при культивировании яйцеклеток китайского хомячка. Дальнейшая иммуноаффинная и ионо-обменная хроматографии позволяют получить гомогенный мономерный белок, не содержащий примесей.
В России НПО «Микроген» выпускает инъекционный препарат «Эритростим», очищенный до 99,5% в сывороточном альбумине на изотоническом цитратном буфере.
Слайд 24 Пептидные факторы
роста представляют собой большую группу клеточных полипептидов, влияющих на
рост и деление клеток различных типов путем взаимодействия со специфическими рецепторами на их поверхности.Группы факторов роста:
Ранозаживляющие;
Колониестимулирующие.
Слайд 25
Ранозаживляющие факторы
Эпидермальный фактор роста (ранозаживляющее действие при трансплантации
кожи, роговицы).
Фибринобластный фактор роста (стимулятор роста капилляров и
фибробластов).
Слайд 26
Ранозаживляющие факторы
3. Тромбоцитарный фактор роста (стимулятор деления
клеток гладких мышц и фибробластов).
4. Инсулиноподобный фактор роста
(регулятор роста соединительной ткани).
Слайд 27
Колониестимулирующие факторы
Макрофагальный
Гранулоцитарный
Гранулоцитарно-макрофагальный
Пример.
Препарат «Нейпоген» содержит филграстим, который
является стимулятором лейкопоэза и вырабатывается
лабораторным штаммом Escherichia coli, в которую методами генной инженерии введен ген гранулоцитарного колониестимулирующего фактора человека.
Слайд 28
Колониестимулирующие факторы являются противоопухолевыми средствами.
Ранозаживляющие и колониестимулирущие факторы
получают методами генной инженерии и культивированием клеток млекопитающих.
Основные производители
этих групп препаратов – США и Япония.Слайд 30 Цитокины - большая гетерогенная группа белков, синтезируемая лимфоретикулярными
клетками.
Они обеспечивают функционирование иммунной системы, контроль гемопоэза, действуют
на сосудистую, нервную и эндокринную системы.Наиболее изученными цитокинами являются
интерлейкины и
интерфероны.
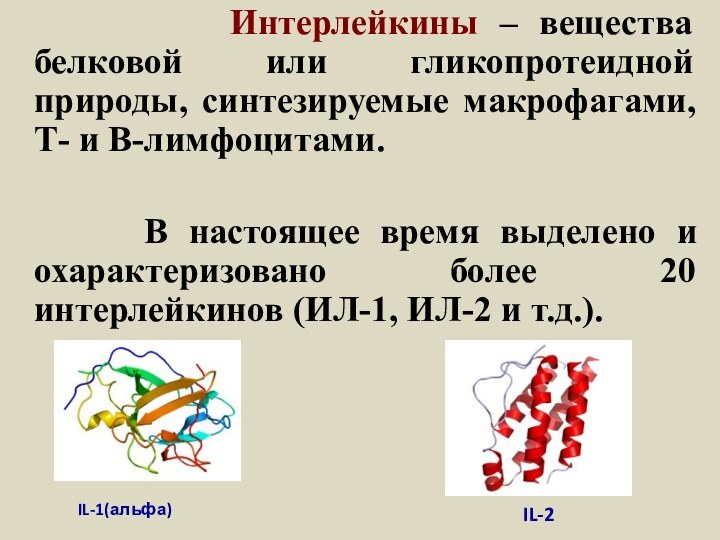
Слайд 32 Интерлейкины –
вещества белковой или гликопротеидной природы, синтезируемые макрофагами, Т- и
В-лимфоцитами.В настоящее время выделено и охарактеризовано более 20 интерлейкинов (ИЛ-1, ИЛ-2 и т.д.).
IL-1(альфа)
IL-2
Слайд 33
Схема получения интерлейкинов
Активация клеток-продуцентов.
Выделение интерлейкинов из
культуральной среды.
Концентрирование.
Очистка.
IL-10
Слайд 34
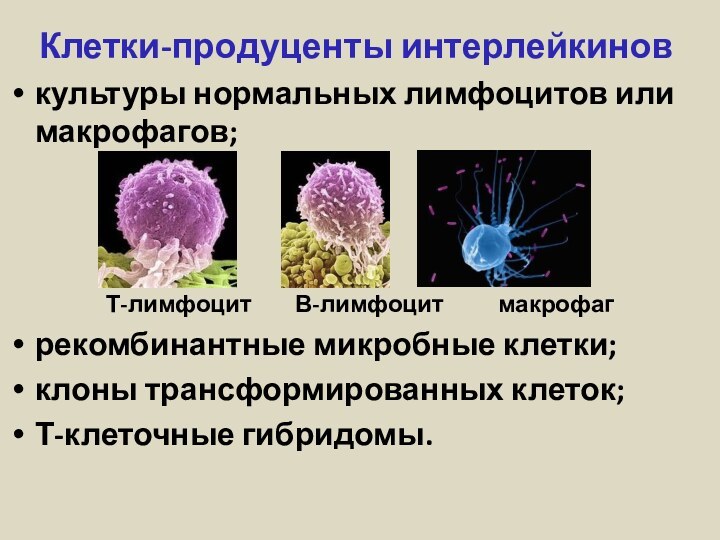
Клетки-продуценты интерлейкинов
культуры нормальных лимфоцитов или макрофагов;
Т-лимфоцит
В-лимфоцит макрофагрекомбинантные микробные клетки;
клоны трансформированных клеток;
Т-клеточные гибридомы.
Слайд 35 Для увеличения продукции
интерлейкинов, культуры клеток стимулируют митогенами – веществами, вызывающими митотическое
деление клеток.В качестве митогенов используют:
1 - глобулярные растительные белки
фитогемаглютинин и
конканавалин;
2 - компоненты клеточной стенки бактерий
мурамилдипептид.
Слайд 37 Интерфероны –
группа биологически активных белков или гликопротеинов, синтезируемых клетками организма
в ответ на воздействие интерфероногенов или в ходе иммунной реакции.К интерфероногенам относятся:
вирусы,
бактерии,
продукты их метаболизма.
Интерфероны характеризуются видоспецифичностью.
Слайд 38
Биологическая роль интерферонов
активация интерфероногенеза и защита организма от
вирусной инфекции;
стимуляция антителообразования;
торможение роста опухолевых клеток за счет усиления
цитостатической активности лимфоцитов и макрофагов;снижение активности некоторых ферментов (гидролаз, эстераз);
подавление синтеза гормонов, участвующих в регуляции и коррекции состояния организма в норме, а при патологиях, связанных с нарушениями функции иммунной системы.
Слайд 39 Классификация интерферонов в зависимости от химической природы и
клеток-продуцентов
ά-интерферон. Является белком. Получают из лейкоцитов крови человека,
подвергнутых действию вирусов-интерфероногенов.β-интерферон. Является гликопротеином. Получают из культуры клеток фибробластов, обработанных вирусом или 2-х цепочечной РНК.
γ-интерферон. Является гликопротеином. Получают из лимфобластов, выделенных от больных злокачественной лимфомой Беркита и стимулированных митогенами.
Слайд 40
Классификация интерферонов по способу получения
Природные, получаемые из
культуры клеток лейкоцитов человека, стимулированных вирусами.
Рекомбинантные, продуцируемые бактериями
со встроенным геном интерферона.
Слайд 41
Традиционная технология получения α-интерферона
Получение лейкоцитов из свежей донорской
крови.
Культивирование лейкоцитов в среде, содержащей сыворотку крови, казеин молока
и вирус Синдай 16-20 ч.
Центрифугирование, снижение рН до 2,5 для инактивации вируса.
Осаждение аммония сульфатом интерферона.
Хроматографическая очистка и концентрирование.
Стандартизация по противовирусной активности.
Растворение в стерильной воде.
Лиофилизация.
Слайд 42
Традиционная технология получения β-интерферона
Культивирование фибробластов поверхностным методом на
питательной среде с добавлением интерфероногенов (двухцепочечной РНК) и антибиотика
актиномицина Д.Выход 1 мг на 10 л культуральной жидкости.
Культура клеток живет 2-ое суток.
Слайд 43
Традиционная технология получения γ-интерферона
Культивирование лимфобластов глубинным методом на
питательной среде с добавлением интерфероногенов (вируса Синдая), кортикостероидов и
5-бромдезоксиуридина (замедление всех реакций метаболизма клеток).Выход 1 мг на 10 л культуральной жидкости.
Культура клеток живет мало.
Слайд 44
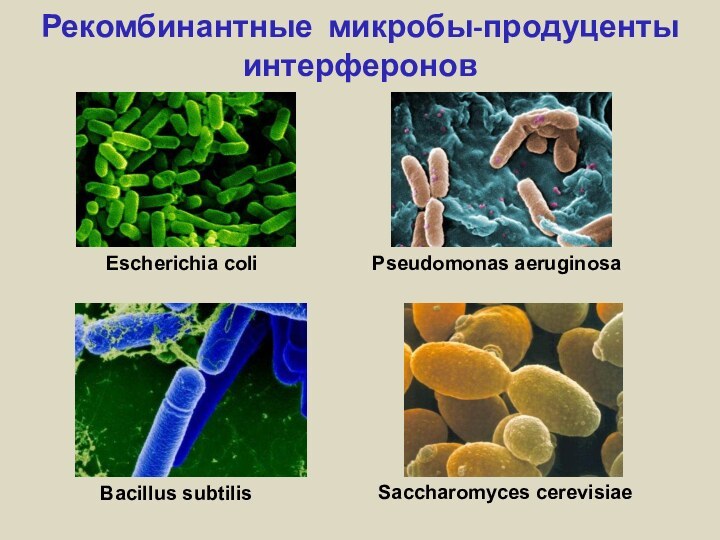
Рекомбинантные микробы-продуценты интерферонов
Escherichia coli
Pseudomonas aeruginosa
Bacillus subtilis
Saccharomyces cerevisiae
Слайд 45 Т е х н о л о г
и ч е с к а я с х
е м а п о л у ч е н и я г е н н о – и н ж е н е р н ы х и н т е р ф е р о н о вСинтез интерфероновой иРНК.
Получение рДНК, комплементарной интерфероновой иРНК.
Встраивание рДНК в плазмиду.
Введение векторной плазмиды в клетки E. coli.
Культивирование бактерий, содержащих векторную плазмиду.
Сепарирование клеток E. coli.
Дезинтеграция и экстракция клеток E. coli.
Осаждение с центрифугированием.
Высаливание интерферона из надосадочной жидкости.
Диализ осадка интерферона.
Растворение интерферона и пропускание раствора через колонку с иммуносорбентом.
Элюация интерферона с последующей хроматографией на целлюлозном катионообменнике.