Слайд 2
Тромбозы у детей
Тромбоз – патологическое состояние, связанное с
нарушением кровотока и ишемией органа вследствие закрытия тромбом просвета
сосуда. Либо избыточное образование тромботических масс, при котором развивается угроза окклюзии сосуда.
Тромбоэмболия – обтурация артериального сосуда тромбом, образовавшимся в более высоко лежащих отделах кровеносной системы и попавшим в сосуд с током крови.
Слайд 3
Артериальные и внутрисердечные тромбы
Артериальные и внутрисердечные тромбы состоят
преимущественно из тромбоцитов – белые тромбы.
Чаще – пристеночные.
Основные
факторы патогенеза: врожденная или приобретенная аномалия сосудистой стенки (ангиоматозные образования, другие врожденные нарушения развития сосудов, инфекционное или иммунное поражение эндотелия), патологическая активация тромбоцитов, абсолютный или относительный дефицит естественных антикоагулянтов.
Слайд 4
Венозные тромбы
Венозные тромбы включают в себя значительное количество
эритроцитов и большее количество фибрина – красные тромбы.
Часто
полностью закрывают просвет сосуда.
Основной механизм образования венозного тромба связан с повышением свертываемости крови и стазом. В детском возрасте ведущее значение имеет катетеризация вен. Повреждение эндотелия, аномалии развития сосудов.
Слайд 5
КАТЕТЕР-АССОЦИИРОВАННЫЕ ТРОМБОЗЫ
Предположительные механизмы (Chidi CC, King DR, Bales
ET. 1983; Wakefield A, Cohen Z, et al. 1989;
Pottecher T, Forrler M, at all.1984):
Повреждение сосудистой стенки
Нарушение характера тока крови
Введение препаратов, повреждающих сосудистую стенку
Тромбогенные материалы из которых изготовлен катетер
Локализация:
Пупочная и воротная вены
Система верхней полой вены, синдром верхней полой вены
Правое предсердие
ТЭЛА
Система нижней полой вены
Диагностика: Ангиография – наиболее чувствительный метод , УЗ - менее чувствительный - 20% , (Mitchell L, Chait P, at all. 1999)
Слайд 6
Тромбозы могут непосредственно угрожать жизни или органу и
могут не нести непосредственной угрозы.
Угрожающие тромбозы:
Любые окклюзирующие артериальные
Системы
верхней полой вены
Внутричерепные
Нижней полой вены
Почечных вен
Печеночных вен
Портальные
Не несущие непосредственной угрозы
Внутрисердечные
Артериальные пристеночные
Периферические вены
Вены конечностей
Слайд 7
ПАТОГЕНЕЗ ТРОМБОЗОВ У ДЕТЕЙ
Почти всегда комплексный
Эпизоды тромбозов у
детей предположительно возникают вследствие сочетанного воздействия наследственных и приобретенных
факторов:
Факторы тромбофилии (врожденное (наследственное) или приобретенное состояние длительно, возможно на протяжении всей жизни предрасполагающее к патологическому тромбообразованию).
Фоновое состояние + Пусковой фактор (острое потромботическое состояние)
Слайд 8
НАСЛЕДСТВЕННЫЙ ДЕФИЦИТ АНТИТРОМБИНА III
Распространенность наследственных форм достигает 2
- 20 : 10.000 (Rosenberg RD.1975; Odegard OR, Abildgaard
U. 1978; Patnaik MM, Moll S. 2008)
Частота у детей с тромбозами от 1,4% до 12,5% (deVeber G, Monagle P. 1998; Tousovská K, Dulícek P. 2000; Miljic P, Rolovic Z. 1999),
По нашим данным, при тромбозах , не связанных с катетеризацией – 16,7%
Слайд 9
НАСЛЕДСТВЕННЫЙ ДЕФИЦИТ ПРОТЕИНА С
Ожидаемая распространённость: 1 : 16.000
– 1 : 32.000 (Horellow MH., Conrad J, at
all. 1984).
Частота у детей с тромбозами 5,4% - 13,9% (Nowak-Göttl U, Debus O. 1997; Miljic P, Rolovic Z. 1999; Bonduel M, Sciuccati G. 1999)
Слайд 10
НАСЛЕДСТВЕННЫЙ ДЕФИЦИТ ПРОТЕИНА S
Распространённость в популяции не менее
5:100.000 (www.isth.org - данные международного регистра мутаций у лиц
с дефицитом прот S)
Частота у детей с тромбозами 1,0 - 3.0% - 14.3% (Koster T, Rosendaal FR. At all. 1995; Srur E, Vargas C. at all. 2004; Hiwood S, Liedner R, at all. 2005)
Слайд 11
Приобретённый дефицит естественных антикоагулянтов:
антитромбина III, протеина С,
протеина S:
Причины:
Инфекция:
менингококкцемия
сепсис различной этиологии
ВИЧ
Поражение печени
Дефицит витамина К
Приём непрямых
антикоагулянтов
Ингибитор
Онкологические заболевания
Системные заболевания
Неспецифический язвенный колит
Слайд 12
ПРОТРОМБОТИЧЕСКИЕ ПОЛИМОРФИЗМЫ
Фактор V R506Q G>A (Лейден)
Повышена устойчивость ф.V
к инактивации протеином С. Обусловливает повышенную резистентность к активированному
протеину С
Распространённость в популяции от <1% в Азии и Африке до 8% (0,1% гомозигот) в Западноевропейской популяции (Dahlback B. 1995; Rees D, Cox M., at all. 1995; Simioni P, Sanson BJ., at all. 1999)
Риск тромбоза у гетерозигот в 5 – 10 раз выше, у гомозигот – в 80 раз выше (Rosendaal FR. 1999)
Слайд 13
ПРОТРОМБОТИЧЕСКИЕ ПОЛИМОРФИЗМЫ
Полиморфизм гена протромбина - (G20210А)
Значимо повышена концентрация
протромбина (тест генерации тромбина) в плазме
Распространённость в популяции от
2% до 5% (Cumming AM, Keeney S, at all. 1997)
Риск тромбоза повышается в 2 – 6 раз (Rosendaal FR. 1999; Martinelli I, Taioli E, at all. 1999.)
Слайд 14
ГИПЕРГОМОЦИСТЕИНЕМИЯ
оказывает протромботическое и проатеросклеротическое воздействие
У детей генетически обусловлена:
Полиморфизм
гена метилентетрагидрофолатредуктазы
Полиморфизмы гена метионин-синтазы редуктазы
Полиморфизмы гена метионин-синтазы
Др.
Реже возникает вследствие:
Приёма метатрексата
Дефицита фолатов
Дефицита витаминов В6, В12
Слайд 15
ДРУГИЕ НАСЛЕДСТВЕННЫЕ ФАКТОРЫ ТРОМБОФИЛИИ
Полиморфизмы тромбоцитарных рецепторов
Другие полиморфизмы (изучаются)
Дисфибриногенемии
Гиперлипопротеинемия
(a)
Митохондриальная патология
Слайд 16
КАТЕТЕРИЗАЦИЯ СОСУДОВ
80% венозных тромбозов у новорождённых и 50%
венозных тромбозов у детей старше месяца связаны с применением
внутрисосудистых катетеров (Monagle P, Michelson AD, at all. 2001)
При применении катетеров в 5% случаев симптоматические тромбозы. Скрининг выявляет тромбозы до 50%! (Revel-Vilk S. 2006).
По другим данным симптоматические тромбозы:
2,2% центральных вен у тяжелобольных детей от 1 мес. до 18 лет (Karapinar B, Cura A. 2007)
1,2% – 13% детей с онкогематологическими заболеваниями (Boersma RS, Jie KS, at all. 2008)
Слайд 17
КАТЕТЕРИЗАЦИЯ СОСУДОВ
Частота возрастает при установке катетера в бедренной
вене. Риск тем выше, чем дольше катетер находится в
вене. (Casado-Flores J, Barja J, at all. 2001)
15-летнее наблюдение 22 детей с тяжелой гемофилией, получавших профилактическую заместительную терапию с использованием катетеров показало, что частота тромбозов составила 1 на 7529 дней установки катетера. (Domm JA, Hudson MG, at all. 2003)
Мы наблюдали 2 эпизода тромбоза при использовании подключичного катетера у детей с ингибиторной формой гемофилии при лечении массивных гематом
Слайд 18
СЕПСИС
Наиболее опасен грамм-отрицательный, в том числе менингококковый сепсис
Бак.
эндотоксины:
активируют свёртывание через ф.XI (Minnema MC, Pajkrt M
D, at all. 1998)
повышают уровень tPA, комплекса плазмин/α2-антиплазмин (van Deventer SJH, Buller HR, at all 1990)
активируют ф.X, возможно через ТФ-ф.VII (ten Cate JW, van der Pol T, at all. 1997)
Снижается содержание тромбомодулина на эндотелии, повышается в плазме; снижается концентрация антигена протеинов С, S, антитромбина (Faust SN, Levin M, at all. 2001)
Повышается содержание тканевого фактора и PAI-1 (Green J, Doughty L, at all. 2002).
Слайд 19
ДРУГИЕ ИНФЕКЦИИ
Ветряная оспа, герпес зостер приводят к транзиторной
выработке ингибирующих антител к протеину S. Следствие - фульминантная
пурпура и др. тромбозы (Levin M, Elev BS at all. 1995)
Неспецифическая инфекция может приводить к развитию ингибитора к протеину S (Levin M, Elev BS at all. 1995)
Менингит, вызываемый Streptococcus pneumoniae, Haemophilus influenzae, Neiserria meningitidis; туберкулёз - ишемические инсульты (Takeoka M, Takahashi T. 2002)
Слайд 20
ДРУГИЕ ИНФЕКЦИИ
Синдром Лемьера – септический тромбофлебит внутренней ярёмной
вены, вызванный Fusobacterium – следствие перенесённой ангины.
Инфекционное поражение кожи,
абсцессы, остеомиелит ведут к тромбозу глубоких вен, часто региональных.
Инфекция ЛОР-органов ведет к тромбозу венозных синусов черепа
Слайд 21
ОНКОЛОГИЧЕСКИЕ ЗАБОЛЕВАНИЯ
Частота при ОЛЛ 1% - 36% (Pavne
JH, Vora AJ. 2007)
Причина тромбозов при ОЛЛ (Athale UH,
Chan AK. 2003, Novak-Gettl U, Kenet J. 2009)
индуцированные аспарагиназой и стероидами
снижение активности антитромбина и плазминогена
повышение активности ф.VIII, ф. Виллебранда, PAI-1
применение венозных катетеров
генетические факторы
Слайд 22
ОНКОЛОГИЧЕСКИЕ ЗАБОЛЕВАНИЯ
Из 70 детей с саркомами 14,3% развили
клинически значимый тромбоз, в 95% связанный с катетерами (Athale
U, Cox S, at all. 2007).
Из 75 детей с саркомами 12% развили клинически значимый тромбоз, в 95% связанный с катетерами (Athale U, Nagel K, at all 2008).
Онкологическое заболевание является независимым фактором риска тромбоза: повышение генерации тромбина при ОЛЛ (Athale UH, Chan AK. 2007)
Слайд 23
НЕФРОТИЧЕСКИЙ СИНДРОМ
Частота тромбозов при НС до 28% (Cilak
A, Emre S, at all. 2000)
Чаще при вторичных формах
(Abella E. 1994)
Артериальные и венозные тромбозы различной локализации (Andrew M, Brooker LA. 1996)
Чаще всего развиваются в течение первых 3 месяцев после диагностики (Andrew M, Montgomery RR. 1995)
Патогенез: повышение уровня фибриногена и потеря с мочой мелких белков, особенно антитромбина III, гемоконцентрация, повышение вязкости крови (Andrew M, Brooker LA. 1996; Schnaper HW. 2001).
Слайд 24
ДРУГИЕ ФАКТОРЫ ПАТОЛОГИЧЕСКОГО ТРОМБООБРАЗОВАНИЯ
Аутоиммунные заболевания (СКВ, антифосфолипидный синдром,
болезнь Бехчета и др.)
Сахарный диабет,
ВИЧ
Врожденные пороки развития сердца и
сосудов
Заболевания печени,
Гемолитические анемии (талассемия, серповидно-клеточная анемия)
Повышение вязкости крови (полицитемия, потеря жидкости)
Пароксизмальная ночная гемоглобинурия
Операция или травма,
Слайд 25
ДИАГНОСТИКА (Roy et al 2002).
Типичная клиническая картина
УЗДГ -
наиболее доступная, безопасная, часто используемая методика, расхождения интерпретации до
90%!
Ангиография – «золотой стандарт»
МРТ, КТ-ангиография
Диагностика церебральных тромбозов
ТЭЛА
Слайд 26
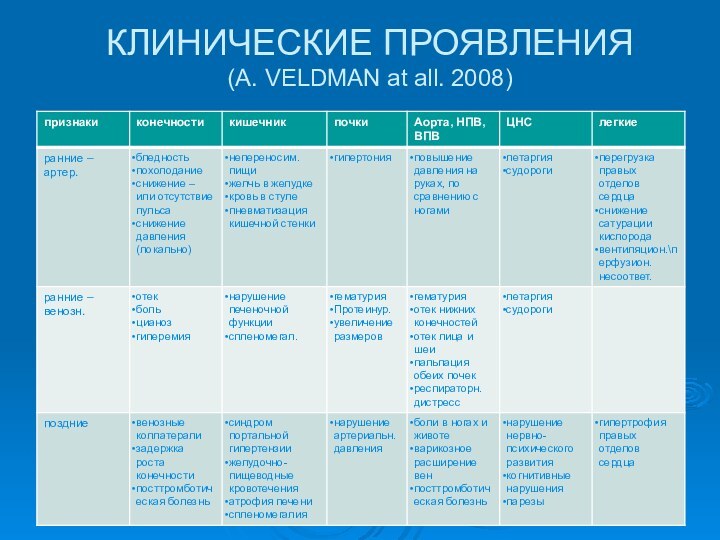
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
(A. VELDMAN at all. 2008)
Слайд 27
ТЕРАПИЯ
(Paul Monagle, Elizabeth Chalmers, Anthony Chan, Gabrielle
deVeber, Fenella Kirkham, Patricia Massicotte and Alan D. Michelson
2008)
При назначении антикоагулянтов прогноз лучше:
Смертность ниже
Резидуальные изменения меньше
Время восстановления короче
Принципы:
Максимально раннее начало
Применение наиболее эффективных схем и доз
Достаточная длительность
Лабораторный и клинический контроль
Слайд 28
ТЕРАПИЯ
Максимально раннее начало
Применение наиболее эффективных препаратов и доз
Достаточная
длительность лечения
Инструментальный контроль
Лабораторный контроль
Заместительная терапия: СЗП, АТIII, протеин С
Слайд 29
ОСНОВАНИЯ ДЛЯ НАЧАЛА ТЕРАПИИ
При угрожающих тромбозах:
Клинические проявления и
отсутствие противопоказаний
Клинические проявления, инструментальные данные и отсутствие абсолютных противопоказаний
При
неугрожающих тромбозах
Клинические проявления, данные инструментального обследования и отсутствие противопоказаний
Данные инструментального обследования и отсутствие противопоказаний
Слайд 30
ОСНОВНЫЕ КОМПОНЕНТЫ ТЕРАПИИ
Гепарины: НФГ или НМГ
Тромболитики:
актилизе (альтеплаза)
тенектеплаза
урокиназа
Хирургическое
лечение
Заместительная терапия:
антитромбин III
протеин С
СЗП
Непрямые антикоагулянты
Слайд 31
ДОЗЫ НФГ ГЕПАРИНА
(Paul Monagle, Elizabeth Chalmers, Anthony
Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and Alan
D. Michelson 2008)
Нагрузочная доза: гепарин 75Ед/кг внутривенно за 10 минут;
Начальная поддерживающая доза: 28 Ед/кг/час < 1 года, и 20 Ед/кг/час для >1 года;
Целевое АЧТВ 60-85 сек. (что соответствует уроню анти-Ха активности 0,35-0,7);
АЧТВ измерять через 4 часа после введения нагрузочной дозы и каждые 4 часа после изменения дозы
По достижению терапевтического интервала АЧТВ – ежедневно ОАК и АЧТВ.
Слайд 32
ДОЗЫ НМГ ГЕПАРИНА
(Paul Monagle, Elizabeth Chalmers, Anthony
Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and Alan
D. Michelson 2008)
Слайд 33
КОНТРОЛЬ ЛЕЧЕНИЯ НИЗКОМОЛЕКУЛЯРНЫМИ ГЕПАРИНАМИ
(MONAGLE P, CHALMERS E, AT
ALL. 2008)
Базируется на определении анти-ф.Xа активности (анализ проводится через
4 – 6 часов после п/к введения НМГ)
Терапевтические значения у детей не определены
Данные экстраполированные из терапевтической практики:
лечебный уровень 0,5 – 1,0 ед/мл (по некоторым данным от 0,3 до 0,7)
проф. уровень 0,1 – 0,3 ед/мл
Слайд 34
Тромболитическая терапия
Более эффективна при артериальных тромбозах
Существует высокий (до
40 – 50%) риск значимых геморрагических осложненй
Риск осложнений пропорционален
эффективности
Слайд 35
Тромболитическая терапия
Урокиназа
Рекомбинантный человеческий тканевой активатор плазминогена (Актелизе, Альтеплазе)
Остальные
тромболитики (стрептокиназа, и др) либо противопоказаны, либо эффективность и
безопасность не исследованы
Слайд 36
Тромболитическая терапия
Противопоказания
Показания:
Массивные тромбозы, опасные для жизни тромбозы, тромбозы
повреждающие (жизненно важные) органы
Слайд 37
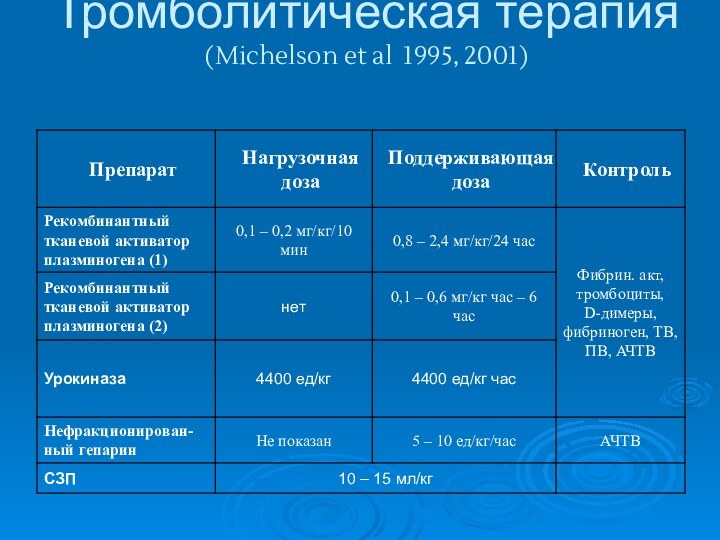
Тромболитическая терапия (Michelson et al 1995, 2001)
Слайд 38
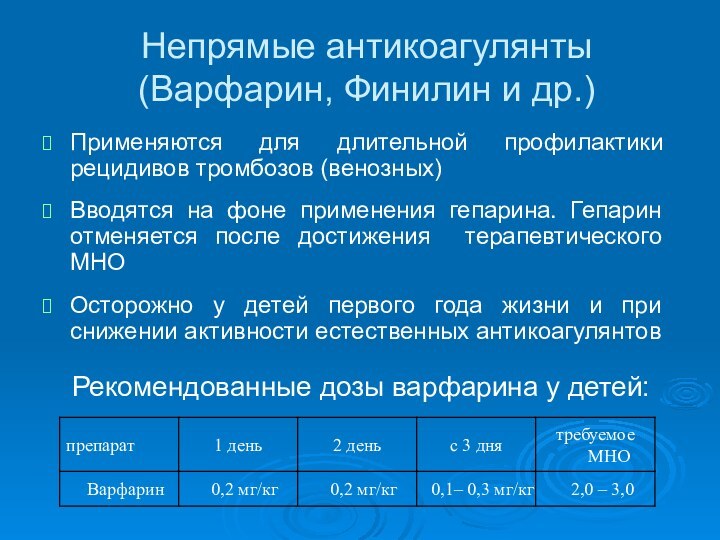
Непрямые антикоагулянты (Варфарин, Финилин и др.)
Применяются для длительной
профилактики рецидивов тромбозов (венозных)
Вводятся на фоне применения гепарина. Гепарин
отменяется после достижения терапевтического МНО
Осторожно у детей первого года жизни и при снижении активности естественных антикоагулянтов
Рекомендованные дозы варфарина у детей:
Слайд 39
Дезагреганты
Применяются для длительной профилактики артериальных тромбозов
Ацетил салициловая кислота
(ТромбоАСС) – 1 – 3 – 5 мг/кг в
сутки
Клопидогрель противопоказан детям
Применение совместно с антикоагулянтами значимо повышает риск тромбоза
Слайд 40
Заместительная терапия при лечении острых тромбозов
Антитромбин III: уровень
не менее 80%
Разовая доза 30 – 100 МЕ/кг
Кратность зависит
от потребления
Лабораторный контроль
Протеин С:
20 - 60 МЕ/кг разово,
Каждые 6 - 12 часов до купирования явлений тромбоза
Не использовать при сепсисе, дыхательных нарушениях, на фоне наркоза
СЗП 10 – 15 мл/кг разово
Слайд 41
ДЛИТЕЛЬНОСТЬ ТЕРАПИИ
Венозные тромбозы:
Не менее 6 недель
До 3 х
месяцев
При необходимости до 6 месяцев
Артериальные тромбозы
Не менее 3 дней
До
10 дней
Слайд 42
ФАКТОРЫ РЕЦИДИВА ТРОМБОЗА У ДЕТЕЙ С ВЕНОЗНЫМИ ТРОМБОЗАМИ
ЦНС (МУЛЬТИЦЕНТРОВОЕ ИССЛЕДОВАНИЕ)
(Kennet G, Kirkham F, at all. 2007)
наблюдали
396 пациентов в возрасте от 0 до 18 лет, в среднем 5,3 года.
250 (65%) получали НФГ или НМГ; 165 (43%) в дальнейшем длительно получали НМГ или варфарин
12 (3%) погибли в острой фазе
22 (6%) имели рецидивы тромбоза различной локализации в течение 6 мес. после первого эпизода
Слайд 43
ФАКТОРЫ РЕЦИДИВА ТРОМБОЗА У ДЕТЕЙ С ВЕНОЗНЫМИ ТРОМБОЗАМИ
ЦНС (МУЛЬТИЦЕНТРОВОЕ ИССЛЕДОВАНИЕ)
(Kennet G, Kirkham F, at all. 2007)
Рецидивы не были связаны с текущими заболеваниями и возникали у детей с первым эпизодом в возрасте старше 2 лет
Рецидивы были связаны:
отсутствие терапии антикоагулянтами
возраст развития первого эпизода старше 2 лет
персистирующая венозная окклюзия
полиморфизм гена протромбина G20210A
Слайд 44
РИСК РЕЦИДИВОВ ВЕНОЗНЫХ ТРОМБОЗОВ У ДЕТЕЙ С НЕСКОЛЬКИМИ
ПРОТРОМОТИЧЕСКИМИ ФАКТОРАМИ
(Nowak-Gettl U, Junker R, at all. 2001)
наблюдали 301
реб. от 0 до 18 лет, в среднем 6 лет со спонтанными венозными тромбозами
катамнез, в среднем, 7 лет (от 6 мес, до 15 лет) после прекращения приёма антикоагулянтов
рецидивы у 21,3%
период от окончания терапии антикоагулянтами до рецидива - от 7 нед. до 15 лет, в среднем 3,5 года
период до рецидива был достоверно короче у детей с несколькими генетическими факторами риска
Слайд 45
ПРОФИЛАКТИКА РЕЦИДИВОВ
АФС – постоянно препаратами АВК (МНО 2
– 3)
Дефицит протеина С, S, антитромбина III с уровнем
активности менее 50% и развитием идеопатических, либо рецидивирующих тромбозов
постоянно препараты АВК (МНО 2,5 – 3,5),
заместительная терапия протеин С (20 – 60 МЕ/кг), антитромбин III (до 80 - 100 МЕ/кг), СЗП при повышении Д-димеров более 1000 или рецидивах тромбозов на фоне целевой гипокоагуляции
Контроль – Д-димеры, МНО, активность антитромбина, протеина С и S
Повторный идеопатический тромбоз – постоянно препараты АВК (МНО 2 – 3)
Продолжающееся воздействие протромботического фактора
Слайд 46
ПРОФИЛАКТИКА РЕЦИДИВОВ
Первично перенесенный ишемический инсульт у детей после
периода новорожденности – препараты ацетилсалициловой кислоты (1 – 5
мг/кг в сут) – до 3х лет при отсутствии значимых протромботических факторов
Повторный ишемический инсульт или первично перенесенный ишемический инсульт при наличии гемодинамически значимой аномалии развития сосудов – препараты ацетилсалициловой кислоты (1 – 5 мг/кг в сут) длительно
Тяжелые травмы, операции на сосудах, ортопедические операции, установка венозного катетера, длительный постельный режим – гепарины на период воздействия неблагоприятного фактора
Слайд 47
ПРОФИЛАКТИКА РЕЦИДИВОВ
(спорные показания)
Сохраняющееся после перенесенного тромбоза гемодинамически значимое
сужение сосуда – препараты АВК (МНО 2 – 3)
Идиопатический
венозный тромбоз у детей от 12 лет.
Перенесенный тромбоз с выявленным снижением активности антикоагулянтов в диапазоне 50 – 70%
Умеренное повышение титра АФА у грудных детей, перенесших тромбоз в неонатальном периоде
Перенесенный венозный тромбоз сосудов ног у пациентов с нижней параплегией
Неонатальные инсульты
Слайд 48
ТРОМБОЗ ПОЧЕЧНЫХ ВЕН
(Andrew M, Monagle P, Brooker
L. 2000)
У 80% возникают преимущественно на 1 месяце или
внутриутробно.
Предположительные механизмы:
Асфиксия
Шок
Полицитемия
«Синие» ВПС
Диабет у матери
Дегидратация
Сепсис
Локализация:
76% - односторонняя без преимущественной локализации
24% - двусторонняя
Диагностика:
ультразвуковое сканирование
КТ, МРТ
Слайд 49
ЭКСТРАЦЕРЕБРАЛЬНЫЕ АРТЕРИАЛЬНЫЕ ТРОМБОЗЫ
Чаще иатрогенные (Flanigan DP, Keifer TJ,
at all. 1983; White JJ, Talbert JL, Haller JA.
1968)
Локализация:
При иатрогенных – зависит от положения катетера
Спонтанные – чаще артерии конечностей
Диагностика:
ультразвуковое сканирование
рентгеноконтрастные исследования проводятся очень редко
Прогноз: экстренные состояния, при отсутствии немедленной терапии исход неблагоприятный
Слайд 50
ИШЕМИЧЕСКИЕ ИНСУЛЬТЫ (deVeber at all. 2000, 2001)
Предрасполагающие факторы
Гиперкоагуляция
у матери
Асфиксия
Родовая травма
Внутрисердечный шунт (сброс право-лево)
Высокий гематокрит
Обезвоживание
Диагностика сложна:
МРТ,
(НСГ?)
Клиника – малоинформативна
Исходы:
Смерть < 10%
Персистирующий неврологический дефицит - 2/3 выживших
Отсутствие остаточных явлений - 1/3 выживших
Слайд 51
ТРОМБОЗЫ ВЕНОЗНЫХ СИНУСОВ
Предрасполагающие факторы (deVeber GA, at all.
2000, 2001) :
Родовая травма
Другая патология родов, в том числе
асфиксия
Высокий гематокрит
Обезвоживание
Постнатальная патология, в т.ч. инфекция
Диагностика сложна: (Ludwig B, Brand M, at all. 1980; Govaert P, Voet D, et al. 1992; deVeber GA, at all. 2000, 2001)
МРТ, КТ, (НСГ?)
Клиника – малоинформативна
Исходы (Barron TF, Gusnard DA, at all. 1992, deVeber, at all. 2000, 2001)
Смертность 7% – 12%
Персистирующий неврологический дефицит , в том числе внутричерепная гипертензия - 33% - 61%
Судороги 21%
Рецидивирующие церебральные или системные тромбозы < 5% - 9%
Слайд 52
ФУЛЬМИНАНТНАЯ ПУРПУРА
Причина – гомозиготный дефицит протеинов С или
S
Проявления:
Кожный синдром
Внутриутробное поражение мозга и глаз
Диагностика:
Клиника
Определение активности протеина
С или S (активность не определяется)
Терапия проявлений
Концентрат протеина С 30 – 60 – 100 МЕ/кг разово активность не ниже 10%
СЗП (при дефиците протеина S)
НФГ, НМГ
Непрямые антикоагулянты пожизненно с МНО – 3,5
Слайд 53
ФУЛЬМИНАНТНАЯ ПУРПУРА
Причина – гомозиготный дефицит протеинов С или
S
Проявления:
Кожный синдром
Внутриутробное поражение мозга и глаз
Диагностика:
Клиника
Определение активности протеина
С или S (активность не определяется)
Терапия проявлений
Концентрат протеина С 30 – 60 – 100 МЕ/кг разово активность не ниже 10%
СЗП (при дефиците протеина S)
НФГ, НМГ
Непрямые антикоагулянты пожизненно с МНО – 3,5
Слайд 54
ПРОТРОМБОТИЧЕСКИЕ ФАКТОРЫ
Дефицит антитромбина III (Chowdhury V, Lane DA,
et al. 1994; Hakten M, Deniz U, at al.
1989; Bjarke B, Herin P, at al. 1974; Schander K, Niessen M, at al. 1980; Brenner B, Fishman A, at al. 1988; Peeters S, Vandenplas Y, at al. 1993; Soutar R, Marzinotto V, at al. 1993; Newman RS, Spear GS, at al. 1998; Jochmans K, Lissens W, at al. 1994; De S, V, Leone G, De Carolis MP, et al. 1987.)
Дефицит протеина С (Auletta MJ, Headington JT. 1988; Bauer K. 1998)
Дефицит протеина S (Mahasandana C, Suvatte V, et al. 1990; Gomez E, Ledford MR, at al. 1994; Marlar RA, Neumann A. 1990; Mahasandana C, Suvatte V, at al. 1990; Pegelow CH, Ledford M. at al. 1992)
Дефицит плазминогена (Mingers AM, Philapitsch A, at al. 1999; Schuster V, Mingers AM, at al. 1997)
Мутация протромбина G20210А (Dilley A, Austin H, et al. 1998)
Мутация фактора V (Лейден) (Pipe SW, Schmaier AH, et al. 1996; Gurgey A, Mesci L, at al. 1996; Kodish E, Potter C, at al. 1995; Haffner D, Wuhl E, at al. 1996)
Слайд 55
ТЕРАПИЯ НЕОНАТАЛЬНЫХ ТРОМБОЗОВ
(Paul Monagle, Elizabeth Chalmers, Anthony
Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and Alan
D. Michelson 2008)
При назначении антикоагулянтов прогноз лучше:
Смертность ниже
Резидуальные изменения меньше
Время восстановления короче
Слайд 56
ТЕРАПИЯ НЕОНАТАЛЬНЫХ ВЕНОЗНЫХ ТРОМБОЗОВ
(Paul Monagle, Elizabeth Chalmers,
Anthony Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and
Alan D. Michelson 2008)
НМГ п/к х 2 раза/сут (анти Xа активность – 0,5 – 1,0)
или
НФГ в/в непрерывно (анти Xа активность – 0,5 – 1,0 или по АЧТВ 60 – 85 сек)
Длительность 6 нед – 3 мес., при необходимости до 6 мес.
Тромболизис только при критическом состоянии или угрозе потери органа
Слайд 57
ТЕРАПИЯ ТРОМБОЗОВ ПОЧЕЧНЫХ ВЕН
(Paul Monagle, Elizabeth Chalmers,
Anthony Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and
Alan D. Michelson 2008)
Односторонний тромбоз – терапия НМГ или НФГ
Двусторонний тромбоз – тромболизис с последующей терапией НМГ до 3 мес. При противопоказании к тромболизису – терапия НМГ или НФГ
Слайд 58
ТЕРАПИЯ ТРОМБОЗОВ ВЕНОЗНЫХ СИНУСОВ
(Paul Monagle, Elizabeth Chalmers,
Anthony Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and
Alan D. Michelson 2008)
Без значимого внутричерепного кровоизлияния – терапия НМГ или НФГ длительность от 6 нед. до 3 мес.
Со значимым внутричерепным кровоизлиянием – мониторинг; при нарастании тромбоза – терапия НФГ или НМГ
При сохранении признаков тромбоза – продолжить ещё 3 мес.
Слайд 59
ТЕРАПИЯ ИШЕМИЧЕСКИХ ИНСУЛЬТОВ
(Paul Monagle, Elizabeth Chalmers, Anthony
Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and Alan
D. Michelson 2008)
При отсутствии очагов эмболии – терапия антикоагулянтами не показана
Рецидивы инсультов – показана терапия антикоагулянтами или дезагрегантами
Слайд 60
ТЕРАПИЯ ИШЕМИЧЕСКИХ ИНСУЛЬТОВ
(Paul Monagle, Elizabeth Chalmers, Anthony
Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and Alan
D. Michelson 2008)
Первичный инсульт: при отсутствии очагов эмболии – терапия антикоагулянтами не показана
Рецидивы инсультов – показана терапия антикоагулянтами или дезагрегантами
Слайд 61
ГОМОЗИГОТНЫЙ ДЕФИЦИТ ПРОТЕИНА С
(Paul Monagle, Elizabeth Chalmers,
Anthony Chan, Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and
Alan D. Michelson 2008)
При наличии клиники (до разрешения клинических проявлений):
СЗП 10 – 20 мл/кг каждые 12 часов
Концентрат протеина С 20 – 60 МЕ/кг
Длительное ведение:
Непрямые антикоагулянты
Препараты протеина С
НМГ
Слайд 62
АРТЕРИАЛЬНЫЕ ТРОМБОЗЫ
(Paul Monagle, Elizabeth Chalmers, Anthony Chan,
Gabrielle deVeber, Fenella Kirkham, Patricia Massicotte and Alan D.
Michelson 2008)
Угроза потери органа:
тромболизис
при противопоказании к тромболизису – хирургическое удаление тромба
Нет угрозы потери органа:
НФГ не менее 5 – 7 дней