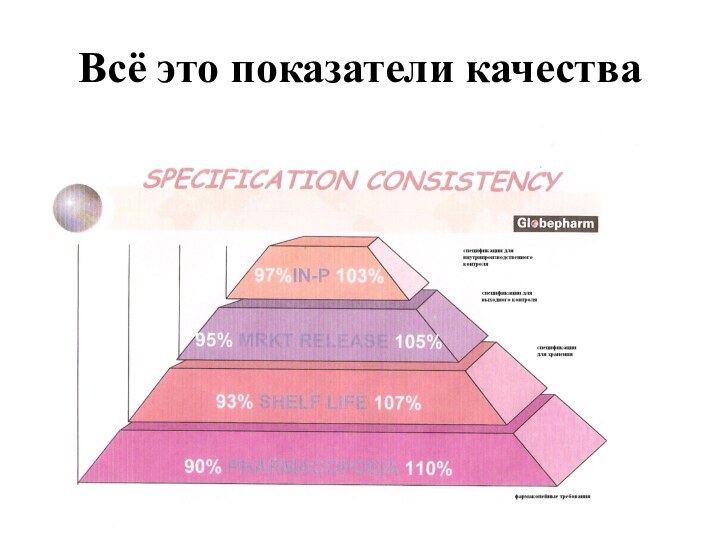
Слайд 2
Гармонизация и глобализация
ВОЗ: начало гармонизации в фармсекторе
(50-е годы)
Глобальная теледеревня Маршала Маклюэна (1960-е годы)
(Западно)европейская экономическая интеграция:
Общий рынок (1950-е/1960-е годы)
Стратегическая цель - предотвращение Третьей мировой войны
Гармонизация регуляторных механизмов в фармсекторе (Директива 65/65 ЕЕС)
Слайд 3
Гармонизация в фармсекторе:
определение
Научное сотрудничество на международном уровне,
основанное на активном участии сторон, комплексном
подходе, и ведущее к
единообразным, надежным,
не односторонним и сбалансированным решениям,
в основном свободном от эмоциональных компонентов,
в результате чего обеспечивается наивысшая
(из возможных) степень защиты интересов пациентов
во всем мире.
Из материалов ICH, 1991 г.
Слайд 4
Отраслевая гармонизация
в России
Стратегия лекарственного обеспечения населения РФ на
период до 2025 года предусматривает, в т.ч. «гармонизацию требований
к проведению доклинических испытаний и клинических исследований, организации производства, хранению, транспортированию, отпуску, уничтожению лекарственных средств, а также правил и форм оценки соответствия с учетом международных стандартов»;
Согласно Положению о Координационном совете в сфере обращения лексредств и медизделий при Минздраве РФ совет призван, среди прочего, анализировать мировой опыт в целях внесения изменений в действующие нормативно-правовые акты, в т.ч. и на основе гармонизации с мировыми нормами
Слайд 5
Парламентские слушания
21 марта с.г., Москва. Парламентские слушания на
тему: «Законодательные аспекты государственного регулирования качества лекарственных средств»
почти все
выступавшие говорили о необходимости гармонизации
В одном выступлении предлагалось перейти от слов к делу и создать раб. группу по гармонизации
Слайд 6
Гармонизация –
с чего начать?
Очевидно, с «видения» (Vision)
Видение:
Оценка сегодняшнего
состояния
Определение желаемого состояния
Сопоставление первого со вторым (gap анализ и
выявление излишнего)
Слайд 7
Пример видения: Система фармацевтического качества
Гармонизированная (отраслевая) система качества,
применимая в течение всего жизненного цикла
лекарственного продукта, основанная
на
интегрированном подходе к управлению рисками
и к научным данным.
ICH, Брюссель, июнь 2003
Видение
Слайд 8
GxP в России: приоритеты
GMP – (?)
GLP – +
GCP
– +
GDP – ?
GPP – ?
GSP – нет
Слайд 9
GxP – забытые аспекты
Good Regulatory Practice (GRP)
Good Pharmacopoeial
Practice
Не менее важный элемент - регистрация препаратов:
ОТД ICH
Процедуры
Слайд 10
GMP: российская практика
Текст правил GMP подготовлен, но не
утвержден
Инспектората по GMP нет
Положения об уполномоченном лице нет
Санкции к
нарушителям слабы
Надежда на внедрение снизу -
по примеру ИСО 9000
Слайд 11
Роль Инспектората по GMP
Основа внедрения – замечания Инспектората
по GMP
В США – Форма 483
Инспекторат по GMP –
образец для групп самоинспектирования производителей
Попытки внедрения без этого – вытаскивание себя из болота по методу барона Мюнхгаузена
Слайд 12
Санкции к нарушителям
Санкции к нарушителям – второй механизм
внедрения GMP
Цель – не удушить отрасль,
а сделать несоблюдение правил
экономически невыгодным
Слайд 13
GLP: российская практика
Текст правил GLP утвержден в 2009
г.:
ГОСТ Р 53434 Принципы надлежащей лабораторной практики
Всего 1 лаборатория
в стране полностью отвечает этим правилам
по оценке специалистов из Словакии
Национальная программа реализации принципов GLP принята 28.12.12
Слайд 14
GСP: российская практика
Текст правил GLP утвержден в 2005
г.:
ГОСТ Р 52379 Надлежащая клиническая практика
Ряд клинических баз позитивно
оценен инспекторами FDA США
Инспекторы по GСP есть; инспектората нет
Слайд 15
GDP: российская практика
Официальный текст утвержден в 2010
г.:
Правила оптовой торговли лекарственными средствами для медицинского применения.
Приказ Минздравсоцразвития РФ от 28 декабря 2010 г. N 1222н
До этого было опубликовано Руководство по надлежащей практике оптовой реализации лекарственных препаратов для медицинского применения. Методические рекомендации (перевод Руководства ЕС)
Слайд 16
В российском нормативе GDP
3 стр. и 14 пунктов;
терминологической части нет
Документ вполне мог бы быть составлен
в СССР, в 70-х – 80-х гг. прошлого века.
Слайд 17
В Европейском руководстве
(от 7 марта 2013 №
2013/C 68/01)
14 стр., преамбула, 10 глав, около 40
разделов, терминологическая часть
Отмечается, что оптовое распределение препаратов – важная часть интегрированного управления цепочкой (системой) лекарственного снабжения
Упоминается противодействие распространению фальсифицированных препаратов, система качества, управление рисками качества и др. элементы GMP
Слайд 18
Качество субстанций –
опыт ЕС
В 2011-2013 гг. прият
ряд важных документов и проектов документов
В июле 2011 была
прията Директива 2011/62/EU,
Предусматривается принятие современных требований GMP
Проект требований к импортерам, производителям и дистрибьюторам АФИ
Слайд 19
Качество субстанций –
опыт ЕС - 2
Планируется оценка
регуляторных систем третьих стран в части контроля производства АФИ
Готовится проект руководства по принципам надлежащей практики распределения АФИ
А также проект руководства по оценке рисков в связи с принятием соответствующих правил GMP для вспомогательных веществ
Слайд 20
GPP: российская практика
Приказ Минздрава РФ от 4 марта
2003 г. № 80
Отражает состояние вопроса на тот период
(более или менее)
Слайд 21
GPP: мировая практика
Новая концепция: Фармацевтическая (лекарственная) помощь (Pharmaceutical
care) –
Документ FIP-ВОЗ Developing pharmacy practice. A focus on
patient care. HANDBOOK – 2006 EDITION. (WHO/PSM/PAR/2006.5)
Акцент в деятельности провизоров перемещается от товара (ЛС) к человеку (пациенту)
Стратегическая цель – не рост продаж, а забота о пациенте
Принятие провизором на себя части ответственности за лечебный исход пациента (patient outcome)
Слайд 22
Лекарственная (фармацевтическая) помощь: компоненты
Непрерывное профессиональное развитие на платформе
Лекарственной помощи
вместо фармобразования на всю жизнь по традиционным программам
В
аптеке – общение с клиентами на платформе Лекарственной помощи
В общине разъяснение своей роли
В обществе (по возможности) – участие в законотворчестве, регуляторной и надзорно-контрольной работе по лекобеспечению
Слайд 23
Надлежащая регуляторная практика (GRP)
Общество предъявляет требования к регуляторам
Контрольно-надзорные
органы должны иметь систему качества
Требования и процедуры оценки д.б.
прозрачны
Чем больше прозрачности, тем меньше уязвимость для коррупции
Слайд 24
Прозрачность
Регуляторные процедуры д.б. транспарентны (прозрачны)
т.е. изложены
письменно
понятным языком
в части сферы деятельности, прав, функций и ответственности
в
особенности в части ответственности:
кто за что отвечает
Слайд 25
Good Pharmacopoeial Practice
Совещания ВОЗ – 2012 г. (Амстердам)
и др.
Нормативный документ – фармакопея в целом, а не
одна статья
Качество лекарств – не соответствие фармакопее, а пригодность к использованию
Фармакопея не является нормативом на этапе разработки и производства
Только в сети распределения и только в одностороннем плане
Фармакопейный комитет – институт гражданского общества