Слайд 2
Содержание
Хромосомные болезни и синдромы,. Патогенез, патоморфология. Клиника, диагностика,
дифференциальный диагноз. Терапия, реабилитация. Профилактика.
Дауна,
1
Шерешевского-Тернера
2
Клайнфельтера
3
трисомия «Х»
4
синдром Эдвардса
синдром Патау
дубль
«У»
6
7
5
Слайд 3
Трисомия 21 , МКБ. Q90 Синдром Дауна
Этиология.
аномалия хромосом:

лица, страдающие этим расстройством, имеют, как правило, 47 хромосом
вместо нормальных 46. Дополнительная хромосома является результатом нарушенного созревания половых клеток. В норме при делении незрелых половых клеток парные хромосомы расходятся, и каждая зрелая половая клетка получает 23 хромосомы. Во время оплодотворения, т.е. слияния материнской и отцовской клетки, нормальный набор хромосом восстанавливается. В основе синдрома Дауна лежит нерасхождение одной из хромосомных пар, обозначаемой как 21-я. В результате у ребенка появляется лишняя (третья) 21-я хромосома. Это состояние называется трисомией по 21-й паре хромосом. Хотя в подавляющем большинстве случаев при синдроме Дауна обнаруживается именно эта трисомия, крайне редко встречаются и другие хромосомные аномалии.
Частота 1:700-1:800 ● Частота рождения детей с синдромом Дауна зависит от возраста матери и в меньшей мере от возраста отца.
● С возрастом существенно возрастает вероятность рождения детей с синдромом Дауна. Так, в возрасте 45 лет она составляет около 3%. Высокая частота детей с синдромом Дауна (около 2%) наблюдается у рано рожающих женщин (до 18 лет).
Слайд 4
Синдром трисомии 21 (синдром Дауна).
А — внешний вид
больного;
Б — кариотип больного
Слайд 5
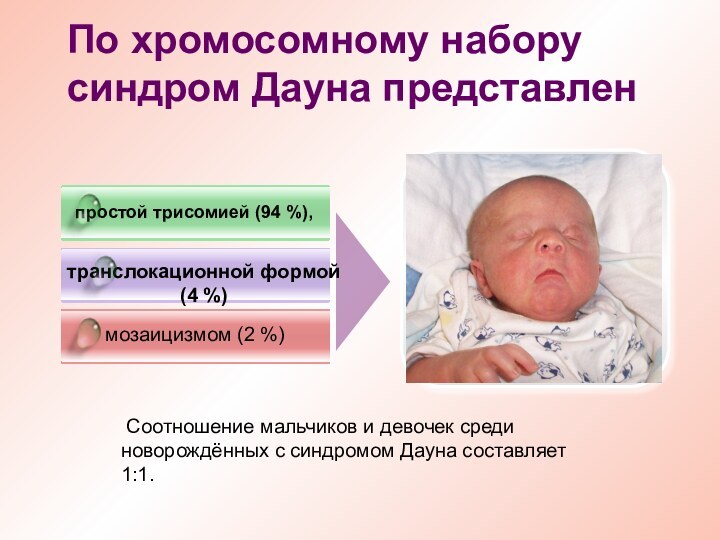
По хромосомному набору синдром Дауна представлен
простой трисомией (94
%),
транслокационной формой (4 %)
мозаицизмом (2 %)
Title in here
ThemeGallery
is a Design Digital Content & Contents mall developed by Guild Design Inc.
1. Description of the contents
2. Description of the contents
3. Description of the contents
Соотношение мальчиков и девочек среди новорождённых с синдромом Дауна составляет 1:1.
Слайд 6
Клиническая симптоматика
Дети с синдромом Дауна рождаются в срок,
но с умеренно выраженной пренатальной гипоплазией (на 8-10% ниже
средних величин). Многие симптомы синдрома Дауна заметны при рождении, в последующем они проявляются более чётко.
Из черепно-лицевых дизморфий отмечаются монголоидный разрез глаз (по этой причине синдром Дауна долго называли монголоидизмом), круглое уплощённое лицо, плоская спинка носа, эпикант, крупный (обычно высунутый) язык, брахицефалия, деформированные ушные раковины.
Характерна мышечная гипотония в сочетании с разболтанностью суставов.
Часто встречаются врождённый порок сердца, клинодактия. характерные изменения дерматоглифики (четырёхпальцевая, или «обезьянья», складка на ладони, две кожные складки вместо трех на мизинце, высокое положение трирадиуса и др.).
Пороки ЖКТ наблюдаются редко. Частота какого-либо симптома в 100% случаев, кроме низкого роста, не отмечена.
Слайд 8
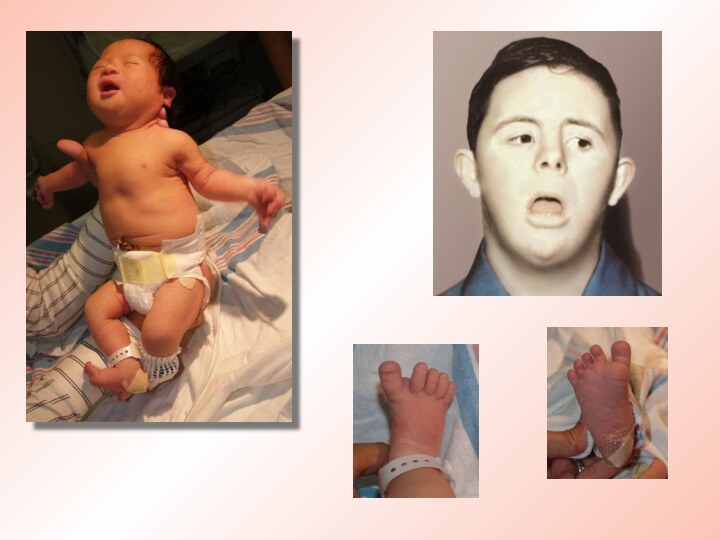
Внешний вид пациентов:
1
2
3
масса новорожденных в среднем составляет 3,2 кг
короткая шея.
голова округлой формы, затылок уплощенный;лоб узкий, лицо широкое
и плоское; запавшая спинка носа;
косой разрез глаз, вертикальные кожные складки, прикрывающие медиальный угол глазной щели;светлые пятна на радужке, катаракта у более старших детей;
4
недоразвитая верхняя челюсть, высокое небо, неправильный рост зубов, толстые губы, утолщенный язык с глубокими бороздами, выступающий изо рта;маленькие, округлой формы, низко расположенные ушные раковины со свисающим завитком;
Слайд 9
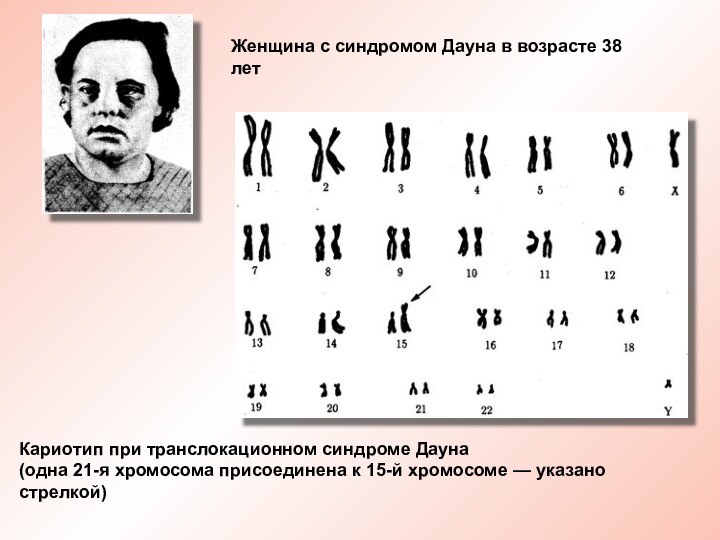
Кариотип при транслокационном синдроме Дауна
(одна 21-я хромосома присоединена
к 15-й хромосоме — указано стрелкой)
Женщина с синдромом Дауна
в возрасте 38 лет
Слайд 10
Пороки внутренних органов:
наиболее типичны пороки сердца: дефекты межжелудочковой
или межпредсердной перегородок, чрезмерное разрастание или нарушение роста эластических
волокон соединительной ткани и др.;
распространены дефекты органов пищеварения: заращение естественных каналов двенадцатиперстной кишки, болезнь Гиршпрунга и др.;
часто встречается лейкемия; также довольна часто снижается функция щитовидной железы;
у маленьких детей резко выражена мышечная гипотония.
1
2
3
4
Слайд 11
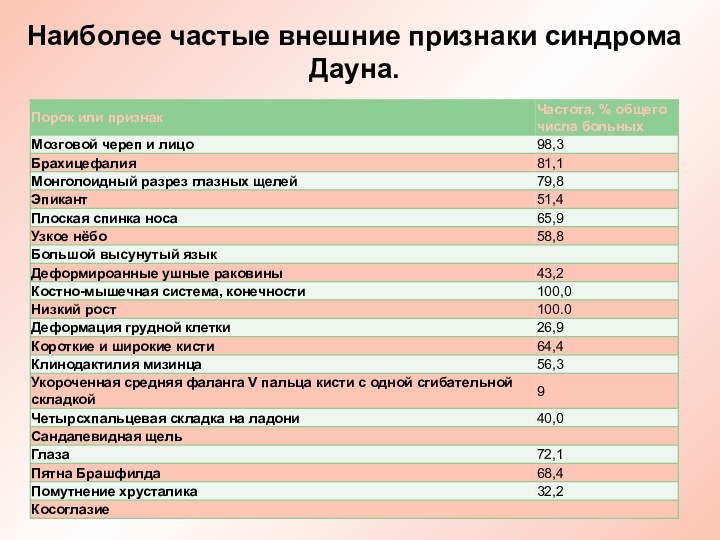
Наиболее частые внешние признаки синдрома Дауна.
Слайд 12
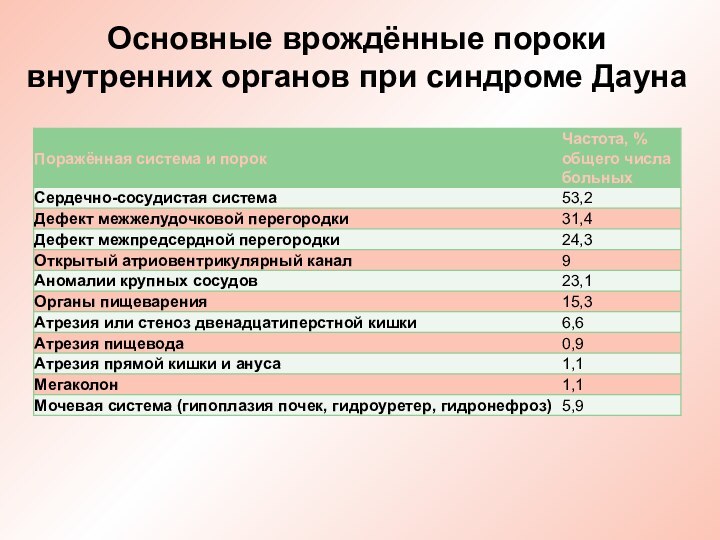
Основные врождённые пороки внутренних органов при синдроме Дауна
Слайд 13
Врождённые пороки внутренних органов, сниженная приспособленность детей с

синдромом Дауна часто приводят к летальному исходу в первые
5 лет. Следствием изменённого иммунитета и недостаточности репарационных систем (для повреждённой ДНК) являются лейкозы, часто встречающиеся у больных с синдромом Дауна. Средняя продолжительность жизни при синдроме Дауна 36 лет.
Большое значение для диагностики имеет динамика физического и умственного развития ребёнка. При синдроме Дауна и то и другое задерживается. Рост взрослых больных на 20 см ниже среднего. Задержка в умственном развитии достигает имбецильности, если не применяются специальные методы обучения. Дети с синдромом Дауна ласковые, внимательные, послушные, терпеливые при обучении. Коэффициент умственного развития (IQ) у разных детей широко варьирует (от 25 до 75).
Реакция детей с синдромом Дауна на факторы окружающей среды часто патологическая в связи со слабым клеточным и гуморальным иммунитетом, снижением репарации ДНК, недостаточной выработкой пищеварительных ферментов, ограниченными компенсаторными возможностями всех систем. По этой причине дети с синдромом Дауна часто болеют пневмониями, тяжело переносят детские инфекции. У них отмечается недостаток массы тела, выражен авитаминоз.
Слайд 14
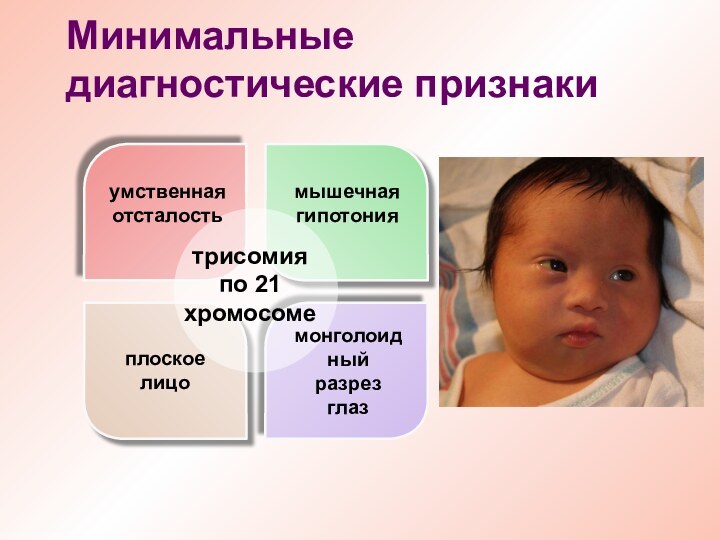
Минимальные диагностические признаки
умственная отсталость
мышечная гипотония
плоское лицо
монголоидный разрез глаз
трисомия
по 21 хромосоме
Слайд 15
Диагностика :
В периоде внутриутробного развития синдрома Дауна может

быть выявлен при проведении биохимического скрининга беременных во II-м
триместре по резкому снижению в сыворотке крови уровня хорионического гонадотропина, что является косвенным признаком наличия синдрома Дауна у плода. В этом случае беременная женщина должна быть направлена на ультразвуковое сканирование 2-го уровня, так как при данной патологии почти в 100% наблюдений выявляются УЗИ-маркеры хромосомных синдромов. Для подтверждения диагноза синдрома Дауна и дальнейшего медико-генетического прогнозирования состояния здоровья будущего потомства родителей показано пренатальное кариотипирование плода.
Дифференциальная диагностика проводится с врождённым гипотиреозом, другими формами хромосомных аномалий. Цитогенетическое исследование у детей показано и при подозрении на синдром Дауна, и при клинически установленном диагнозе, поскольку цитогенетическая характеристика пациента необходима для прогноза здоровья будущих детей у родителей и их родственников.
Лечение. Предпринимались попытки лечить детей с синдромом Дауна гормонами щитовидной железы и гипофиза, однако эти методы находятся пока на стадии разработки. Как и другие умственно отсталые дети их уровня, больные с синдромом Дауна поддаются обучению бытовым навыкам, координации движений, речи и другим простым функциям, необходимым в повседневной жизни.
Слайд 16
На ладони часто обнаруживают поперечную складку
Болезнь Дауна
Кариотип больного
Слайд 17
Шерешевского — Тернера синдром (Н.А. Шерешевский, сов. эндокринолог, 1885—1961; Н.Н. Turner,
амер. эндокринолог, родился в 1892 г.; синоним: синдром Тернера, синдром
Ульриха, сексогенная карликовость и др.)
генетически обусловленная форма первичной агенезии или дисгенезии гонад, относится к хромосомным болезням, сопровождается аномалиями соматического развития и низкорослостью.
Частота Ш.-Т. с. среди новорожденных составляет в среднем 0,03%
Слайд 19
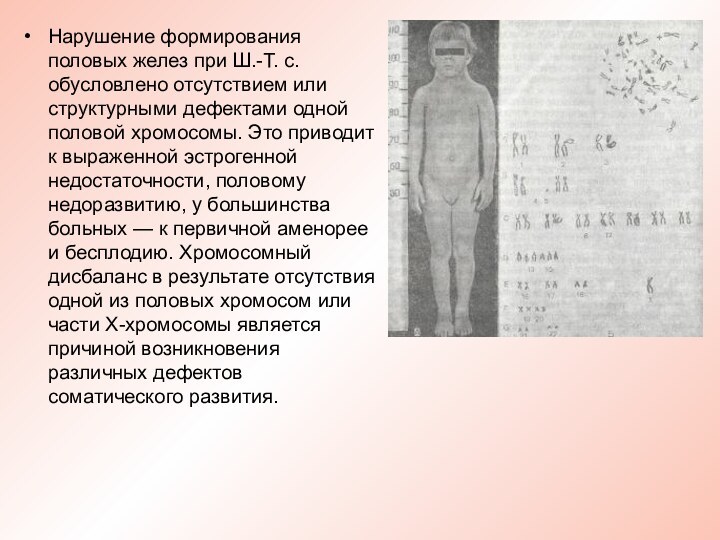
Нарушение формирования половых желез при Ш.-Т. с. обусловлено
отсутствием или структурными дефектами одной половой хромосомы. Это приводит
к выраженной эстрогенной недостаточности, половому недоразвитию, у большинства больных — к первичной аменорее и бесплодию. Хромосомный дисбаланс в результате отсутствия одной из половых хромосом или части Х-хромосомы является причиной возникновения различных дефектов соматического развития.
Слайд 20
Гонады при Ш.-Т. с. представляют собой недифференцированные соединительнотканные
тяжи. Реже встречаются рудименты яичников, включающие овариальную строму, а
иногда и отдельные примордиальные фолликулы. В гонадных тяжах могут быть обнаружены элементы яичек и рудименты семявыносящего протока. Наиболее важны изменения костно-суставной системы — spina bifida, деформация суставов, укорочение метакарпальных и метатарзальных костей, фаланг, остеопороз и др., изменения сердца и крупных сосудов — коарктация аорты, незаращение аортального (боталлова) протока, дефект межжелудочковой перегородки, стеноз устья аорты, почечных артерий и др., пороки развития почек — подковообразная почка, удвоение лоханок и мочеточников и др.
Слайд 21
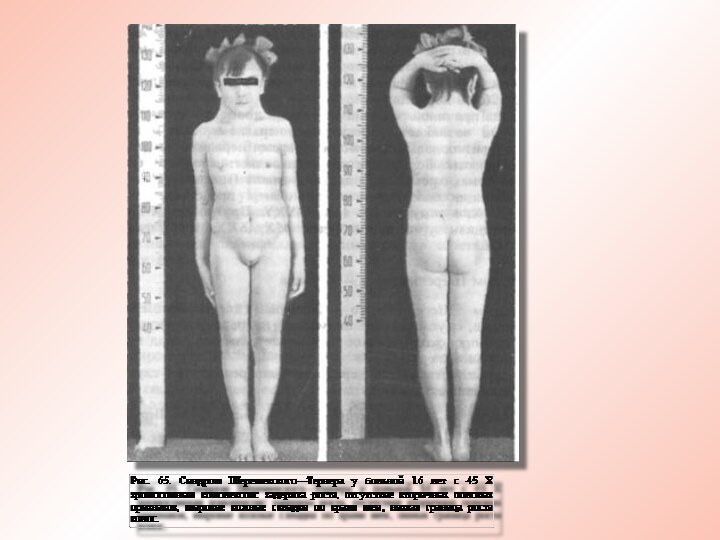
Отставание больных с Ш.-Т. с. в физическом развитии
заметно уже с рождения. Для доношенных новорожденных характерны малая
длина (42—48 см) и масса тела 2800—2500 г и менее), т.е. задержка физического развития носит внутриутробный характер. Это послужило причиной причисления Ш.-Т. с к примордиальному нанизму Патогномоничными для Ш.-Т. с. при рождении являются складки кожи по бокам укороченной шеи (птеригиум-синдром), другие пороки соматического развития, особенно костно-суставной и сердечно-сосудистой систем, так называемое лицо сфинкса, лимфостаз.
Для течения постнатального периода характерно общее беспокойство новорожденных, нарушение сосательного рефлекса, срыгивания фонтаном, рвота. В раннем возрасте у части больных отмечают задержку статического развития и развития речи, что свидетельствует о патологии эмбриогенеза нервной системы. Примерно у 15—20% больных задержка развития наблюдается в пубертатном периоде.
Слайд 22
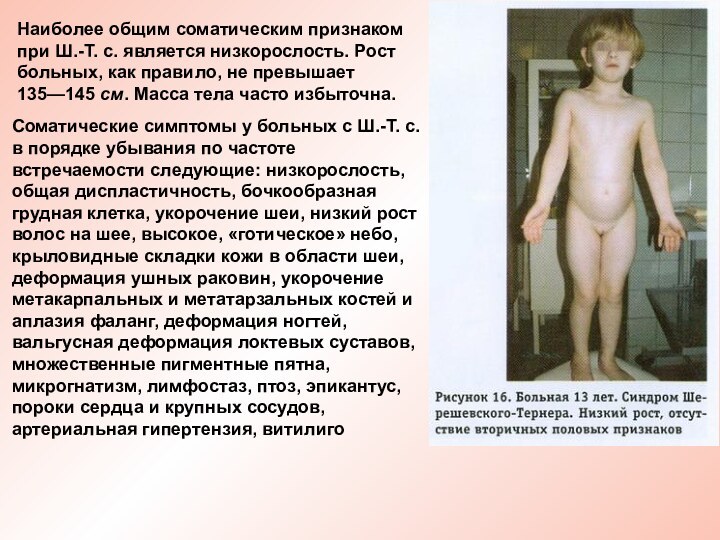
Соматические симптомы у больных с Ш.-Т. с. в
порядке убывания по частоте встречаемости следующие: низкорослость, общая диспластичность,
бочкообразная грудная клетка, укорочение шеи, низкий рост волос на шее, высокое, «готическое» небо, крыловидные складки кожи в области шеи, деформация ушных раковин, укорочение метакарпальных и метатарзальных костей и аплазия фаланг, деформация ногтей, вальгусная деформация локтевых суставов, множественные пигментные пятна, микрогнатизм, лимфостаз, птоз, эпикантус, пороки сердца и крупных сосудов, артериальная гипертензия, витилиго
Наиболее общим соматическим признаком при Ш.-Т. с. является низкорослость. Рост больных, как правило, не превышает 135—145 см. Масса тела часто избыточна.
Слайд 23
Клинические симптомы синдрома Шерешевского-Тёрнера и их частота
Слайд 24
На рентгенограммах кистей и стоп встречаются аплазия фаланг,
гипоплазия метакарпальных и метатарзальных костей, деформация костей лучезапястного сустава,
на рентгенограммах позвоночника и грудной клетки — синостозы позвонков и ребер, явления гипертрофического остеопороза. Дифференцировка скелета умеренно отстает от возрастных норм, однако к пубертатному периоду она прогрессирует и обычно соответствует фактическому возрасту.
Рентгенологически при Ш.-Т. с. турецкое седло и кости свода черепа обычно не изменены, лишь в отдельных случаях турецкое седло может иметь своеобразную форму с обызвествлением диафрагмы, быть уменьшенным или увеличенным.
Слайд 25
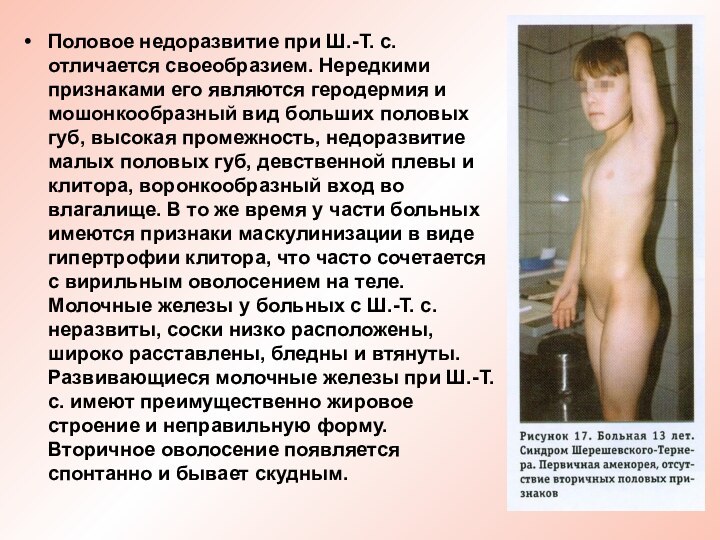
Половое недоразвитие при Ш.-Т. с. отличается своеобразием. Нередкими
признаками его являются геродермия и мошонкообразный вид больших половых
губ, высокая промежность, недоразвитие малых половых губ, девственной плевы и клитора, воронкообразный вход во влагалище. В то же время у части больных имеются признаки маскулинизации в виде гипертрофии клитора, что часто сочетается с вирильным оволосением на теле. Молочные железы у больных с Ш.-Т. с. неразвиты, соски низко расположены, широко расставлены, бледны и втянуты. Развивающиеся молочные железы при Ш.-Т. с. имеют преимущественно жировое строение и неправильную форму. Вторичное оволосение появляется спонтанно и бывает скудным.
Слайд 26
В отличие от гипофизарного нанизма при Ш.-Т. с.
наблюдают высокую гипоталамо-гипофизарную активность, что проявляется изменениями по типу
поствакцинального синдрома, выражается в склонности к повышению АД у лиц молодого возраста и к ожирению с нарушениями трофики тканей, в характерных изменениях ЭЭГ
Интеллект большинства больных с Ш.-Т. с. сохранен, имеющаяся иногда интеллектуальная недостаточность выражена нерезко. В психическом статусе больных с Ш-Т. с. главную роль играет своеобразный психический инфантилизм с эйфорией при хорошей практической приспособляемости и социальной адаптации.
Диагноз устанавливают на основании характерных клинических особенностей, определения полового хроматина и исследования кариотипа. Для дифференциальной диагностики с нанизмом информативными являются данные определения содержания в крови тронных гормонов гипофиза, особенно гонадотропинов, и электроэнцефалографии.
Слайд 27
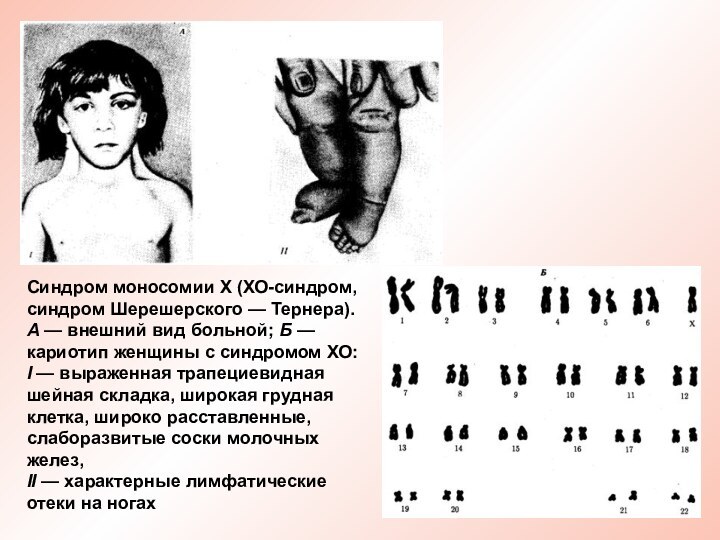
Синдром моносомии Х (ХО-синдром, синдром Шерешерского — Тернера).
А — внешний вид больной; Б — кариотип женщины
с синдромом ХО:
I — выраженная трапециевидная шейная складка, широкая грудная клетка, широко расставленные, слаборазвитые соски молочных желез,
II — характерные лимфатические отеки на ногах
Слайд 28
Лечение больных с Ш.-Т. с. заключается в стимуляции

роста тела анаболическими стероиидами и другими анаболическими препаратами. Учитывая
большую склонность больных к андрогенизации, лечение следует проводить минимально эффективными дозами анаболических стероидов с перерывами при регулярном гинекологическом контроле. Основным видом терапии больных с Ш.-Т. с. является эстрогенизация, которую осуществляют с 14—16 лет и в течение всего детородного возраста: вначале непрерывно до появления первого менструальноподобного кровотечения, далее — курсами, имитируя нормальный менструальный цикл. Лечение приводит к феминизации телосложения, развитию женских вторичных половых признаков, улучшает трофику половых путей, вызывает индуцированные менструации, уменьшает повышенную активность гипоталамо-гипофизарной системы, предотвращает развитие гипоталамической патологии по типу посткастрационного синдрома. При Ш.-Т. с. у мужчин в случае гипогонадизма применяется заместительная терапия мужскими половыми гормонами.
Слайд 29
Прогноз для жизни при Ш.-Т. с. благоприятный, исключение
составляют больные с тяжелыми врожденными пороками сердца и крупных
сосудов, с ренальной гипертензией. Лечение эстрогенами делает больных с Ш.-Т. с. способными к семейной жизни, однако абсолютное большинство из них остаются бесплодными.
Слайд 30
Синдром Клайнфельтера
Наследственное заболевание характеризующееся полисомией по половым хромосомам.
Классический хромосомный набор при синдроме Клайнфельтера имеет следующий вид:
47 ХХY. Возможно и большее количество Х-хромосом, но такие варианты синдрома Клайнфельтера встречаются весьма нечасто. Обязательным условием заболевания является наличие Y-хромосомы, что и определяет возникновение синдрома Клайнфельтера только у лиц мужского пола.
Частота встречаемости: около 1:700 новорожденных мальчиков. Такое изменение хромосомного набора связано с нарушением процессов клеточного деления в эмбриональном периоде. Y-хромосома обуславливает развитие мужских первичных половых признаков, однако избыток Х-хромосом подавляет ее влияние.
Слайд 32
Клиника синдрома Клайнфельтера
Заболевание до периода полового созревания практически

не проявляется. Мальчики растут и развиваются нормально, однако иногда
может обращать на себя внимание задержка психического и умственного развития (дебильность). В пубертатном периоде начинают проявляться присущие для синдрома Клайнфельтера черты: происходит недоразвитие яичек и вторичных половых признаков. Характерен внешний вид больных: высокий рост, евнухоидный тип телосложения (узкие плечи, относительно широкий таз, оволосение по женскому типу). Также происходят дегенеративные процессы в яичках и семенных канальцах. Сперматозоиды функционально несостоятельны, а позже перестают вырабатываться совсем, что обуславливает наступление стерильности. Молочные железы увеличиваются, но процесса лактации не происходит, так как толщу желез выполняет соединительная ткань – развивается гинекомастия. Волосяной покров и мышечная масса выражены слабо. Больные с синдромом Клайнфельтера малопригодны для физического и умственного труда. Задержка психического развития все четче проявляется с возрастом, доходя порой до имбецильности. Больным с синдромом Клайнфельтера присущи поведенческие отклонения: лабильность психики, агрессивность, которые чередуются с безразличием ко всему окружающему. Данные клинические проявления всегда имеются у лиц с набором ХХХY, ХХХХY. У больных с двумя Х-хромосомами ряда перечисленных клинических признаков может и не быть.
Слайд 33
Синдром Клайнфельтера. А —внешний вид больного (характерен высокий
рост, непропорционально длинные конечности); Б—кариотип больного (XXY)
Слайд 34
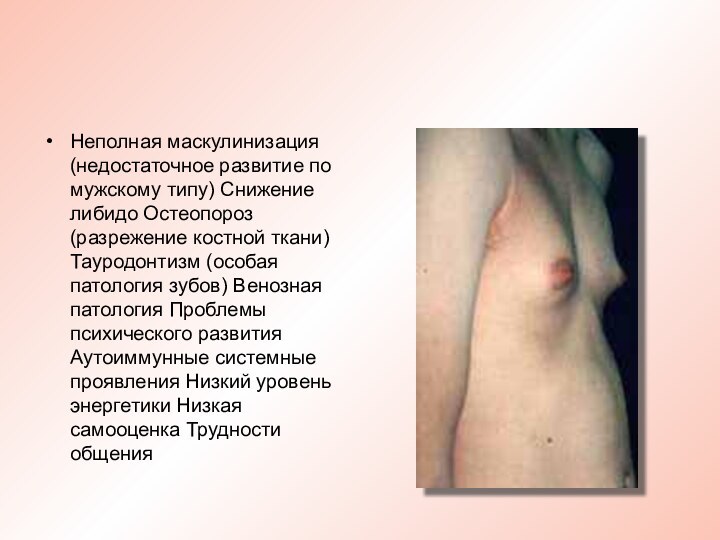
Неполная маскулинизация (недостаточное развитие по мужскому типу) Снижение
либидо Остеопороз (разрежение костной ткани) Тауродонтизм (особая патология зубов)
Венозная патология Проблемы психического развития Аутоиммунные системные проявления Низкий уровень энергетики Низкая самооценка Трудности общения
Слайд 35
Диагностика и лечение синдрома Клайнфельтера
Диагностика синдрома Клайнфельтера несложна.

Распознать заболевание можно даже по внешнему виду больных и
по изменениям со стороны вторичных половых признаков. Евнухоидный тип телосложения обусловлен циркуляцией в крови повышенной концентрации фолликулостимулирующего гормона, являющегося неотъемлемой частью гормональной регуляции менструальной функции женского организма. Кроме того, в биохимическом анализе крови часто отмечается абсолютный дефицит андростерона и тестостерона. Поэтому данные изменения являются крайне ценными в диагностике синдрома Клайнфельтера. Поскольку заболевание в детском возрасте практически никак себя не проявляет, вовремя выявить больных удается очень редко, что, в свою очередь, делает весьма сомнительным прогноз лечения. Наиболее эффективным способом свести к минимуму проявления синдрома Клайнфельтера является курсовая гормональная терапия в виде инъекций метилтестостерона - синтетического аналога тестостерона. Наиболее видимые результаты от такого лечения достигаются, если синдром Клайнфельтера был выявлен в возрасте до 10 лет.
Слайд 37
Трисомия Х
Частота трисомии-Х составляет среди новорожденных девочек и

женщин 1:1000, среди умственно отсталых — 0,59 %. Большинство
девочек и женщин с трисомией-Х выявлены среди больных психиатрических больниц.
Трисомию-Х иногда называют синдромом трипло-Х, однако это не является обоснованным: трисомия-Х не обусловливает четкого постоянного симптомокомплекса.
Клинические проявления весьма полиморфны, а у части пациентов с трисомией-Х вообще не обнаруживается каких-либо отклонений в физическом и психическом развитии. Вместе с тем одним из частых проявлений трисомии-Х является неглубокая умственная отсталость, которая отмечается у 75 % больных. Особое внимание привлекает частота заболевания шизофренией. У многих больных с трисомией-Х наблюдаются задержка физического развития, негрубые диспластические признаки: эпикант, высокое твердое небо, клинодактилия мизинцев. Реже встречаются больные высокого роста. У некоторых пациентов отмечается бесплодие, обусловленное недоразвитием фолликулов.
Диагноз ставят только при цитогенетическом исследовании: выявляют 47 хромосом и двойной половой хроматин. Описано также много случаев так называемой полисомии-Х: тетрасомия (ХХХХ) и пентасомия (ХХХХХ) с соответствующим увеличением количества телец полового хроматина. В этих случаях степень психического недоразвития выражена грубее и коррелирует с количеством дополнительных Х-хромосом.
Слайд 38
Синдром Э́двардса (синдром трисомии 18)
характеризуется комплексом множественных пороков
развития и трисомией 18 хромосомы. (трисомия 18; 47, XX(XY)+18
)
МКБ-10: Q91.0 Трисомия 18, мейотическое нерасхождение
Q91.1 Трисомия 18, мозаицизм (митотическое нерасхождение)
Q91.2 Трисомия 18, транслокация
Q91.3 Синдром Эдвардса неуточненный
Вариации
Кроме трисомии 18, присутствующей во всех клетках организма, а также мозаичной трисомии 18, возможна и частичная трисомия. При этом часть хромосомы 18 присоединяется к другой хромосоме. Такой эффект называется транслокация, и он может произойти как при созревании гамет, так и после оплодотворения в клетках зародыша. В клетках организма при этом оказываются две гомологичные хромосомы 18 и, дополнительно, часть хромосомы 18, прикрепленная к другой хромосоме. У людей, страдающих частичной трисомией 18, аномалии проявляются слабее, нежели при типичном синдроме Эдвардса.
Слайд 39
Этиология.
Причиной заболевания является наличие дополнительной 18-й хромосомы (трех
вместо двух).
В одном случае из десяти наблюдается мозаицизм в
явлении трисомии 18: лишнюю хромосому несут не все клетки организма. Это говорит о том, что нерасхождение произошло на ранней стадии развития зародыша, а все клетки с трисомией — потомки неправильно поделившейся клетки зародыша.
Дети с трисомией 18 чаще рождаются у пожилых матерей, взаимосвязь с возрастом матери менее выражена, чем в случаях трисомии хромосомы 21 и 13. Для женщин старше 45 лет риск родить больного ребенка составляет 0,7 %.
Слайд 40
Основные клинические проявления синдрома Эдвардса. Внешний вид:
дети рождаются

со средним весом 2, 2 кг, хотя сроки беременности
нормальные или даже превышают норму;
в процессе развития организма наиболее часты аномалии мозгового и лицевого черепа, мозговой череп чрезмерно длинной формы;
нижняя челюсть и ротовое отверстие маленькие;
глазные щели узкие и короткие;
ушные раковины деформированы и в подавляющем большинстве случаев расположены низко, несколько вытянуты в горизонтальной плоскости, мочка, а часто и козелок отсутствуют;
наружный слуховой проход сужен, иногда отсутствует;
грудина короткая, из-за чего межреберные промежутки уменьшены и грудная клетка шире и короче нормальной;
в 80 % случаев наблюдается аномальное развитие стопы: пятка резко выступает, свод провисает (стопа-качалка), большой палец утолщен и укорочен.
Дефекты внутренних органов:
наиболее часты пороки сердца и крупных сосудов: дефект межжелудочковой перегородки, врожденное отсутствие одной створки клапанов аорты и легочной артерии;
недоразвитие мозжечка и мозолистого тела, изменения структур олив;
выраженная умственная отсталость;
снижение мышечного тонуса, переходящее в повышение со спастикой.
Слайд 42
Это болезнь характеризуется недоразвитием многих органов и систем,

а также многочисленными пороками внутриутробного развития. Наиболее часто патология
встречается со стороны опорно-двигательного аппарата, половых органов, строения костей черепа, сердечно-сосудистой системы, а также пищеварительной системы.
Нарушения опорно-двигательного аппарата проявляются неправильным развитием первого пальца кисти, а первый палец стопы короткий и широкий, за счет чего второй палец стопы кажется длиннее. Выявляется неправильное анатомическое строение стопы, косолапость, пятка выступает, а свод стопы провисает. Пальцы на стопе и на кистях могут быть сращены за счет кожных складок.
При внешнем осмотре обращает на себя внимание короткая грудная клетка.
Изменения со стороны мочеполовой сферы проявляются пузырьками с жидкостью в почках, сращением, удвоением почек и/или мочеточников, увеличением клитора у девочек, неопущением яичек в мошонку у мальчиков.
Изменения со стороны мозгового и лицевого черепа проявляются вытянутой формой черепа, ушные раковины низко посажены и деформированы, маленькая нижняя челюсть, высокое небо, в 5-7% случаев выявляется расщелина неба. Нарушается нормальное развитие основных мозговых структур, за счет чего появляется неврологическая симптоматика.
Со стороны органов пищеварения может встречаться заращение просвета пищевода, заращение выводных протоков желчного пузыря и желчных ходов, грыжеподобные выпячивания кишечника, может быть незавершенный поворот петель кишечника, аномальное расположение ткани поджелу дочной железы.
Слайд 43
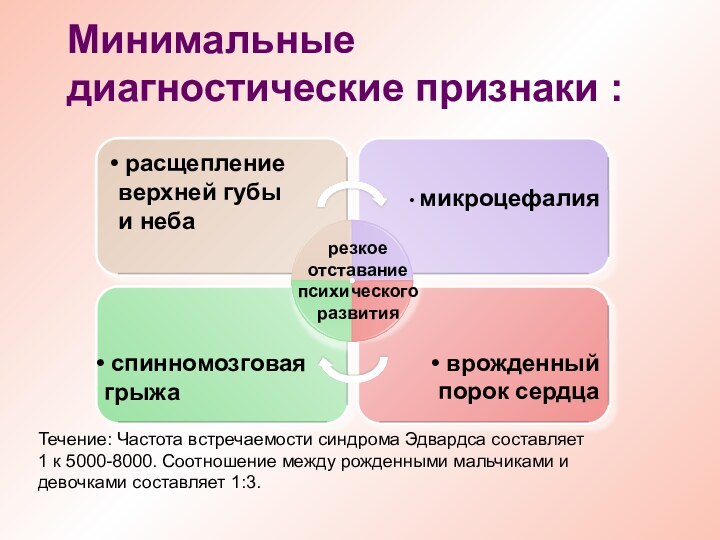
Минимальные диагностические признаки :
расщепление верхней губы и
неба
спинномозговая грыжа
микроцефалия
врожденный порок сердца
Течение: Частота встречаемости
синдрома Эдвардса составляет 1 к 5000-8000. Соотношение между рожденными мальчиками и девочками составляет 1:3.
резкое отставание психического развития
Слайд 44
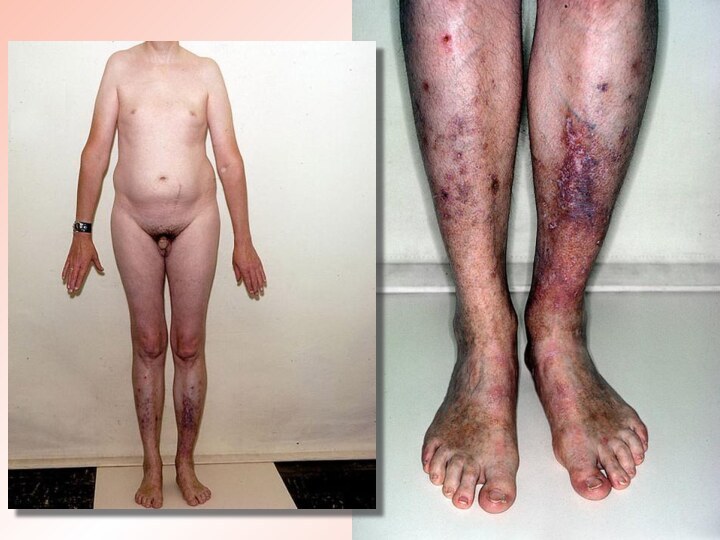
Синдром трисомии 18 (синдром Эдвардса). А — внешний
вид больного; Б — кариотип больного при трисомии в
группе Е:
I — черепно-лицевые аномалии, II — характерное расположение пальцев на кистях больного
Слайд 45
Прогноз: Продолжительность жизни детей с синдромом Эдвардса невелика:
60 % детей умирают в возрасте до 3 мес, до
года доживает лишь 5-10 %. Основной причиной смерти служат остановка дыхания и нарушения работы сердца. Оставшиеся в живых — глубокие олигофрены.
Диагностика : В периоде внутриутробного развития синдрома Эдвардса может быть выявлен при проведении биохимического скрининга беременных во II-м триместре по резкому снижению в сыворотке крови уровня хорионического гонадотропина, что является косвенным признаком наличия синдрома Эдвардса у плода. В этом случае беременная женщина должна быть направлена на ультразвуковое сканирование 2-го уровня, так как при данной патологии почти в 100% наблюдений выявляются УЗИ-маркеры хромосомных синдромов.
Слайд 46
Для подтверждения диагноза синдрома Эдвардса и дальнейшего медико-генетического
прогнозирования состояния здоровья будущего потомства родителей показано пренатальное кариотипирование
плода.
Для своевременной диагностики заболевания применяется цитогенетическое исследование.
Дифференциальная диагностика проводится с врождённым гипотиреозом, другими формами хромосомных аномалий. Цитогенетическое исследование у детей показано и при подозрении на синдром Дауна, и при клинически установленном диагнозе, поскольку цитогенетическая характеристика пациента необходима для прогноза здоровья будущих детей у родителей и их родственников.
Слайд 47
Синдром Патау
Частота синдрома Патау среди новорождённых равна 1:5000-1:7000.
Соотношение полов при близко к 1:1.
Цитогенетические варианты этого
синдрома следующие. Простая полная трисомия 13 как следствие нерасхождения хромосом в мейозе у одного из родителей (главным образом у матери) встречается у 80-85% больных. Остальные случаи обусловлены в основном передачей дополнительной хромосомы (точнее, её длинного плеча) в робертсоновских транслокациях типа D/13 и G/13.
Слайд 48
Синдром трисомии 13 (синдром Патау).
А — внешний вид
больного; Б — кариотип больного с трисомией в группе
D:
I — аномалии лица, II — двусторонняя полисиндактилия стоп
Слайд 49
Дети с синдромом Патау рождаются с истинной пренатальной
гипоплазией (на 25-30% ниже средних величин), которую нельзя объяснить
небольшой недоношенностью (средний срок гестации 38,3 нед). Характерное осложнение беременности при вынашивании плода с синдромом Патау - многоводие: оно встречается почти в 50% случаев синдрома Патау.
Слайд 50
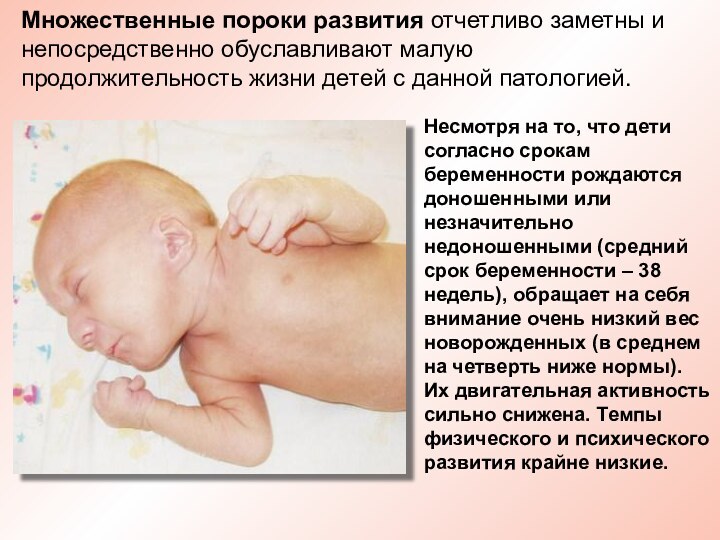
Множественные пороки развития отчетливо заметны и непосредственно обуславливают
малую продолжительность жизни детей с данной патологией.
Несмотря на
то, что дети согласно срокам беременности рождаются доношенными или незначительно недоношенными (средний срок беременности – 38 недель), обращает на себя внимание очень низкий вес новорожденных (в среднем на четверть ниже нормы). Их двигательная активность сильно снижена. Темпы физического и психического развития крайне низкие.
Слайд 51
Внешние аномалии развития многочисленны и патогномоничны для синдрома
Патау. У ребенка малые размеры черепа, который, к тому
же, имеет неправильную форму (башенный череп либо треугольный с верхушкой, обращенной кверху); глазные яблоки уменьшены (иногда и вовсе отсутствуют), глазная щель узкая, лоб скошен. Обращают на себя внимание низко расположенные и деформированные ушные раковины, запавшая переносица. Однако наиболее облигатным признаком синдрома Патау является двусторонняя расщелина неба и верхней губы в сочетании с полидактилией обычно только на руках (могут быть варианты полидактилии на руках и ногах одновременно).
Слайд 52
Аномалии внутренних органов при синдроме Патау тяжелые и
многочисленные. Врожденные пороки сердца представлены в основном дефектами межжелудочковой
перегородки различной величины.
Кишечник во время внутриутробного развития при синдроме Патау не до конца завершает свой поворот, ткань поджелудочной железы гипоплазирована. Почки – с признаками поликистоза, половые органы недоразвиты.
Слайд 54
В связи с тяжёлыми врождёнными пороками развития большинство
детей с синдромом Патау умирают в первые недели или
месяцы (95% - до 1 года). Однако некоторые больные живут несколько лет. Более того, в развитых странах отмечается тенденция увеличения продолжительности жизни больных с синдромом Патау до 5 лет (около 15% детей) и даже до 10 лет (2-3% детей).
Диагностика и своевременное обнаружение синдрома Патау во время беременности во многом облегчилась благодаря скрининговому ультразвуковому исследованию беременных. Наиболее важный признак, позволяющий заподозрить данную патологию, - многоводие. Почти у половины женщин с многоводием во время беременности рождаются дети с различными аномалиями развития, в том числе с синдромом Патау. Клиническая диагностика основывается на данных осмотра новорожденного. Обычно правильный диагноз в этом случае поставить несложно.
Слайд 56
Другие синдромы врождённых пороков развития (синдромы Меккеля и
Мора, тригоноцефалия Опитца) по отдельным признакам совпадают с синдромом
Патау. Решающий фактор в диагностике - исследование хромосом. Цитогенетическое исследование показано во всех случаях, в том числе у умерших детей. Точный цитогенетический диагноз необходим для прогноза здоровья будущих детей в семье.
Лечебная помощь детям с синдромом Патау неспецифическая: операции по поводу врождённых пороков развития (по жизненным показаниям), общеукрепляющее лечение, тщательный уход, профилактика простудных и инфекционных болезней. Дети с синдромом Патау практически всегда имеют глубокую идиотию.
Слайд 57
Характеристика наиболее частых трисомий
Слайд 58
Синдром дубль-Y
Синдром XYY характеризуется кариотипом 47, XYY. Он

впервые описан в 1960 г. Частота синдрома по среднестатистическим данным
составляет среди новорожденных около 1:1000. Иногда приводятся значительно более высокие данные— 1:250.
Наиболее частым признаком является высокий рост, который у взрослых больных составляет в среднем 186 см. Однако этот признак не является абсолютным, так как в литературе имеются описания мужчин с кариотипом 47, XYY среднего роста. У части больных отмечаются нерезко выраженные евнухоидные черты телосложения и диспластические признаки: неправильное строение зубов, увеличение нижней челюсти, аномальный прикус, девиация коленных и локтевых суставов, радиоульнарный синостоз. У некоторых больных обнаруживается повышение уровня андрогенов и лютеинизирующего гормона. Половая функция не нарушена. Наличие добавочной Y-хромосомы может и не сопровождаться клинической патологией, но, несомненно, оно коррелирует как с интеллектуальным недоразвитием, так и с эмоционально-волевыми нарушениями.
При цитогенетическом исследовании с помощью люминесцентной микроскопии в буккальных мазках обнаруживается Y-хроматин. При анализе кариотипа выявляется дополнительная Y-хромосома.