Слайд 2
ГЕМОПОЭЗ
Кроветворение – многостадийный процесс дифференцировки клеточных элементов, в
результате которого образуются эритроциты, лейкоциты, тромбоциты, составляющие в норме
около 40% объема крови.
Образование и дифференцировка этих клеток осуществляется в кроветворных органах: костном мозге, тимусе, селезенке и лимфотических узлах, представляющих единую кроветворную систему.
Слайд 3
Эмбриональное кроветворение
В результате дробления оплодотворенной яйцеклетки образуется бластоцита,
затем бластула и гаструла.
Внутренняя клеточная масса бластоциты содержит
30-150 эмбриональных стволовых клеток (ЭСК).
Эти клетки обладают тотипотентностью (способность давать начало всем без исключения клеткам и тканям организма).
Слайд 4
Эмбриональное кроветворение
На стадии гаструлы, в результате сложных
перемещений клеток, образуется 3 зародышевых листка – экто-, мезо-
и эндодерма. Мезодерма (средний зародышевый листок) дает начало костному мозгу, крови и сердечно-сосудистой системе. Мезенхима является производной мезодермы, из нее формируется соединительная ткань организма. Образование органов из ЭСК, включая гемопоэтические – костный мозг, тимус, селезенку, лимфатические узлы, лимфоидную ткань, ассоциированную со слизистыми оболочками, - осуществляется благодаря функционированию генов, реализующих генетическую программу в клетке.
Слайд 5
Эмбриональное кроветворение
Закладка кроветворной системы осуществляется при взаимодействии трех
клеточных пулов - производных мезодермы –
гемопоэтического,
стромального
сосудистого
Слайд 6
4 критических периода становления гемопоэза
I период -
возникновение первых кроветворных клеток-предшественников в желточном мешке эмбриона (внеэмбриональное
кроветворение) - 4-5-я неделя развития плода;
II период - заселение печени плода кроветворными клетками-предшественниками и начало внутриэмбрионального печеночного кроветворения (5-я неделя внутриутробного развития);
III период - проникновение ранних Т-лимфоцитов в тимус и формирование Т-клеточной иммунной системы (9-10-я неделя);
IV период - смена печеночного кроветворения на костномозговое (15-18-я неделя).
Слайд 7
1 период становления гемопоэза
зарождение кроветворных клеток во внеэмбриональной
мезенхиме
становление начального гемопоэза в желточном мешке, хорионе в
виде кровяных островков, окруженных клетками эндотелия. Эндотелиальные клетки, сливаясь в капилляры, соединяют желточный мешок с эмбрионом.
формирование сосудистой сети,
создаются возможности для миграции примитивных кроветворных клеток в печень и в тимус ( к 4-5-й неделе развития эмбриона)
Слайд 8
1 период становления гемопоэза
в желточном мешке (4-5 нед.
развития эмбриона)
образуются бласты, примитивные эритробласты-мегалобласты, синтезирующие “примитивный” тип
гемоглобина - HbP.
возникают полипотентные клетки-предшественники гранулоцито-эритро-моноцито- мегакариоцитопоэза, образующие смешанные колонии
в составе этих клеток - КОЕ-ГЭММ (колониеобразующие единицы гранулоцито-эритро-моноцито-мегакариоцитопоэза), экспрессирующие рецепторы стволовых клеток CD34 (CD - кластер дифференцировки).
Слайд 9
1 период становления гемопоэза
в желточном мешке (4-5-я неделя
развития эмбриона)
появляются бипотентные грануломоноцитарные клетки-предшественники - КОЕ-ГМ.
обнаруживаются
эритроидные клетки-предшественники - бурстобразующие единицы эритропоэза (БОЕ-Э) и колониеобразующие единицы эритропоэза (КОЕ-Э), способные образовывать крупные эритроидные колонии из нескольких агрегатов - бурсты
Активный гемопоэз в желточном мешке полностью заканчивается к 10-12-й неделе.
Слайд 10
II критический период эмбрионального гемопоэза
формирование печеночного кроветворения.
Печень
- центральный орган гемопоэза с 5-й по 22-ю неделю
внутриутробного развития плода.
Печеночная ткань представлена гепатоцитами - производными эндодермы и кроветворными клетками - производными мезодермы.
К 30-му дню в эмбриональной печени - первые гемопоэтические клетки, несущие маркер ранних клеток-предшественников - CD34. Гемопоэз преимущественно эритроидный, изменение морфологии эритробластов сопровождается сменой типов гемоглобина.
Слайд 11
II критический период эмбрионального гемопоэза
С 7-й недели до
конца 3-го месяца эритробласты печени синтезируют фетальный гемоглобин (HbP),
одновременно продолжает существовать и примитивный эритропоэз. Печень в этот период является органом преимущественного синтеза гемоглобина.
7-8 неделя - в печени осуществляется гранулоцитопоэз, моноцитопоэз, мегакариоцитопоэз
К 9-й неделе в печени плода - В-лимфопоэз.
8-9 и 16-22-я недели - наибольшая интенсивность пролиферативной активности в печени, свидетельствующая о том, что процесс миграции стволовых клеток из печени в костный мозг имеет пролонгированный характер.
Кроветворение в небольшом объеме в печени остается до 7-го месяца
Слайд 12
III критический период гемопоэза
Формирование Т-клеточной иммунной системы
Тимус,
селезенка и кости с костномозговыми полостями начинают формироваться сразу
после образования печени, не являясь кроветворными.
Тимус закладывается на 6-й неделе развития плода, его заселение лимфоидными клетками-предшественниками происходит после 8-й недели. Начинается активный лимфопоэз.
К концу 3-го месяца тимическая ткань разделена на кору, богатую мелкими лимфоцитами, и мозговую часть, содержащую лимфоциты на разных стадиях созревания и тимические тельца.
Слайд 13
Селезенка формируется с 5-6-й недели.
На 12-й неделе
в строме селезенки появляются первые островки эритробластов, гранулоцитов.
Образование
белой пульпы с лимфопоэзом начинается с 15-й недели.
Гемопоэз в селезенке достигает своего максимума к 4-му месяцу, а затем идет на убыль и прекращается к 6,5 мес. внутриутробного развития
Эмбриональное кроветворение
Гемопоэз в селезенке
Слайд 14
IV период эмбрионального кроветворения
происходит в костном мозге и
его становление идет параллельно с формированием костей скелета (8-11
недель).
Костный мозг в течение 2 недель не является гемопоэтическим. Образуется его стромальный матрикс. Костные рудименты окружаются сетью капилляров, а также клетками - предшественниками остеобластов и макрофагов.
К 10-й неделе между костными трабекулами образуются большие сосудистые синусы и костномозговые полости.
Слайд 15
IV период эмбрионального кроветворения
С 15-16-й недели костный мозг
становится центральным органом гемопоэза, функционирующим весь период жизни человека.
В костном мозге плода представлены клетки всех ростков кроветворения различной степени зрелости.
Для костномозгового кроветворения, в отличие от печени, характерна миелоидная направленность. Снова меняется тип гемоглобина: до 20-й недели у плода синтезируется в основном фетальный гемоглобин (HbP), с нарастанием синтеза цепей глобина увеличивается образование взрослого типа гемоглобина - НbА.
Слайд 16
Роль лимфатических узлов в гемопоэзе
Первые лимфатические узлы
появляются примерно на 13-14-й неделе развития эмбриона, они в
начале представляют универсальный орган кроветворения.
На 7-м месяце миелопоэз в лимфатических узлах быстро сменяется образованием лимфоцитов.
К моменту рождения ребенка определяется около 220 лимфатических узлов. Однако окончательное формирование синусов и стромы лимфатических узлов происходит в постнатальном периоде.
Слайд 17
Итак, эмбриональное кроветворение
характеризуется последовательной сменой кроветворных органов.
вначале
гемопоэз проходит в желточном мешке,
затем в печени, тимусе,
селезенке, лимфатических узлах и в костном мозге, который после рождения остается единственным органом миелопоэза.
Лимфоциты, имея с миелоидными клетками единую стволовую кроветворную клетку, пройдя определенные стадии дифференцировки в костном мозге и тимусе, в последующем развиваются в лимфоидных органах.
Слайд 18
Эмбриональное кроветворение
До 7-го месяца эмбриональное кроветворение носит универсальный
характер.
Период изменения территории и типа кроветворения наиболее уязвим
для возникновения врожденных заболеваний крови.
Интерес к эмбриональному гемопоэзу значительно возрос в связи с возможностью трансплантации гемопоэтических предшественников, полученных из пуповинной крови.
Слайд 19
Костный мозг ребенка и взрослого человека
У ребенка красный
(активный) костный мозг располагается во всех костях скелета, а
с 3-4 лет начинается постепенное его замещение на жировой.
У взрослого человека красный костный мозг находится в губчатых костях скелета и эпифизах трубчатых костей.
Масса красного костного мозга составляет 1400-1500 гр.
Слайд 20
Структурная организация костного мозга
Костный мозг - главный орган
гемопоэза.
Кроветворная ткань заключена в костный чехол, который выполняет
защитную и регулирующую гемопоэз функцию.
Кость, ее балки и трабекулы образуют опорную структуру, ограничивающую зоны кроветворения.
Клеточные элементы костной ткани : остеобласты, остеоциты и остеокласты
Слайд 21
Структурная организация костного мозга
Костный мозг - высоко васкуляризированный
орган, сообщается с кровотоком посредством капиллярной сети.
Различают два
типа капилляров: питающие (обычные) и функциональные (синусоиды), впадающие в общий ствол центральную вену.
Синусоиды располагаются радиально, между ними, в полости или нише, находятся кроветворные клетки
Слайд 22
Структурная организация костного мозга
Стенка синусоидов состоит из трех
слоев: базальная мембрана, клетки эндотелия и адвентиции.
Эндотелий синусоидов
образует поры, через которые клетки покидают костный мозг.
Базальная мембрана - это субэндотелиальный матрикс, состоящий из ламинина и коллагена IV типа. Этот слой не является непрерывным и отсутствует, прежде всего, в местах образования пор.
Слайд 23
Структурная организация костного мозга
Клетки адвентиции - фибробласты -
непрерывным слоем покрывают эндотелий и вместе с ним образуют
барьер для кроветворных клеток, покидающих костный мозг. По мере созревания клетки перемещаются к стенке синусоидов и поступают в кровоток.
Способность гемопоэтических клеток распознавать соответствующие клетки стромы и размещаться в своих определенных зонах называется хомингом.
Слайд 24
Островки кроветворения
Кроветворение в костном мозге происходит островками, в
которых группируются клетки по росткам гемопоэза.
Расположение предшественников и
развивающихся кроветворных клеток:
в центре - делящиеся и незрелые клетки, на периферии (около стенок синусоидов) - более зрелые клетки.
Слайд 25
Островок эритробластного кроветворения. Развитие эритроцитов
Состоит из центрально
расположенного макрофага и окружающих его эритробластов, концентрирующихся напротив синуса,
к стенке прилегают ретикулоциты.
Макрофаги обеспечивают фагоцитоз ядер, передачу железа и цитокинов, для дифференцировки и созревания эритрокариоцитов.
Слайд 26
Островок эритробластного кроветворения
Мегакариоциты плотно располагаются у стенки
синусоидов.
Тромбоциты образуются в просвете синусоидов при проникновении цитоплазмы
мегакариоцита между эндотелиальными клетками.
Иногда клетки могут проходить через мегакариоциты. Это явление называется эмпириополезисом и обусловлено способностью мегакариоцитов к эндоцитозу - захвату других гемопоэтических клеток.
Слайд 27
Островок эритробластного кроветворения.
Лимфоциты и моноциты располагаются вокруг ветвей
артериальных сосудов. Гранулоциты локализуются преимущественно в отдалении от синусоидов
и лишь на стадии метамиелоцитов приближаются к их стенке.
Слайд 28
Созревание клеток
Созревая, клетки продвигаются ближе к стенке венозного
синуса и проникают между слоями стенки. Для этого в
цитоплазме эндотелиальных клеток имеются поры в 1-2 мкм, через которые клетки могут проходить при условии, что они обладают достаточной эластичностью. В противном случае клетки гибнут. Способность зрелых клеток перемещаться в направлении венозного синуса называется хемотаксисом. Этот процесс опосредован влиянием на клетку специальных веществ - хемоаттрактантов, продуцируемых пристеночными клетками
Слайд 29
Строение костного мозга
Жировые клетки заполняют у взрослых пространство
костномозговой полости, не занятое миелоидной тканью. Они являются энергетическим
депо костного мозга, лабильным матриксом, легко теряющим липиды для обеспечения плацдарма развития кроветворных клеток в условиях повышенного запроса при различных патологических состояниях.
Способность жировых клеток адсорбировать на своей поверхности достаточно большой спектр физиологически активных субстанций позволяет им участвовать в регуляции процессов пролиферации и дифференцировки гемопоэтических клеток-предшественников.
Слайд 30
Стромальное микроокружение
Строма - производное мезенхимы.
Состоит из
высокоспециализированных клеток - фибробластов, жировых клеток (адипоцитов), макрофагов, остеобластов,
эндотелиальных клеток, внеклеточного матрикса, кровеносных сосудов и нервных окончаний.
Внеклеточный (экстрацеллюлярный) матрикс - продукты секреции стромальных клеток (коллагеновые или ретикулиновые волокна, фибронектин, ламинин, гликозаминогликаны, тенасцин и др.).
Клетки стромы и соединительнотканные волокна образуют сеть, в которой располагаются кроветворные элементы, составляющие паренхиму костного мозга.
Слайд 31
Стромальное микроокружение
Гемопоэтические клетки находятся в тесном контакте с
клетками стромы.
В регуляции процессов пролиферации и дифференцировки гемопоэтических
клеток большую роль играет стромальное микроокружение.
Строма костного мозга является источником сигналов, которые воспринимаются рецепторами мембран клеток, преобразуются при участии сложных взаимодействий клеточных органелл и поступают в ядро, где происходит запуск экспрессии генов, необходимых для клеточной пролиферации и дифференцировки.
Слайд 32
Стромальное микроокружение
В результате этого начинают реализовываться генетические программы,
ответственные за формирование тканеспецифических и стадиеспецифических клеточных фенотипов с
соответствующими морфологическими и функциональными особенностями клеток гемопоэза.
Функциональные и структурные изменения элементов микроокружения могут быть причиной нарушений кроветворной функции костного мозга.
Слайд 33
Клетки стромы костного мозга
Фuбробласmы - крупные веретенообразные или
вытянутые клетки с ядром овальной формы, несколькими ядрышками и
базофильной цитоплазмой
Слайд 34
Клетки стромы костного мозга
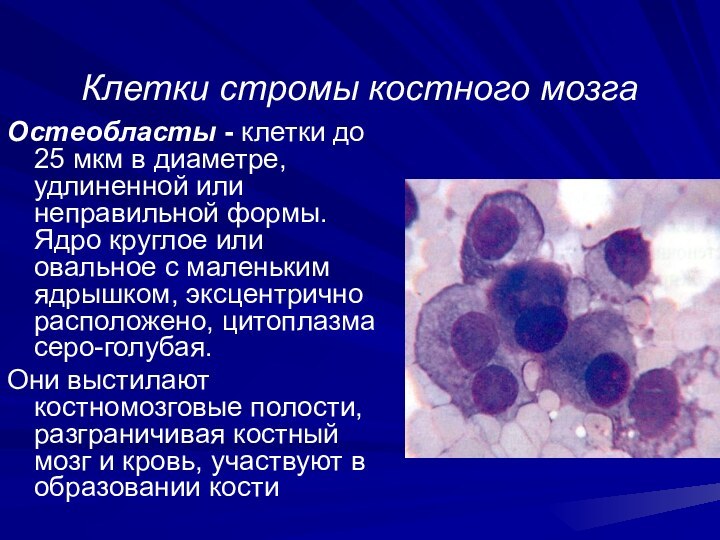
Осmеобласmы - клетки до 25
мкм в диаметре, удлиненной или неправильной формы. Ядро круглое
или овальное с маленьким ядрышком, эксцентрично расположено, цитоплазма серо-голубая.
Они выстилают костномозговые полости, разграничивая костный мозг и кровь, участвуют в образовании кости
Слайд 35
Клетки стромы костного мозга
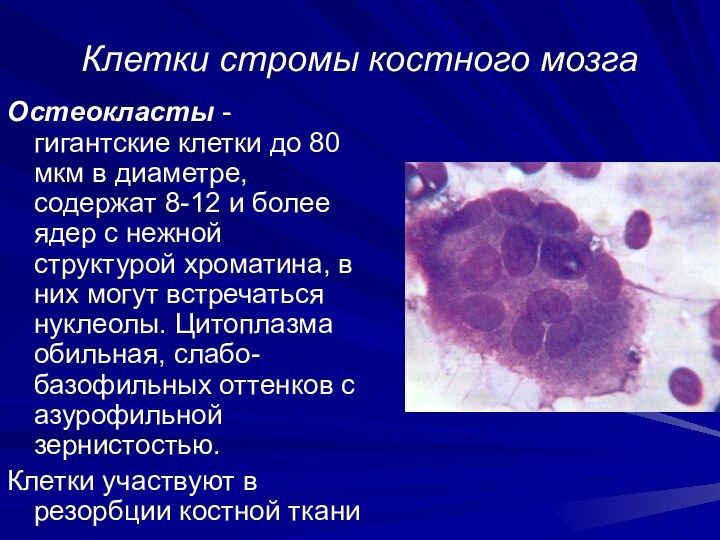
Остеокласты - гигантские клетки до
80 мкм в диаметре, содержат 8-12 и более ядер
с нежной структурой хроматина, в них могут встречаться нуклеолы. Цитоплазма обильная, слабо-базофильных оттенков с азурофильной зернистостью.
Клетки участвуют в резорбции костной ткани