Слайд 2
План лекції
Істроя відкриття вірусу імунодефіциту людини.
Структура
вірусу імунодефіциту людини.
Патогенетичні механізми розвитку імунодефіциту при ВІЛ-інфекції.
Клінічна класифікація та основні клінічні прояви ВІЛ-інфекції у різні стадії.
Специфічна діагностика. Нормативно-правові аспекти тестування на ВІЛ-інфекцію.
Сучасні підходи до проведення антиретровірусної терапії.
Опортуністичні інфекції: пневмоцистна пневмонія, криптоспоридіоз, цитомегаловірусная інфекція.
Слайд 3
ВІЛ-інфекція
Антропонозне прогресуюче захворювання, яке виникає у випадку
зараження вірусом імунодефіциту людини та вражає імунну систему з
подальшим розвитком імунодефіциту
Синдром набутого імунодефіциту
Це кінцева стадія ВІЛ-інфекції, яка характеризується глибоким імунодефіцитом, приєднанням тяжких оппортуністичних захворювань, які неминуче призводять до смерті хворого.
Слайд 4
У 1981 році вірусолог Роберт Галло (США) припустив,
що збудником може бути вірус
У 1981 році у США
було зареєстровано декілька декілька випадків тяжкої пневмоцистної пневмонії летальним кінцем. У всіх хворих був глибокий імунодефіцит і всі мали гомосексуальні контакти.
У 1983 році Люк Монтанье (Франція) повідомляє про відкриття раніше невідомого лімфотропного ретровірусу.
Слайд 5
Люк Монтанье
Нобелівськая премія у 2008 році "за
відкриття вірусу імунодефіциту людини"
Слайд 6
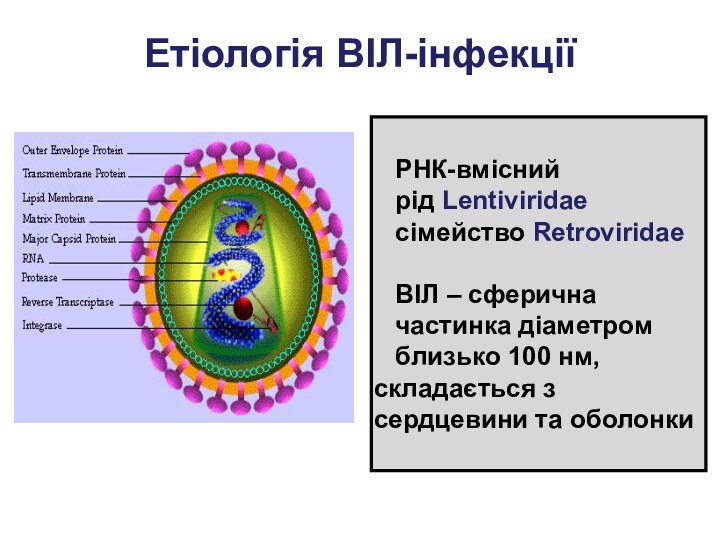
Етіологія ВІЛ-інфекції
РНК-вмісний
рід Lentiviridae
сімейство Retroviridae
ВІЛ – сферична
частинка діаметром
близько 100 нм, складається з сердцевини та оболонки
Слайд 7
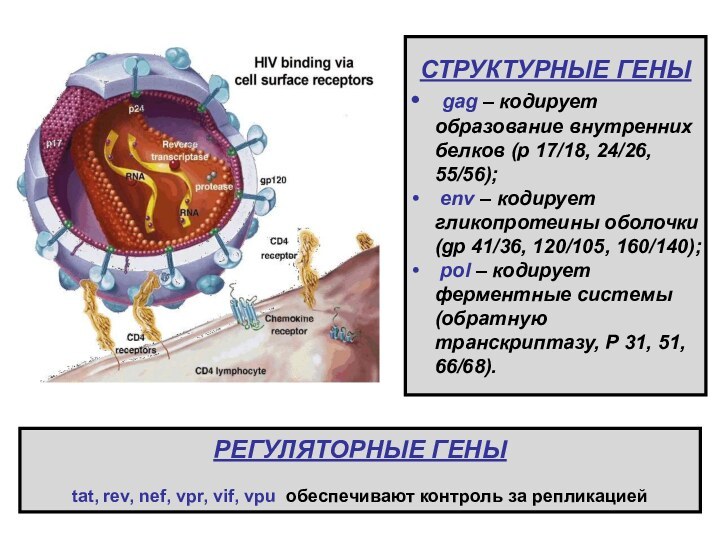
РЕГУЛЯТОРНЫЕ ГЕНЫ
tat, rev, nef, vpr, vif, vpu обеспечивают
контроль за репликацией
СТРУКТУРНЫЕ ГЕНЫ
gag – кодирует образование внутренних
белков (р 17/18, 24/26, 55/56);
env – кодирует гликопротеины оболочки (gp 41/36, 120/105, 160/140);
pol – кодирует ферментные системы (обратную транскриптазу, Р 31, 51, 66/68).
Слайд 8
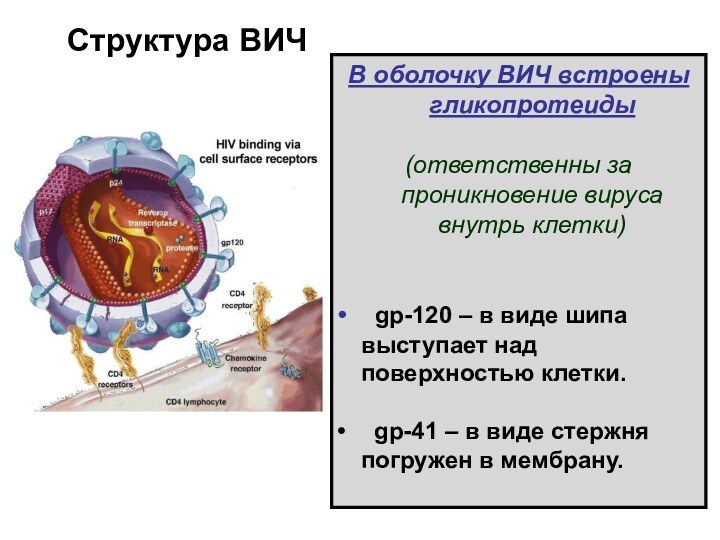
Структура ВИЧ
В оболочку ВИЧ встроены гликопротеиды
(ответственны за
проникновение вируса внутрь клетки)
gp-120 – в виде шипа
выступает над поверхностью клетки.
gp-41 – в виде стержня погружен в мембрану.
Слайд 9
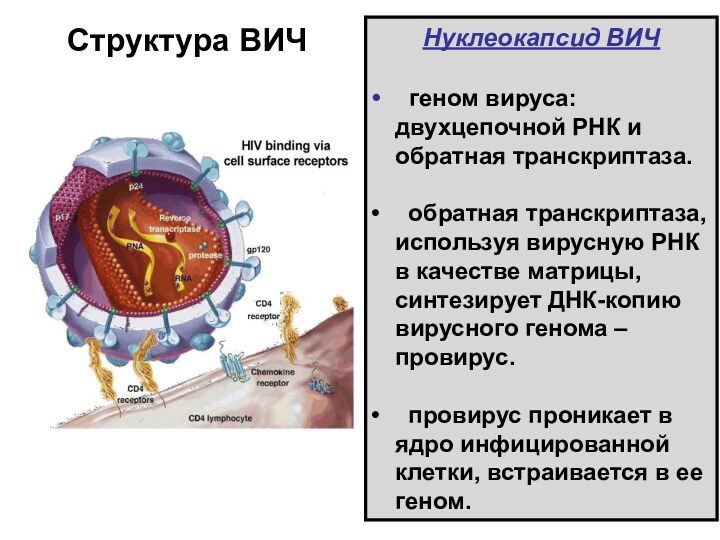
Структура ВИЧ
Нуклеокапсид ВИЧ
геном вируса: двухцепочной РНК и
обратная транскриптаза.
обратная транскриптаза, используя вирусную РНК в
качестве матрицы, синтезирует ДНК-копию вирусного генома – провирус.
провирус проникает в ядро инфицированной клетки, встраивается в ее геном.
Слайд 10
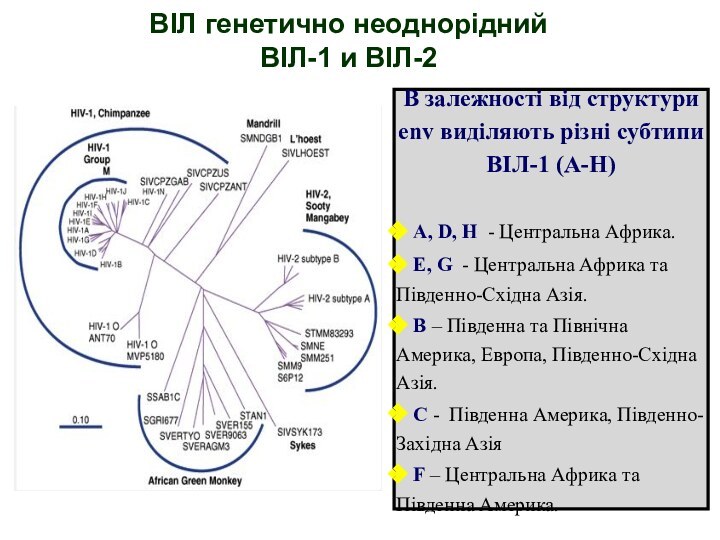
ВІЛ генетично неоднорідний
ВІЛ-1 и ВІЛ-2
В залежності від структури
env виділяють різні субтипи
ВІЛ-1 (А-H)
A, D, H -
Центральна Африка.
E, G - Центральна Африка та Південно-Східна Азія.
В – Південна та Північна Америка, Европа, Південно-Східна Азія.
С - Південна Америка, Південно-Західна Азія
F – Центральна Африка та Південна Америка.
Слайд 11
Стійкість ВІЛ у зовнішньому середовищі
при кип'ятінні гине через
1 хвилину;
при пастеризації – через 30 хвилин;
96° спирт вбивает
вірус через 1 хвилину;
быстро гине під дією хлораміну, 3% розчину перекису водню (3-5 хв.).
Стійкий до ультрафиолетового опромінення, іонизируючої радіації та заморожуванні при мінус 70°С.
Слайд 12
Епідеміологія
Джерело інфекції – ВІЛ-інфіковані: хворі усіма клінічними формами
хвороби, в крові яких циркулює вірус.
Наибільшу епідемічну небезпеку мають
кров, сперма, менструальні виділення, вагінальний секрет, які мають достатню для зараження дозу збудника.
ВІЛ виявляється у грудному молоці, слюні, слізній та спинномозковій рідині, у бронхіальній рідині.
Слайд 13
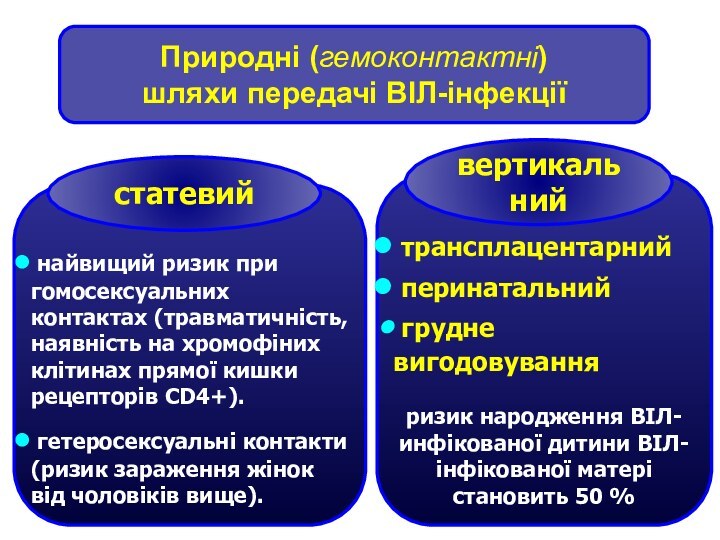
Природні (гемоконтактні)
шляхи передачі ВІЛ-інфекції
найвищий ризик при гомосексуальних
контактах (травматичність, наявність на хромофіних клітинах прямої кишки рецепторів
CD4+).
гетеросексуальні контакти (ризик зараження жінок від чоловіків вище).
статевий
трансплацентарний
перинатальний
грудне вигодовування
ризик народження ВІЛ-инфікованої дитини ВІЛ-інфікованої матері становить 50 %
вертикальний
Слайд 14
АРТИФІЦІАЛЬНІ (гемоконтактные)
шляхи передачі ВІЛ-інфекції
переливання крові та препаратів крові;
операції,
ендоскопічні маніпуляції;
ризик професіонального инфікування медпрацівників при контакті з
кров`ю 3%
медичні
в/в вживання наркотиків (ризик зараження дуже високий);
немедичні
Слайд 15
Епідемічна ситуація у світі
ПАНДЕМІЯ: за даними ВОЗ у
світі інфіковано приблизно 40 млн людей;
Поширеність ВІЛ-инфекції різна в
різних країнах світу:
Найбільша кількість ВІЛ-інфікованих у краінаї Центральної та Південної Африки – 25 млн.
Найшвидше епідемічна ситуація погуршється у країнах Центральної та Східної Європи.
Слайд 16
Епідемічна ситуація в Україні
В Україні найбільш високий показник
ВІЛ-інфікованних в Європі – 1,4 %.
10 % від всіх
інфікованих– діти;
60 % інфікованих – особи до 30 років;
В Україні зростає частота гетеросексуального шляху передачі ВІЛ;
в Україні :
більше 95000 ВІЛ-інфікованих,
з них більше 11000 – хворі СНІДом
Слайд 17
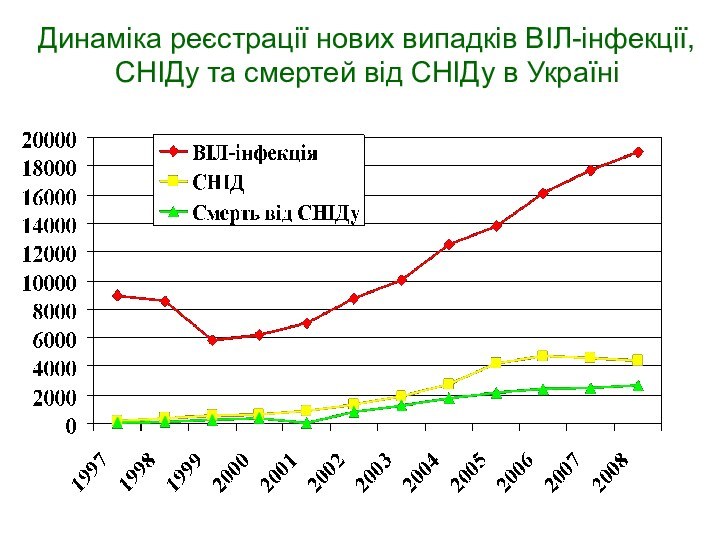
Динаміка реєстрації нових випадків ВІЛ-інфекції, СНІДу та смертей
від СНІДу в Україні
Слайд 18
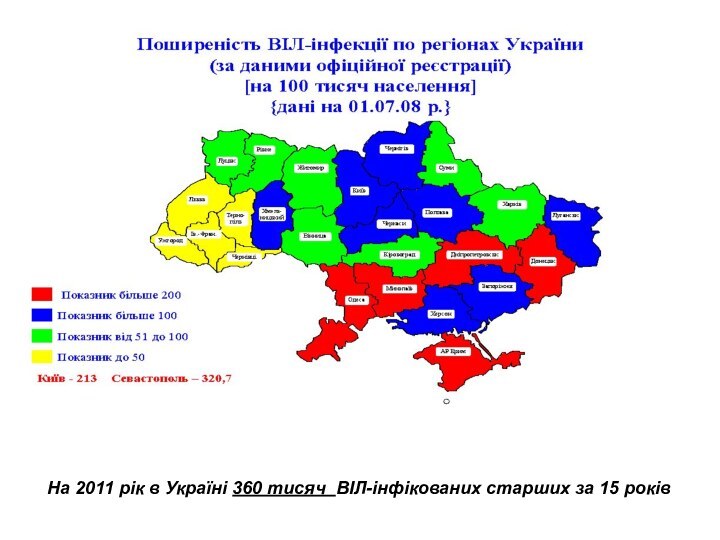
На 2011 рік в Україні 360 тисяч ВІЛ-інфікованих
старших за 15 років
Слайд 19
ВІЛ може проникати тількі в ті клітини, які
мають рецептори антигений комплекс CD 4+
CD4+ є на мембранах
клітин:
Т-хелпери (мають найбільшу кількість рецепторів CD4+);
моноцити / макрофаги;
клітини олигодендроглії та астроциты мозку;
тимус, кістковий мозок;
ендотелиоцити судин;
макрофаги альвеол;
хромафінні клітини кишківника;
клітини Лангерганса
фолікуллярні дендритні клітини л/в.
Слайд 20
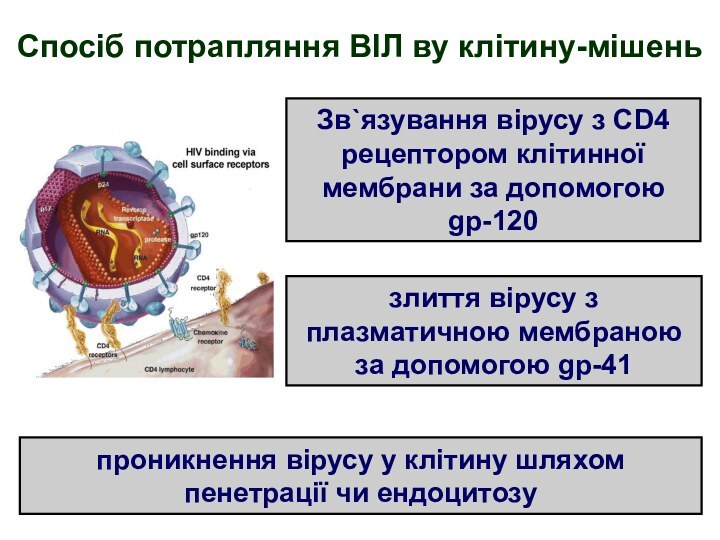
Спосіб потрапляння ВІЛ ву клітину-мішень
Зв`язування вірусу з CD4
рецептором клітинної мембрани за допомогою gp-120
злиття вірусу з плазматичною
мембраною за допомогою gp-41
проникнення вірусу у клітину шляхом пенетрації чи ендоцитозу
Слайд 21
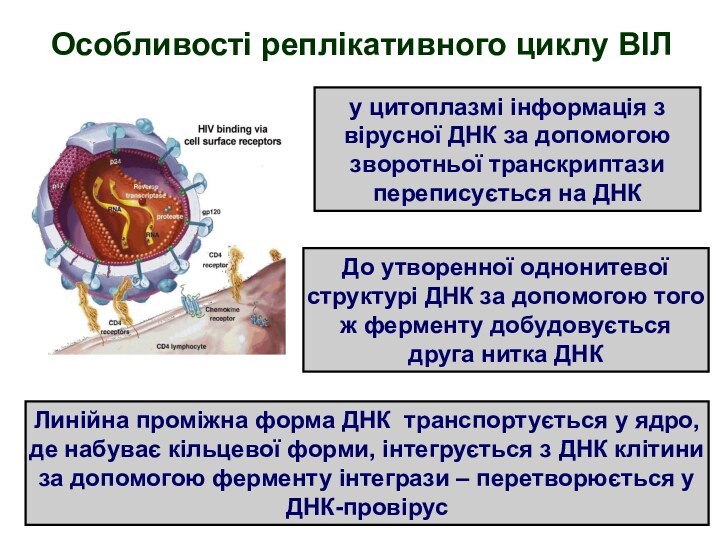
Особливості реплікативного циклу ВІЛ
у цитоплазмі інформація з вірусної
ДНК за допомогою зворотньої транскриптази переписується на ДНК
До утворенної
однонитевої структурі ДНК за допомогою того ж ферменту добудовується друга нитка ДНК
Линійна проміжна форма ДНК транспортується у ядро, де набуває кільцевої форми, інтегрується з ДНК клітини за допомогою ферменту інтегрази – перетворюється у ДНК-провірус
Слайд 22
Особливості реплікативного циклу ВІЛ
інтеграція ВІЛ в геном –
можлива тривала латенція у деяких хворих;
ключовий момент патогенезу ВІЛ
– активація провирусу (життевий цикл 1-2 доби);
активна вирусна реплікація напряму корелюється з клінічними проявами. Щодня 10 млрд нових вірусних частинок та руйнування 200 млн CD4-лімфоцитів;
Частота мутацій вирусу 1 на 1000 реплікацій (через нестабільність зворотньої транскриптази): «уникання» імунного надзору та змінення чутливості до противовірусних препаратів.
Слайд 23
Ранні імунні порушення при ВІЛ-інфекції
Вірусемия різко зростає, загальна
кількість Т-хелперів зменшується через цитопатогенний эфект ВІЛ.
Формується клон специфичних
Т-хелперів та Т-кілерів, виробляються противовірусні імуноглобуліни зменшується вірусемія та відновлюється кількість Т-хелперів.
Можлива лимфомоноцитарна реакція на проліферацію вірусу.
У 25-35 % хворих – гострий ретровірусний синдром
Слайд 24
Патогенез первинного пошкодження мозку
при ВІЛ-інфекції:
пряма цитопатична дія ВІЛ
на інфіковані клітини нервової системи
нейротоксичність розчинного вірусного білку gp120.
ВІЛ
вражає ендотеліальні клітини судинних сплетінь мозку та епендими шлуночків з развитком вірус-індукованого васкуліту.
Пошкоджуюча дія противовірусних антитіл та сенсибілизованних лімфоцитів.
Вірус знижує продукцію нейропептидів – гормонів епіфізарно-гіпоталамічного комплексу.
Слайд 25
Інкубаційний період (від моменту інфікування до перших клінічних
проявів чи сероконверсії)
від 2 тижнів до 1 року.
Класифікація
ВОЗ (2006) виділяє клінічні стадії:
Стадія первинної ВІЛ-інфекції
Безсимптомний перебіг
Гострий ретровірусний синдром:
- мононуклеозоподібний синдром
- грипоподібний синдром часто з п`ятнисто-
папульозними висипами
- серозний менінгіт, енцефаліт
- тромбоцитопенічна пурпура
- пневмонія
- гастроентерит
Слайд 26
Класифікація ВОЗ (2006) виділяє клінічні стадії :
Клінічна
стадія 1
Безсимптомний перебіг
Генералізована персистуюча лімфоаденопатія
збільшення 2 груп
лімфатичних вузлів
(за виключенням пахових) більше 1 см протягом більше 3-х місяців
Тривалість данної стадії напряму залежить від
абсолютної кількості СD4+ лімфоцитів.
Слайд 27
Класифікація ВОЗ (2006) виділяє клінічні стадії :
Клінічна
стадія 2
Немотивоване зниження ваги тіла < 10 %
Рецидивуючі інфекційні
ураження дихальних шляхів (ГРЗ, синусити, фарінгіти та інше.)
Herpes zoster
Рецидивуючі віриазкові ураження порожнини роту
Ангулярний хейліт
Папульозний чи уртикарний висип із зудом
Себорейний дерматит
Грибкові ураження пальців
Слайд 28
Класифікація ВОЗ (2006) виділяє клінічні стадії :
Клінічна
стадія 3
Значна втрата ваги тіла> 10 %, пітливість
Діарея, яка
продовжується більше 1 місяця
Постійна чи ремітуюча лихоманка більше 1 міс
Кандидоз порожнини рота.
Волосиста лейкоплакія язику
Легеневий туберкульоз, підтверджений в останні 2 роки
Тяжкі бактеріальні інфекції (пневмонія, емпіема, кісткова чи поєднанна з нею інфекція, менінгіт)
Гострий некротичний виразковий стоматит, гінгівіт
Нез`ясованного генезу анемія(Hb <8 г/дл), нейтропенія (<500 клітин/мкл), тромбоцитопенія (<50000 клітин/мкл) впродовж 1 міс.
Слайд 29
Класифікація ВОЗ (2006) виділяє клінічні стадії :
Клінічна
стадія 4
Пневмоцистна пневмонія
ВІЛ-кахексія
Саркома Капоши
Хронічний Herpes simplex (оролабіальний, генітальний, аноректальний)
впродовж більше 1 місяця
Вісцеральні ураження Herpes simplex
Кандидоз стравоходу, трахеї, бронхів, легень
Інші диссеменовані мікози(гістоплазмоз та інше.)
Позалегеневий криптококкоз, включаючи менінгіт
Позалегеневий туберкульоз
Токсоплазмоз ЦНС
ЦМВ-інфекція (ретиніт, ураження внутрішніх органів)
ВІЛ-енцефалопатія
Криптоспоридіоз
Лімфома мозку
Слайд 30
ВІЛ-енцефалопатія / СНІД-дементний комплекс (первинне ураження мозку- підгострий
енцефаліт)
На 1 вражений лімфоцит припадає 10000 неуражених,
на 1
вражену нервову клітину - від 10 до 100 неуражених
I стадія – професійні навички та самообслуговування збережено, незначні порушення походки. При спеціальному психіатричному обстеженні – незначне порущення когнітивних функцій.
II стадія - основні навички самообслуговування збережено, самостійне пересування з використанням опори. Вирішення складних побутових задач та професійна діяльність ускладнена.
III стадія - тяжке порушеня когнітивних функцій: хворий не може слідкувати за новинами, не запам`ятовує події, які торкаються його особисто, не може підтримувати розмову, загальованність, порушення координації, неможливість пересування без сторонної допомоги.
IV стадія – стан близький до вегетативного, повна втрата інтелектуальних можливостей, мовний контакт неможливий, парези, паралічі, тазові розлади.
Слайд 31
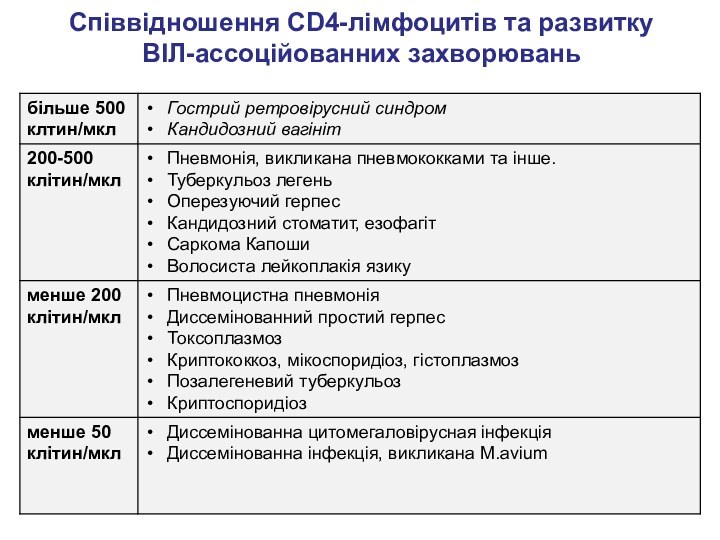
Співвідношення CD4-лімфоцитів та развитку
ВІЛ-ассоційованних захворювань
Слайд 32
Тестування крові проводиться тільки після добровільної письмової згоди
пацієнта та предтестової консультації
Слайд 33
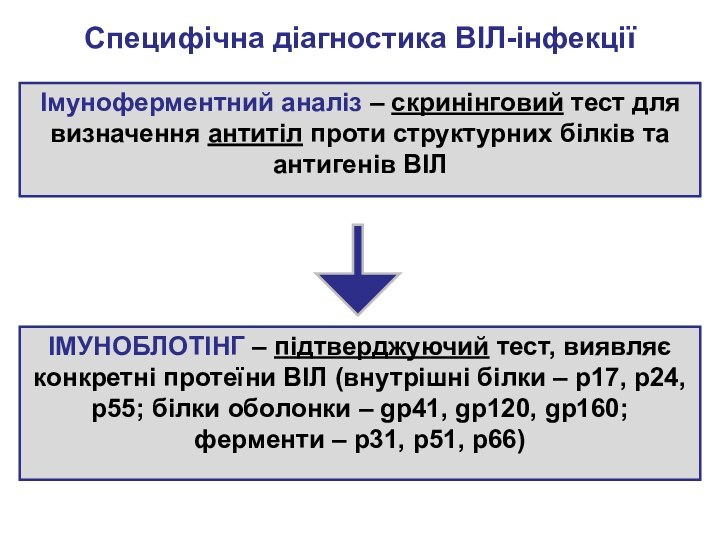
Специфічна діагностика ВІЛ-інфекції
Імуноферментний аналіз – скринінговий тест для
визначення антитіл проти структурних білків та антигенів ВІЛ
ІМУНОБЛОТІНГ –
підтверджуючий тест, виявляє конкретні протеїни ВІЛ (внутрішні білки – р17, р24, р55; білки оболонки – gp41, gp120, gp160; ферменти – р31, р51, р66)
Слайд 34
Показання до високоактивної антиретровірусної терапії
Кількість CD4-лімфоцитів менше 350
клітин/мкл, незалежно від симптомів захворювання.
Кількість CD4-лімфоцитів більше 350 клітин/мкл,
але високе вірусне навантаження (>100000 копій/мл)
Будь-яке ВІЛ-індикаторне захворювання.
Вагітність, незалежно від вірусологічних чи імунологічних показників.
Ко-інфекция ВІЛ/ВГВ при наявності показань до лікування ВГВ
Слайд 35
Високоактивна антиретровірусна терапія
назначення одразу 3-х препаратів, два з
яких відносяться до класу інгібіторів зворотьої транскриптази
I
Інгібітори зворотньої транскриптази:
Нуклеозидні:
ЗИДОВУДИН, АЗИДОТИМИДИН – по 600 мг/добу;
СТАВУДИН – по 60-80 мг/добу;
ДИДАНОЗИН – по 250-400 мг/добу (вага х-го менше та більше 60 кг);
ЛАМИВУДИН – по 300 мг/добу;
АБАКАВИР – по 600 мг/добу.
Ненуклеозидні:
НЕВИРАПИН – по 400 мг/добу;
ДЕЛАВИРДИН – по 1200 мг/добу.
II Інгібітори протеази:
САКВИНАВИР – по 1,6-3,6 гр/добу;
ИНДИНАВИР – по 2,4 гр/добу;
РИТОНАВИР – по 1,2 гр/добу.
Слайд 36
Критерії оцінки ефективності ВААРТ:
- зменшення вірусного навантаження
- збільшення
кількості CD4-лімфоцитів
- ослаблення клінічних проявів
Змінити схему терапії потрібно при:
неефективності
поточної схеми терапії з доказами прогресування захворювання на основі вірусологічних, імунологічних та клінічних данних
Токсичність чи непереносимість поточної схеми
Поява змоги назначення нової схеми, яка перевершує по ефективності поточну терапію.
Слайд 37
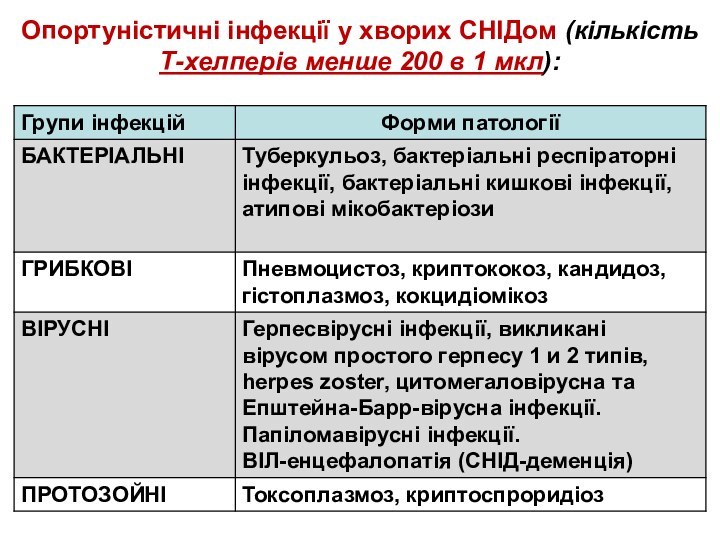
Опортуністичні інфекції у хворих СНІДом (кількість Т-хелперів менше
200 в 1 мкл):
Слайд 38
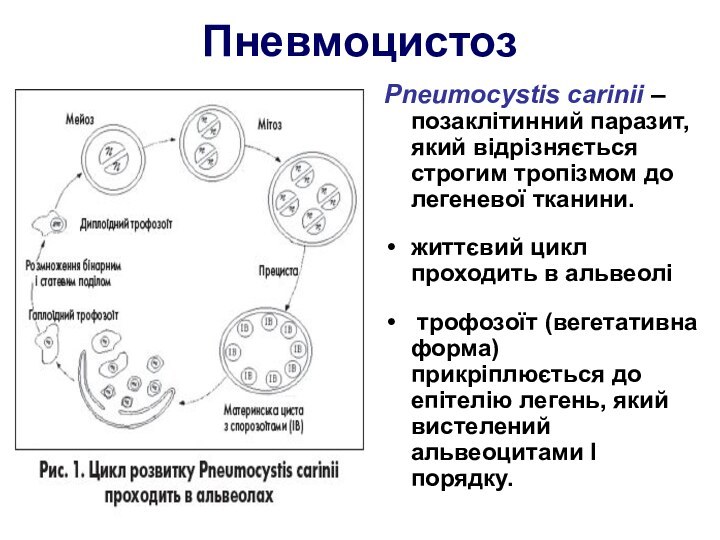
Пневмоцистоз
Pneumocystis carinii – позаклітинний паразит, який відрізняється строгим
тропізмом до легеневої тканини.
життєвий цикл проходить в альвеолі
трофозоїт
(вегетативна форма) прикріплюється до епітелію легень, який вистелений альвеоцитами I порядку.
Слайд 39
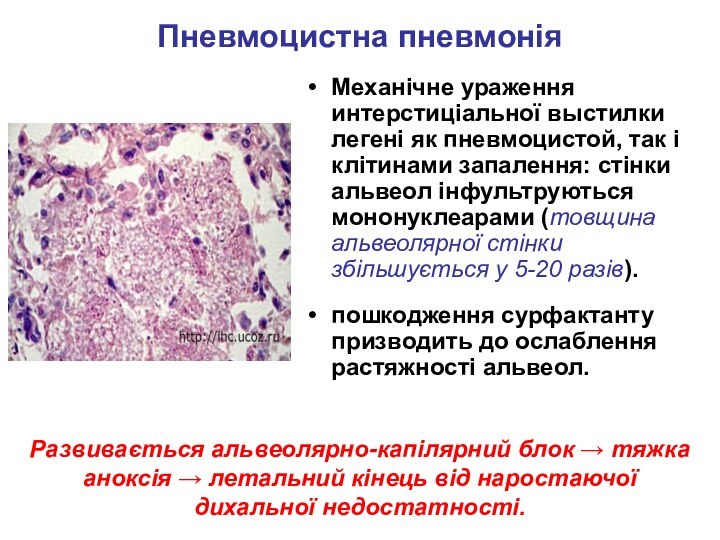
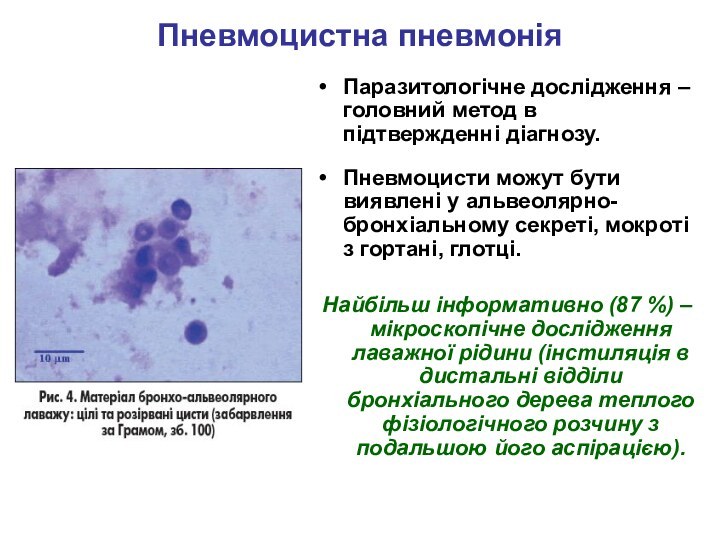
Пневмоцистна пневмонія
Механічне ураження интерстиціальної выстилки легені як пневмоцистой,
так і клітинами запалення: стінки альвеол інфультруються мононуклеарами (товщина
альвеолярної стінки збільшується у 5-20 разів).
пошкодження сурфактанту призводить до ослаблення растяжності альвеол.
Развивається альвеолярно-капілярний блок → тяжка аноксія → летальний кінець від наростаючої дихальної недостатності.
Слайд 40
Пневмоцистна пневмонія
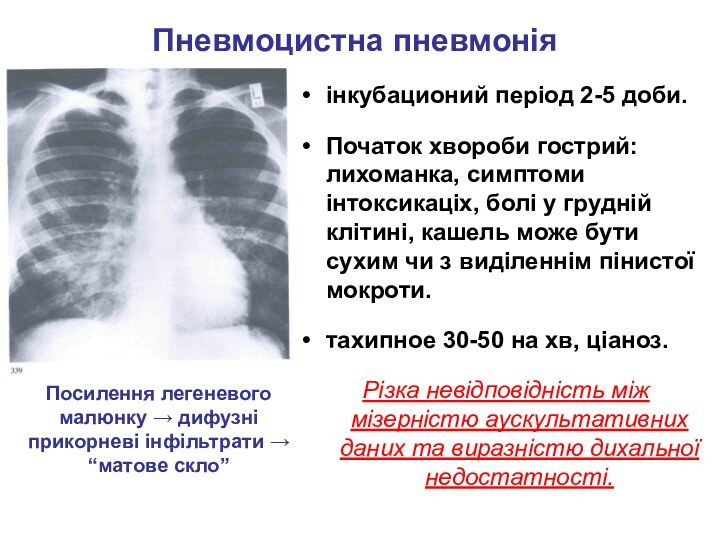
інкубационий період 2-5 доби.
Початок хвороби гострий: лихоманка,
симптоми інтоксикаціх, болі у грудній клітині, кашель може бути
сухим чи з виділеннім пінистої мокроти.
тахипное 30-50 на хв, ціаноз.
Різка невідповідність між мізерністю аускультативних даних та виразністю дихальної недостатності.
Посилення легеневого малюнку → дифузні прикорневі інфільтрати → “матове скло”
Слайд 41
Пневмоцистна пневмонія
Паразитологічне дослідження – головний метод в підтвержденні
діагнозу.
Пневмоцисти можут бути виявлені у альвеолярно-бронхіальному секреті, мокроті з
гортані, глотці.
Найбільш інформативно (87 %) – мікроскопічне дослідження лаважної рідини (інстиляція в дистальні відділи бронхіального дерева теплого фізіологічного розчину з подальшою його аспірацією).
Слайд 42
Пневмоцистна пневмонія
ПРОФІЛАКТИКА:
при зниженні вмісту СD4+ лімфоцитів менше
200 кл в 1 мкл назначають ТРИМЕТОПРИМ-СУЛЬФАМЕТОКСАЗОЛ 0,96 г
1 раз на добу 3 дні підряд кожного тижня.
ЛІКУВАННЯ:
Триметоприм по 0,015 г/кг добу (в/в, per os) в поєднанні з Дапсоном по 100 мг/добу per os протягом 3-х тижнів;
Клиндамицин по 1,2 г/добу (в/в, per os) в поєднанні з Примахином по 30 мг/добу per os протягом 3-х тижнів;
Триметоприм-сульфаметоксазол (по Триметоприму 0,02 г/кг добу) – 3 тижні, потім по 0,96 г – 4 тижні.
Слайд 43
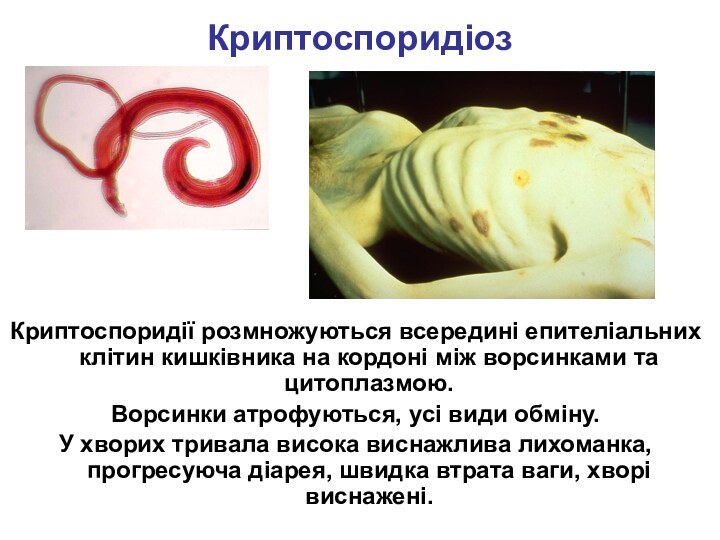
Криптоспоридіоз
Криптоспоридії розмножуються всередині епителіальних клітин кишківника на кордоні
між ворсинками та цитоплазмою.
Ворсинки атрофуються, усі види обміну.
У хворих тривала висока виснажлива лихоманка, прогресуюча діарея, швидка втрата ваги, хворі виснажені.
Слайд 44
Криптоспоридіоз
ДІАГНОСТИКА:
мікроскопія калу при окрасці по Циль-Нильсону.
ЛІКУВАННЯ:
макролідний
антибіотик СПИРАМИЦИН per os по 6-9 млн ОД на
добу у 3 прйоми протягом 4-х тижнів.