- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Ароматические амины.
Содержание
- 2. Ароматические амины – соединения, образующиеся при замещении атомов водорода в молекуле аммиака на ароматические радикалы
- 3. I. По положению аминогруппы относительно ароматического ядра.
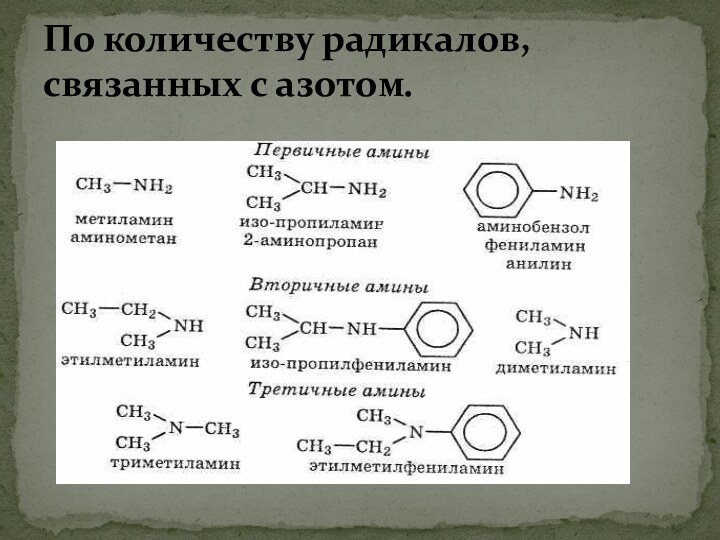
- 4. По количеству радикалов, связанных с азотом.
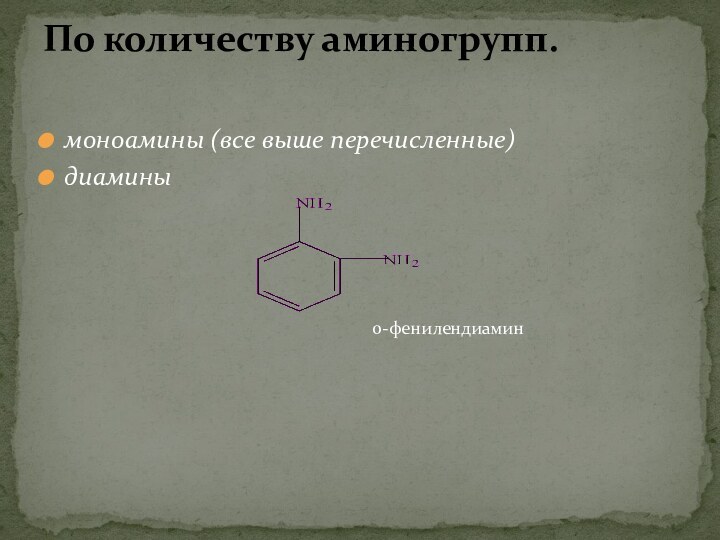
- 5. моноамины (все выше перечисленные)диаминыПо количеству аминогрупп. о-фенилендиамин
- 6. Восстановление нитросоединений – основной технический и лабораторный
- 7. Наличие неподеленной электронной пары у
- 8. Основные (т.е.щелочные) свойства ароматических аминов.
- 9. Алкилирование ароматических аминов
- 10. Горение аминов сопровождается образованием углекислого газа, азота
- 11. В ароматических
- 12. Толуидины (аминотолуолы, метиланилины, толиламины) — ароматические органические соединения, амминопроизводные толуола.
- 13. Дифениламин ((N-фенил)-анилин) — вещество
- 14. Фенилендиами́н C6H4(NH2)2 —
- 15. Источники Ароматических аминов.Антропогенные:промышленные отходы(загрязнения воды и воздуха)табачный дымнекоторые виды продуктов питания
- 16. Ароматические амины используются при производстве: пластмасс красителей пестицидов лекарстввзрывчатых веществ. Использование.
- 17. Многие амины довольно
- 19. Скачать презентацию
- 20. Похожие презентации
Ароматические амины – соединения, образующиеся при замещении атомов водорода в молекуле аммиака на ароматические радикалы















Слайд 2 Ароматические амины – соединения, образующиеся при замещении атомов
водорода в молекуле аммиака на ароматические радикалы
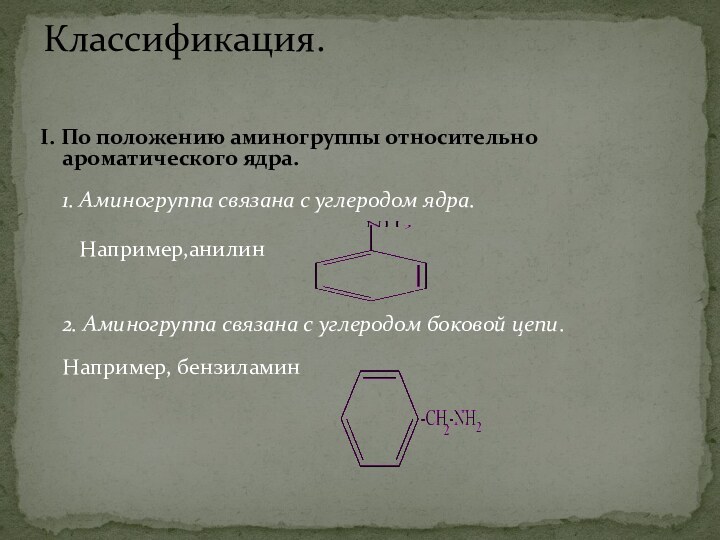
Слайд 3 I. По положению аминогруппы относительно ароматического ядра. 1. Аминогруппа
связана с углеродом ядра.
Например,анилин
2. Аминогруппа
связана с углеродом боковой цепи.
Например, бензиламин
Классификация.
Слайд 6 Восстановление нитросоединений – основной технический и лабораторный способ
получения первичных ароматических аминов. В настоящее время применяют, в
основном, процесс каталитического восстановления.Восстановление других азотсодержащих соединений.
Например, C6H5NO + 4H H2O + C6H5NH2 нитрозобензол ,
C6H5-NH-NH2 + 2H C6H5NH2 +NH3фенилгидразин Взаимодействие галогенопроизводных ароматического ряда с аммиаком. Идет с трудом, чаще применяется при наличии в о- или п-положении к галоиду группы NO2. P, t
п-O2N-C6H4-Cl + NH3 HCl + п-O2N-C6H4-NH2
п- нитрохлорбензол, п-нитроанилин
Получение .
Слайд 7 Наличие неподеленной электронной пары у атома
азота обуславливает более высокие температуры кипения, чем у соответствующих
алканов. Амины обладают неприятным резким запахом. При комнатной температуре и атмосферном давлении первые представители ряда первичных аминов — газы, неплохо растворяющиеся в воде. С увеличением углеродного радикала температура кипения повышается и уменьшается растворимость в воде.Физические свойства аминов
Слайд 8
Основные (т.е.щелочные) свойства ароматических аминов.
Основные свойства ослаблены из-за влияния ароматического ядра Если аминогруппа
связана с двумя ароматическими ядрами, то основные свойства будут еще слабее.Трифениламин вообще не проявляет основных свойств.
Заместители I рода способствуют усилению основных свойств, заместители II рода – их ослаблению.
Ароматические амины, имеющие алкильные заместители у азота, имеют большую основность, например,
N-метиланилин более сильное основание, чем анилин.
Основные свойства проявляются в способности образовывать соли C6H5-NH2-CH3 + HCl [C6H5N+H3]Cl- или С6H5-NH2 . HCl, хлористый фениламмоний солянокислый анилин – растворимая в воде соль.
C6H5-NH2 + H2SO4 [C6H5NH3]+SO4-H или С6H5-NH2 . H2SO4
сернокислый анилин– мало растворимая в воде соль.
. Химические свойства.
Слайд 9
Алкилирование ароматических аминов
Ароматические
амины способны замещать водород аминогруппы на алкилы. Эта реакция
приводит к вторичным и третичным аминам:C6H5NH2 + CH3I → C6H5-NH-CH3 + CH3I → C6H5-N(CH3)2
Алкилирование ведут спиртами или хлоралканами, в качестве катализаторов используют соли одновалентной меди в виде аммиачных комплексов. Важно, что процесс алкилирования является последовательно-параллельным. Это обусловлено тем, что образовавшийся амин, в свою очередь, способен реагировать с алкилирующим агентом. Состав продуктов зависит от соотношения реагентов.
Ацилирование ароматических аминов.
При действии ацилирующих агентов (кислоты, ангидриды, хлорангидриды) водородные атомы аминогруппы замещаются на ацильные остатки.
Ацильные производные не обладают основными свойствами. Они обладают устойчивостью к окислителям и потому используются в качестве промежуточных веществ в реакциях аминов в присутствии окислителей, например, нитрования.
Слайд 10 Горение аминов сопровождается образованием углекислого газа, азота и
воды:4CH3NH2+9О2=4СO2+2N2+10Н2О Ароматические амины самопроизвольно окисляются на воздухе. Так, анилин быстро
буреет на воздухе вследствие окисления. Присоединение алкилгалогенидов Амины присоединяют галогеналканы с образованием соли: Обрабатывая получившуюся соль щелочью, можно получить свободный аминВзаимодействие аминов с азотистой кислотой Огромное значение имеет реакция диазотирования первичных ароматических аминов под действием азотистой кислоты, получаемой in situ по реакции нитрита натрия с соляной кислотой:
вторичные ароматические амины дают N-нитрозопроизводные: R-NH2 + NaNO2+НСl=R-OH+N2+NaCl+H2O
Окисление.
Слайд 11 В ароматических аминах
аминогруппа облегчает замещение в орто- и пара-положениях бензольного кольца.
Поэтому галогенирование анилина происходит быстро и в отсутствие катализаторов, причем замещаются сразу три атома водорода бензольного кольца, и выпадает белый осадок 2,4,6-триброманилина:Эта реакция бромной водой используется как качественная реакция на анилин.
Ароматическое электрофильное замещение в ароматических аминах
Слайд 12 Толуидины (аминотолуолы, метиланилины, толиламины) — ароматические органические соединения, амминопроизводные толуола. Жидкости
или твёрдые вещества, хорошо растворяются в Этаноле, диэтиловом эфире, ацетоне, хлороформе, плохо — в
воде. Перегоняются с водяным паром, при хранении на свету в присутствии воздуха, как и анилин, темнеют.Применение:
Для получения аминотолуолсульфокислот, крезолов, азокрасителей, трифенилметановых и сернистых красителей.
п-толуидин входит в состав ингибиторов коррозии.
м-толуидин используют для получения 3-хлортолуола.
2- аминотолуол
Представители ароматических аминов.
Слайд 13 Дифениламин ((N-фенил)-анилин) — вещество с
формулой (С6Н5)2NН, молярная масса которого равна 169,23.
Физические свойства.Бесцветные кристаллы, темнеющие на свету; Температура плавления 54-55 °C, Температура кипения 302 °C, Легко растворим в диэтиловом эфире, бензоле, ацетоне, четыреххлористом углеродеИспользование Дифениламин — исходный продукт в производстве антиоксидантов для полимеров; стабилизатор и флегматизатор термо- и атмосферостойкости нитратов целлюлозы, в том числе пироксилиновых порохов; промежуточный продукт в синтезе триарилметановых и азокрасителей, инсектицидов;ингибитор коррозии мягких сталей. Используется в аналитической химии для обнаружения ионов , и других окислителей, как окислительно-восстановительный индикатор (Е0 = + 0,75 В).
Слайд 14
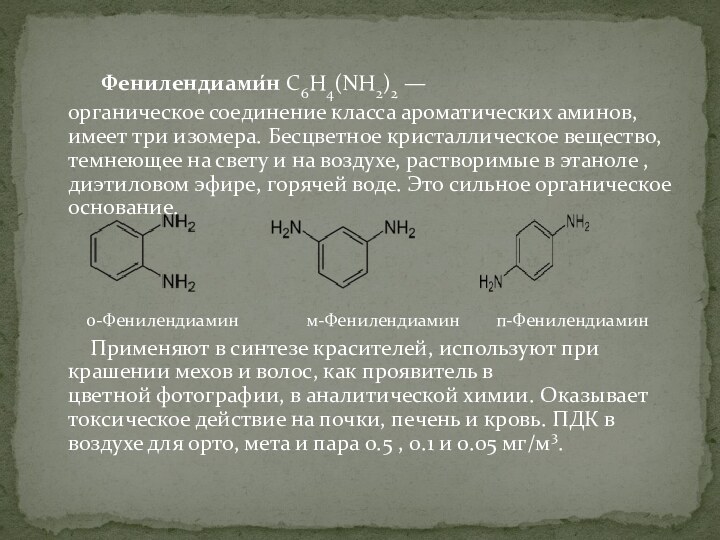
Фенилендиами́н C6H4(NH2)2 —
органическое соединение класса ароматических аминов, имеет три изомера. Бесцветное кристаллическое
вещество, темнеющее на свету и на воздухе, растворимые в этаноле , диэтиловом эфире, горячей воде. Это сильное органическое основание.о-Фенилендиамин м-Фенилендиамин п-Фенилендиамин
Применяют в синтезе красителей, используют при крашении мехов и волос, как проявитель в цветной фотографии, в аналитической химии. Оказывает токсическое действие на почки, печень и кровь. ПДК в воздухе для орто, мета и пара 0.5 , 0.1 и 0.05 мг/м3.
Слайд 15
Источники Ароматических аминов.
Антропогенные:
промышленные отходы(загрязнения воды и воздуха)
табачный дым
некоторые
виды продуктов питания
Слайд 16
Ароматические амины используются при производстве:
пластмасс
красителей
пестицидов
лекарств
взрывчатых веществ.
Использование.
Слайд 17 Многие амины довольно токсичны.
Анилин и другие ароматические амины являются кровяными и нервными
ядами. Легко проникают в организм человека через кожу или при вдыхании паров. Анилин оказывает жаропонижающее действие, однако не применяется в медицине из-за своей токсичности. Предполагавшаяся ранее сильная канцерогенность анилина в дальнейшем не нашла подтверждения. Более опасными оказались аминопроизводные нафталина и бифенила, такие, как 2-нафтил-амин, 4-аминобифенил и бензидин, вызывающие раковые опухоли у человека.Влияние вещества на организм человека.
Слайд 18
Абсорбция паров анилина через дыхательные пути составляет 5-11 мг/ч.
Жидкий анилин всасывается через кожу человека со скоростью 0,2-0,7 мг/см2/ч. Считают, что в условиях производства 2/3 анилина проникают в организм через кожу. Превращения анилина происходят в основном путем гидроксилирования ароматического кольца с образованием 55% п-аминофенола, 10% о-аминофенола и 0,1% м-аминофенола. Кроме того, образуются фенилсульфаминовая кислота (8%) и ацетанилид (0,2%). Метаболиты выделяются с мочой в виде конъюгатов. Неизмененного анилина выводится 3,5%, 6% - в виде глюкуронида (всего с мочой экскретируется 80% от дозы). Есть данные, что 70% анилина метаболизируется в фенилгидроксиламин - основное метгемоглобинообразующее соединение.Распределение и трансформация в окружающей среде и живых организмах.





























