Слайд 2
Синдром паркинсонизма. КЛАССИФИКАЦИЯ
Первичный (идиопатический) паркинсонизм (болезнь Паркинсона, наследственный
ювенильный паркинсонизм).
Вторичный паркинсонизм (лекарственный, васкулярный, токсический и гипоксический, метаболический
и постэнцефалический, опухолевый и паранеопластический, травматический при тяжелых ЧМТ или частой травматизации).
Паркинсонизм при мультисистемных нейродегенеративных заболеваниях (так называемый, паркинсонизм «плюс»): прогрессирующий надъядерный паралич, множественная системная атрофия, деменция с тельцами Леви, кортико-базальная дегенерация.
Паркинсонизм при наследственных заболеваниях ЦНС: гепатолентикулярная дегенерация (болезнь Вильсона–Коновалова), нейроферритинопатия (болезнь Галлервордена–Шпатца), дофа-чувствительная дистония, ригидная форма болезни Гентингтона, ряд форм липидозов и митохондриальных энцефалопатий.
Слайд 3
Классификация
Первичный паркинсонизм
Вторичный паркинсонизм
Паркинсонизм при других спорадических
и наследственных дегенеративных заболеваниях ЦНС
Спорадический паркинсонизм:
1.Прогрессирующий надъядерный паралич
2.Мультисистемная атрофия ( МСА):
-синдром Шая-Дрейджера
-оливопонтоцеребеллярная дегенерация
-стриатонигральная дегенерация
3.Кортикобазальная дегенерация
4.Деменция с тельцами Леви
5.БАС-паркинсонизм-деменция (паркинсонизм Гуам)
Ирритативный паркинсонизм:
1.При хорее Гентингтона
2.При болезни Вильсона-Коновалова
3.При системной кальцификации базальных ганглиев( болезнь Фара)
4. Болезнь Галлервордена – Шпатца (БГШ)
5. Нейроакантоцитоз (болезнь Бессена – Корнцвейга)
Слайд 4
Синдром «паркинсонизм плюс». признаки:
Отсутствие ответа на леводопу/агонистов дофаминовых
рецепторов на ранних стадиях заболевания
раннее развитие постуральной неустойчивости
ранняя
деменция в сочетании с расстройствами речи и глотания
пирамидная недостаточность
вегетативные симптомы
симметричность клинических проявлений на ранней стадии заболевания
Слайд 5
Нейродегенеративные заболевания
синуклеинопатии таупатии
Альфа-синуклеин в норме присутствует в пресинаптических терминалях головного мозга. При НДЗ данный белок накапливается и формирует внутри глиальных клеток нитевидные структуры.
Тау-протеин представляет собой растворимый низкомолекулярный белок, играющий важную роль в процессе роста аксона и его функционировании. При НДЗ обнаруживаются его патологические формы, образующие нити, преобладающие в телах нейронов и аксонов.
Слайд 6
Прогрессирующий надъядерный паралич
Болезнь Стила-Ричардсона-Ольшевского:
Дегенеративное заболевание головного
мозга, нейропатологически характеризующееся скоплением тау-белка в астроцитах, нейрональных отростках и нейронах; анатомически
преимущественно в бледном шаре, субталамическом ядре, красном ядре, черной субстанции и зубчатом ядре.
Распространенность: 1,39 – 6,4 на 100 тыс. населения. 4% паркинсонизма по данным патоморфологических исследований. Клинические проявления ПНП чаще развиваются в возрасте 50—60 лет, в равной степени среди мужчин и женщин.
Одним из самых важных диагностических признаков прогрессирующего надъядерного паралича является паралич взора по вертикали, который может развиваться уже на ранних стадиях заболевания. Сначала развивается паралич взора вниз, а потом вверх. Горизонтальные движения глазных яблок сохраняются или нарушаются на самых поздних стадиях болезни.
Слайд 7
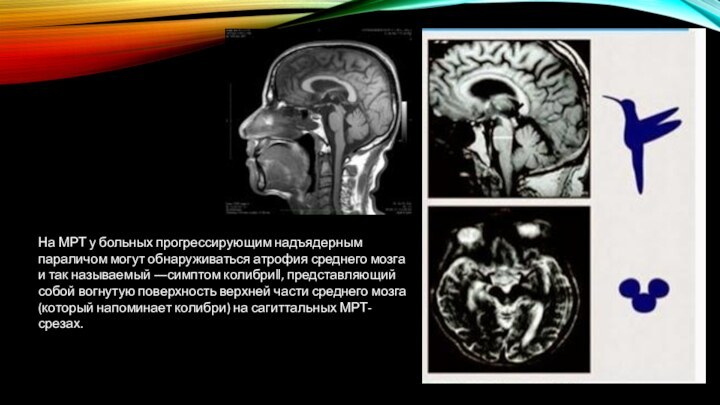
На МРТ у больных прогрессирующим надъядерным параличом могут
обнаруживаться атрофия среднего мозга и так называемый ―симптом колибри‖,
представляющий собой вогнутую поверхность верхней части среднего мозга (который напоминает колибри) на сагиттальных МРТ-срезах.
Слайд 8
Диагностические критерии
(the National Institute of Neurological Disorders and
Stroke (NINDS) and the Society for Progressive Supranuclear Palsy)
Возможный
диагноз:
постепенно прогрессирующее заболевание с возрастом начала после 40 лет
надъядерный вертикальный паралич взора или замедление произвольных движений глазных яблок по вертикали и постуральная неустойчивость с падениями в течение первого года болезни
отсутствие других заболеваний, объясняющих вышеописанные нарушения (см. критерии исключения).
Слайд 9
Вероятный диагноз:
постепенно прогрессирующее заболевание с возрастом начала после
40 лет;
надъядерный вертикальный паралич взора и постуральная неустойчивость
с падениями в течение первого года болезни;
отсутствие других заболеваний, объясняющих вышеописанные нарушения (см. критерии исключения).
Достоверный диагноз:
клиническая картина вероятного или возможного прогрессирующего надъядерного паралича + гистопатологические доказательства этого заболевания.
Слайд 10
Критерии исключения для прогрессирующего надъядерного паралича:
недавно перенесенный энцефалит;
синдром «чужой руки»‖, корковые чувствительные нарушения, лобная или височно-теменная
атрофия;
галлюцинации или бред, не связанные с допаминергической терапией;
Альцгеймеровский тип корковой деменции (выраженная амнезия и афазия/агнозия);
ранние мозжечковые симптомы или беспричинная дизавтономия (значительная гипотензия или нарушения мочеиспускания);
выраженные асимметричные паркинсонические признаки (например, брадикинезия);
нейровизуализационные данные наличия структурной патологии (например, инфаркты в области базальных ганглиев или ствола мозга, лобная атрофия);
болезнь Уиппла, в случае необходимости, подтвержденная данными полимеразной цепной реакции.
Слайд 11
Подтверждающие критерии для прогрессирующего надъядерного паралича:
симметричная акинезия
или ригидность, более выраженная в проксимальных отделах, чем в
дистальных;
патологический наклон головы, особенно ретроколлис;
низкий терапевтический эффект или отсутствие эффекта при лечении паркинсонизма препаратами леводопы;
раннее развитие дизартрии и дисфагии;
раннее развитие когнитивных нарушений, включающих, по крайней мере, два признака из перечисленных: апатия, нарушения абстрактного мышления, снижение беглости речи, нарушения поведения или лобные симптомы.
Слайд 12
лечение
Нет препаратов, способных предотвратить прогрессирования заболевания. Лечение направлено
лишь на уменьшение симптомов:
Дофаминовые агонисты+леводопа
Трициклические антидепрессанты
Метисергид (ПЭ: фиброзные поражения
внутренних органов)
Ботулотоксин (при ригидности и дистонии)
Слайд 13
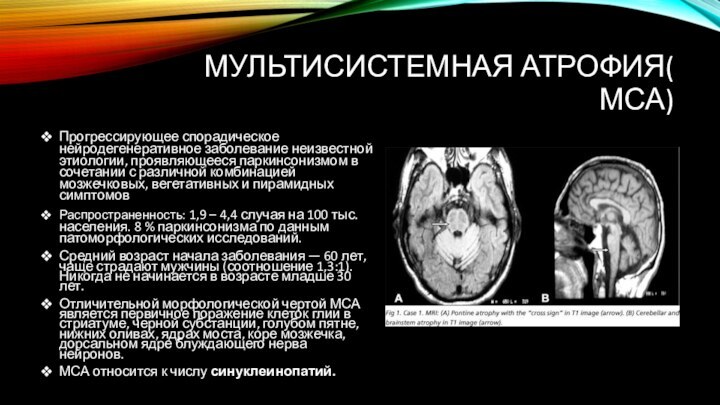
Мультисистемная атрофия( МСА)
Прогрессирующее спорадическое нейродегенеративное заболевание неизвестной этиологии,
проявляющееся паркинсонизмом в сочетании с различной комбинацией мозжечковых, вегетативных
и пирамидных симптомов
Распространенность: 1,9 – 4,4 случая на 100 тыс. населения. 8 % паркинсонизма по данным патоморфологических исследований.
Средний возраст начала заболевания — 60 лет, чаще страдают мужчины (соотношение 1,3:1). Никогда не начинается в возрасте младше 30 лет.
Отличительной морфологической чертой МСА является первичное поражение клеток глии в стриатуме, черной субстанции, голубом пятне, нижних оливах, ядрах моста, коре мозжечка, дорсальном ядре блуждающего нерва нейронов.
МСА относится к числу синуклеинопатий.
Слайд 14
Клинические варианты МСА
Стриатонигральныя дегенерация (паркинсоническая форма), проявляющаяся быстро

прогрессирующим синдромом паркинсонизма( чаще акинетико-ригидный синдром) с выраженной постуральной
неустойчивостью, нередко сочетается с вегетативной недостаточностью, пирамидными и псевдобульбарными синдромами;
оливопонтоцеребеллярная атрофия, при которой доминирует мозжечковая симптоматика в виде атаксии, тремора (постурально-кинетического, миоклонического, интенционного характера, значительно реже тремора покоя), нистагма, скандированной речи , при сочетании с псевдобульбарным синдромом, сопровождающаяся паркинсонизмом, вегетативными нарушениями и наличием пирамидных знаков;
синдром Шая-Дрейджера, который дебютирует выраженными вегетативными нарушениями с последующим быстрым развитием синдрома прогрессирующей вегетативной недостаточностью, к которой присоединяются паркинсонизм и другие проявления мультисистемной атрофии. Вегетативные нарушения: ортостатическая гипотензия, нарушение потоотделения, расстройства мочеиспускания (учащенное, задержки, недержание), запоры и редко недержание кала. Импотенция у больных мультисистемной атрофией может развиваться за 5-10 лет до появления других клинических проявлений
Слайд 15
Диагностика
(критерии 2007 г.)
Часть 1. Критерии вероятной мультисистемной
атрофии:
Спорадическое, прогрессирующее заболевание с возрастом дебюта старше 30 лет,
характеризующееся следующими проявлениями:
вегетативная дисфункция, проявляющаяся недержанием мочи (неспособность контролировать мочеиспускание, с эректильной дисфункцией у мужчин) или ортостатическое снижение артериального давления в течение 3 минут после вставания как минимум на 30 мм. рт. ст. для систолического давления или на 15 мм. рт. ст. для диастолического давления и
плохо поддающийся лечению леводопой паркинсонизм (брадикинезия с ригидностью, тремором или постуральной неустойчивостью) или
мозжечковый синдром (атаксия при ходьбе с мозжечковой дизартрией, атаксия конечностей или мозжечковые глазодвигательные нарушения).
Слайд 16
Часть 2. Критерии возможной мультисистемной атрофии:
Спорадическое, прогрессирующее
заболевание с возрастом дебюта старше 30 лет, характеризующееся следующими
проявлениями:
паркинсонизм (брадикинезия с ригидностью, тремором или постуральной неустойчивостью) или
мозжечковый синдром (атаксия при ходьбе с мозжечковой дизартрией, атаксия конечностей или мозжечковые глазодвигательные нарушения) и
по крайней мере, один признак вегетативной дисфункции не связанный с каким-либо другим заболеванием (ложные позывы на мочеиспускание, учащенное мочеиспускание или неполное опорожнение мочевого пузыря, эректильная дисфункция у мужчин или значительная ортостатическая гипотензия, которая не соответствует уровню, требуемому для критериев вероятной мультисистемной атрофии) и
по крайней мере, один дополнительный признак, указанный в части 3.
Слайд 17
Часть 3. Дополнительные признаки возможной мультисистемной атрофии.
Возможная
мультисистемная атрофия (паркинсоническая или мозжечковая форма):
положительный рефлекс Бабинского
с гиперрефлексией;
стридор.
Возможная мультисистемная атрофия (паркинсоническая форма):
быстро прогрессирующий паркинсонизм;
плохой терапевтический эффект леводопы;
постуральная неустойчивость, развившаяся в течение 3-х лет после начала двигательных симптомов заболевания;
атаксия при ходьбе, мозжечковая дизартрия, атаксия конечностей или мозжечковые глазодвигательные нарушения;
дисфагия, развившаяся в течение 5-и лет после начала двигательных симптомов заболевания;
атрофия скорлупы, средних ножек мозжечка, моста или мозжечка на МРТ;
гипометаболизм в скорлупе, стволе или мозжечке, выявленный при проведении ПЭТ с флюородеоксиглюкозой.
Слайд 18
Возможная мультисистемная атрофия (мозжечковая форма):
паркинсонизм (брадикинезия или
ригидность);
атрофия скорлупы, средних ножек мозжечка или моста на
МРТ;
гипометаболизм в скорлупе, выявленный при проведении ПЭТ с флюородеоксиглюкозой;
пресинаптическая нигростриальная допаминергическая денервация, выявленная с помощью SPECT и ПЭТ.
Слайд 19
Часть 4. Признаки, подтверждающие диагноз мультисистемной атрофии
и
признаки не характерные для мультисистемной атрофии.
Признаки, подтверждающие диагноз мультисистемной
атрофии:
орофациальная дистония;
диспропорциональный антероколлис;
каптокормия (выраженный наклон туловища вперед) и/или синдром Пизы (выраженный наклон туловища вбок);
контрактуры кистей рук или стоп;
дыхательные нарушения;
выраженная дисфония;
выраженная дизартрия;
недавно появившийся или усилившийся храп;
холодные ладони и стопы;
патологический смех или плач;
толчкообразный, миоклонический постуральный / кинетический тремор.
Слайд 20
Признаки не характерные для мультисистемной атрофии:
классический тремор
покоя по типу скатывания пилюль;
клинически значимая нейропатия;
не
индуцированные лекарствами галлюцинации;
начало заболевания после 75 лет;
наследственный анамнез атаксии или паркинсонизма;
деменция;
очаги поражения белого вещества, характерные для рассеянного склероза.
Слайд 21
лечение
Леводопа, агонисты дафаминовых рецепторов, амантадин
Лечение вегетативной недостаточности:
Ортостатической гипотензии:
повышенное потребление соли и жидкости, сон в положении полусидя,
медикаментозная терапия (флудрокортизон, эритропоэтин, нпвс)
Нарушения моторики ЖКТ: домперидон, лоперамид (мотилиум)
Нарушения мочеиспускания: празозин, амитриптиллин
Ночной полиурии: адиуретин
Нарушения эрекции: иохимбин, силденафил.
Слайд 22
Кортикобазальная дегенерация (КБД)
Нейродегенеративное заболевание, характеризующееся атрофией, глиозом и

тау-иммунореактивными патологическими изменениями в сером и белом веществе неокортекса,
базальных ганглиях и черной субстанции.
Встречается с частотой 0,45 на 100 тыс., средний возраст дебюта: 63 года
Патоморфологически при КБД поражаются нигростриарная система, таламус, субталамическое, красное и зубчатое ядра, лобная и теменная области коры. КБД относится к подтипу синуклеинопатий.
Специфическим проявлением кортикобазальной дегенерации является синдром ―чужой руки‖ (alien hand phenomenon), который наблюдается в 60% случаев этого заболевания. Синдром чужой руки‖ проявляется неспособностью осознавать и контролировать действия одной из рук, которая не подчиняется произвольному контролю. В то же время на пораженной руке сохраняется чувствительность.
Наиболее часто первым проявлением кортикобазальной дегенерации является неловкость в руке (50% случаев), нарушения ходьбы (36%), односторонняя болезненная парестезия (29%), лобная деменция (21%), падения (21%), дизартрия (14%), депрессия (7%).
Слайд 23
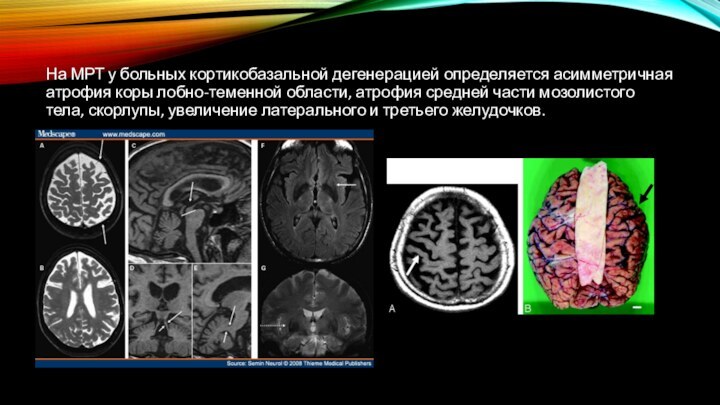
На МРТ у больных кортикобазальной дегенерацией определяется асимметричная
атрофия коры лобно-теменной области, атрофия средней части мозолистого тела,
скорлупы, увеличение латерального и третьего желудочков.
Слайд 24
Критерии для постановки диагноза КБД
1.Хроническое прогрессирующее течение
2.Асимметричное
начало (включая развитие афазии или апраксии)
3.Нарушение высших корковых функций:
А.
Идеомоторная апраксия ( нарушение выполнения смысловых действий, которое невозможно объяснить элементарными двигательными расстройствами)
Б. Нарушение ложны видов чувствительности ( при сохранности простых видов чувствительности и понимании больным задания)
В. Синдром «чужой» конечности
4.Наличие экстрапирамидных нарушений, в том числе акинетико-ригидного синдрома, резистентного к препаратам Л-дофы в сочетании с одним из следующих синдромов:
А. Дистония конечности с ее патологической установкой
Б. Спонтанная и рефлекторная фокальная миоклонии
Слайд 25
1. Начало с когнитивных нарушений ( иных, чем
афазия или апраксия)
2. Хорошая и стойкая реакция на препараты
Л-дофы
3. Тремор покоя.
4.Тяжелая вегетативная недостаточность.
5.Рано развивающегося пареза взора вниз
Критерии, исключающее диагноз КБД
Слайд 26
лечение
Симптоматическое. У некоторых больных дофаминергические средства уменьшают симптомы
паркинсонизма, но чаще эти препараты оказываются неэффективными.
Для уменьшения миоклонии
применяют клоназепам, при выраженном гипертоническом гиперкинезе возможно введение ботулотоксина.
Слайд 27
Деменция с тельцами Леви (ДТЛ)
Чаще страдают мужчины

65—70 лет
Морфологические признаки ДТЛ — преобладающие в коре лобной и
височной долей тельца Леви, представляющие собой цитоплазматические включения, состоящие из белков альфа-синуклеина и убиквитина, а также увеличение в размерах нейронов.
Характерным началом ДТЛ является триада синдромов: экстрапирамидные нарушения, деменция и галлюцинации .
Экстрапирамидный синдром при ДТЛ не имеет асимметрии, в отличие от болезни Паркинсона, и проявляется изолированной акинезией, а также выраженной постуральной неустойчивостью.
Когнитивные расстройства проявляются нарушением внимания, снижением интеллекта, потерей способности к обобщению, абстрагированию и умозаключению;
Для ДТЛ характерны зрительные галлюцинации, которые четко очерчены по цвету, форме, размерам, действию и объему. Типичное проявление ДТЛ — полное исчезновение галлюцинаций при попытке взаимодействия больного с вымышленным объектом .
К другим психическим расстройствам у больных деменцией с тельцами Леви относятся зрительные галлюцинации и галлюцинации в других модальностях (слуховые, тактильные), депрессия и различные нарушения сна (расстройства фазы быстрого сна, чрезмерная дневная сонливость и др.)
При ДТЛ нередко встречается ортостатическая гипотензия, которая проявляется липотимиями или обмороками при изменении положения тела.
ДТЛ отличается неуклонным прогрессированием. Cредняя продолжительность жизни таких больных с момента проявления первых признаков болезни — 5 лет.
Слайд 28
Диагностические критерии
Центральный признак
(необходим для постановки вероятного или
возможного диагноза деменции с тельцами Леви)
прогрессирующая деменция.
Основные
признаки
(для постановки вероятного диагноза необходимы два основных признака, для постановки возможного диагноза необходим один основной признак)
когнитивные флюктуации;
рецидивирующие зрительные галлюцинации;
паркинсонизм.
Наводящие признаки
(для постановки вероятного диагноза необходим один или более наводящий признак + один или более основной признак, для постановки возможного диаг-ноза необходим один или более наводящий признак, при отсутствии основных признаков)
поведенческие расстройства фазы быстрого сна;
выраженное повышение чувствительности к нейролептикам;
низкий уровень накопления транспортеров допамина в базальных ганглиях, выявленный с помощью SPECT или PET.
Слайд 29
Дополнительные признаки
(часто присутствуют, но не имеют диагностической
специфичности)
повторяющиеся падения и синкопальные состояния;
транзиторные потери сознания;
выраженные вегетативные нарушения, например, ортостатическая гипотензия, недержание мочи;
галлюцинации в других модальностях;
систематизированный бред и мании;
депрессия;
зрительно-пространственные расстройства;
относительная анатомическая сохранность структур височных долей полушарий головного мозга при исследовании с помощью КТ или МРТ;
генерализованное снижение перфузии на SPECT или ПЭТ со снижением окципитальной активности;
снижение поглощения метайодбензилгуанидина при проведении сцинтиграфии миокарда;
медленно-волновая активность на электроэнцефалограмме с присутствием острых волн в височных отведениях.
Слайд 30
Симптомы, наличие которых не характерно для деменции с
тельцами Леви
очаговые неврологические симптомы или нейровизуализационные изменения, вызванные
цереброваскулярной патологией;
присутствие сопутствующей патологии, искажающей клиническую картину заболевания;
в случае если паркинсонизм дебютирует у больного с выраженной деменцией.
Последовательность развития симптомов
Диагноз деменции с тельцами Леви следует устанавливать, когда деменция развилась до паркинсонизма, одновременно с паркинсонизмом или в течение первого года после появления симптомов паркинсонизма.
Золотым стандартом подтверждения диагноза деменции с тельцами Леви является патоморфологическое исследование после смерти больного, так как, несмотря на наличие клинических диагностических критериев этого заболевания вероятность диагностической ошибки при жизни больного очень высока, и большое количество случаев деменции с тельцами Леви не диагностируются при жизни
Слайд 31
лечение
Агонисты дофаминовых рецепторов часто провоцируют психотические расстройства
При психотических
расстройствах и эпизодах возбуждения следует отменить некоторые противопаркинсонические средства
(холинолитики, агонисты дофаминовых рецепторов), снизить дозу леводопы. При неэффективности: атипичные нейролептики (клозепин(левонекс),оланзапин),антисеротониновые средства (ондасетрон – зофран, 12-24 мг/сут)
Для уменьшения выраженности когнитивных нарушений: антихолинэстеразные средства (ривастигмин, донепезил, галантамин), предшественники ацетилхолина (холина альфосцерат)
Слайд 32
Синдром паркинсонизм-БАС-деменция, болезнь острова Гуам
Впервые описана у жителей острова

Гуам в Тихоокеанском бассейне, относится к таупатиям. Страдают преимущественно
мужчины 50 – 60 лет.
В качестве возможной причины развития заболевания предположено воздействие на местное население эндогенных и экзогенных факторов. К числу эндогенных факторов исследователи отнесли изолированность острова и, как следствие, частые кровнородственные браки, способствующие генным мутациям, а также преобладание среди населения острова лиц старше 55 лет. Экзогенные факторы, по их мнению, включали особенности питания местных жителей, которое было однообразным, с высоким уровнем жира, низким содержанием питательных веществ и минералов (кальция, магния) в питьевой воде и почве. В последующем изменение социоэкономических, этнографических и экологических условий населения острова Гуам привело к снижению числа этой патологии.
По данным P.A. Cox et al. [5], S.J. Murch et al. , одним из природных небелковых веществ, обладающих нейротоксическим действием, является betamethylaminoLalanin. Это вещество синтезируют цианобактерии, расположенные на кораллах, которыми, в свою очередь, питаются морские черепахи. Частое употребление местными жителями мяса черепах приводит к повышению его концентрации в тканях в 10–240 раз. Таким образом, в пищевой цепи на острове Гуам формируется эндогенный нейротоксический резервуар, оказывающий влияние на метаболизм белков, что способствует развитию заболевания.
Слайд 33
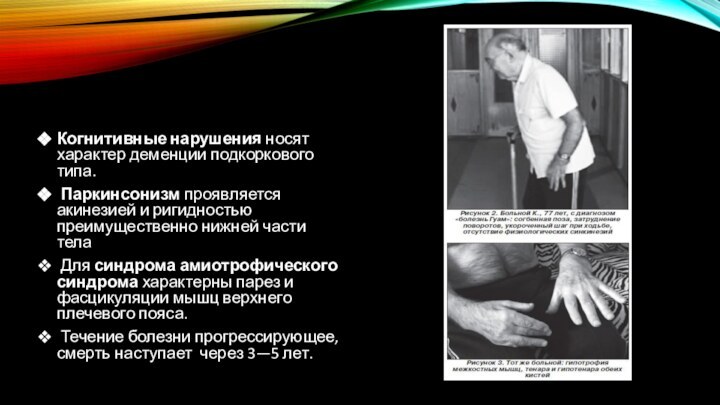
Когнитивные нарушения носят характер деменции подкоркового типа.
Паркинсонизм проявляется акинезией и ригидностью преимущественно нижней части тела
Для синдрома амиотрофического синдрома характерны парез и фасцикуляции мышц верхнего плечевого пояса.
Течение болезни прогрессирующее, смерть наступает через 3—5 лет.
Слайд 35
Лечение ндз
В настоящее время наиболее распространена симптоматическая терапия

нейродегенеративных заболеваний:
1. Средства, воздействующие на специфические нейромедиаторные системы мозга (реминил,
нейромидин, глиатилин). Указанные препараты являются центральными холиномиметиками, восполняют дефицит ацетилхолина в мозге за счет блокады холинэстеразы и приводят к увеличению продолжительности его действия на постсинаптические рецепторы, усиливая холинергическую передачу. Схожим механизмом действия обладают антиглутаматергические средства (мемантин), являющиеся неконкурентными селективными антагонистами NMDA-рецепторов. Благодаря модулированию глутаматэргической передачи улучшаются когнитивные процессы. В контролируемых исследованиях доказана эффективность препарата при всех видах деменции
2. Cредства с нейротрофическим действием (кортексин, церебролизин) способны повышать эффективность метаболических процессов в ткани мозга, снижать образование токсических свободных радикалов, стимулировать репаративные процессы.
3.Cредства с нейрометаболическим действием (актовегин, глицин, семакс, луцетам, пирацетам), стимулирующие обменные процессы в головном мозге, повышают устойчивость к гипоксии, усиливают холинергическую передачу, улучшают микроциркуляцию, блокируя агрегацию тромбоцитов.
Слайд 36
4. Коррекция экстрапирамидных нарушений при НДЗ возможна путем

назначения леводопасодержащих препаратов (мадопар, наком), дофаминовых агонистов (мирапекс, проноран)
или амантадинов (мидантан, ПК-Мерц). Эффективность препаратов леводопы при НДЗ, в отличие от болезни Паркинсона, не столь высока и, по данным W. Poewe, составляет 26%. В связи с этим назначение агонистов дофаминовых рецепторов и амантадинов представляется более предпочтительным, так как указанные средства не только повышают чувствительность постсинаптических рецепторов, но и обладают антиоксидантным эффектом .
5. В случае прогрессирующей вегетативной недостаточности, не поддающейся коррекции немедикаментозными способами, эффективны кортинефф или гутрон, назначаемые в утренние часы.
6. При повышении мышечного тонуса пирамидного типа назначают баклофен.
7. Психотические нарушения корригируются назначением атипичных нейролептиков (клозапид).
8. Коррекция тремора, мышечных дистоний или миоклоний возможна с помощью клоназепама, при неэффективности повторно можно ввести диспорт в заинтересованные мышцы.
9. При тяжелых формах дистонии прибегают к нейрохирургическому вмешательству — электрической стимуляции бледного шара, которая, по данным B. Biolsy et al., эффективна у 42% больных .