- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Органические вещества, входящие в состав клетки
Содержание
- 2. Углеводы, или сахариды, — органические вещества, в
- 4. моносахаридыМолекулы моносахаридов могут иметь вид прямолинейных цепочек
- 5. Свойства моносахаридов: низкая молекулярная масса; сладкий вкус; легко растворяются в воде; кристаллизуются
- 6. Дисахариды (олигосахариды) Наиболее широко распространены
- 7. Полисахариды Свойства полисахаридов:
- 8. Функции углеводов: Энергетическая. Одна из основных функций
- 9. Рибоза и дезоксирибоза входят в состав мономеров
- 10. Липиды Липиды — сборная
- 12. Простые липиды.Жиры. Жиры широко распространены в природе.
- 13. Функции липидов. Основная функция липидов —
- 14. Каталитическая. Эта функция связана с жирорастворимыми витаминами
- 15. Как устроен белок? Белки – это сложные высокомолекулярные природные соединения, построенные из аминокислот.
- 16. СТРОЕНИЕ АМИНОКИСЛОТВ аминокислотах выделяют три функциональные группы:1.Аминогруппа 2.Карбоксильная группа3.Радикал ( они разные у всех аминокислот)
- 17. В состав белков входит 20 различных аминокислот
- 18. ПЕПТИДНАЯ СВЯЗЬПептидная связь — вид амидной связи, возникающей
- 19. Свойства.Размер белка может измеряться количеством аминокислот Самый
- 20. Денатурация. Резкое изменение условий, например, нагревание
- 22. Б Е Л К ИПростыеСостоят только из
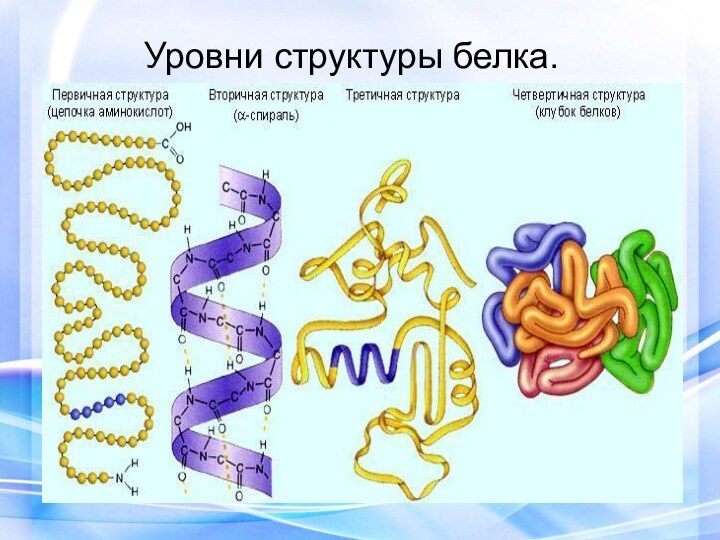
- 23. Уровни структуры белка.
- 24. Первичная структура — последовательность аминокислот
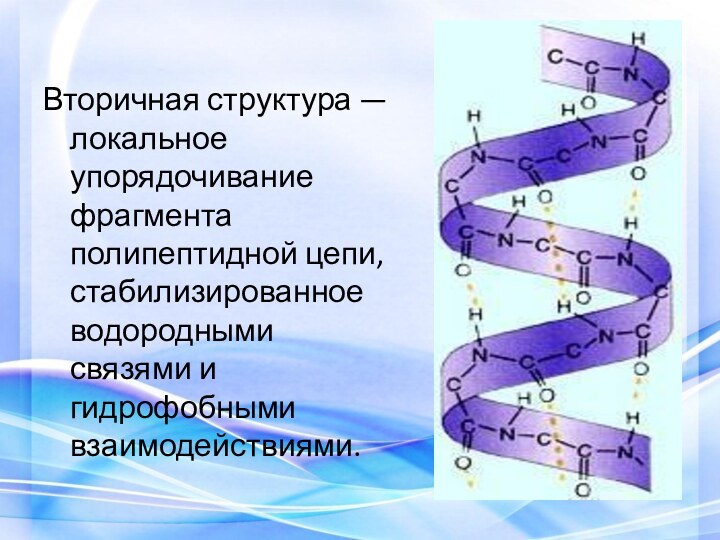
- 25. Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями и гидрофобными взаимодействиями.
- 26. Третичная структура — пространственное строение
- 27. Четверичная структура — субъединичная структура белка.
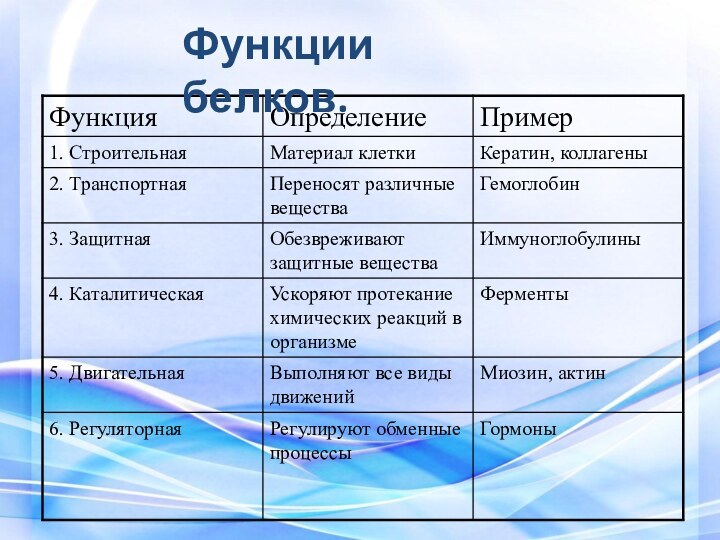
- 28. Функции белков.
- 29. Нуклеиновые кислоты природные высокомолекулярные органические соединения, обеспечивающие хранение
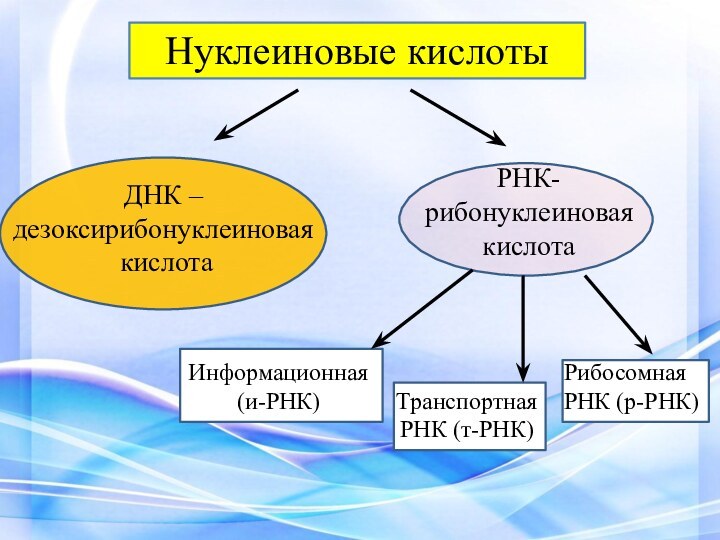
- 30. Нуклеиновые кислотыДНК – дезоксирибонуклеиновая кислотаРНК- рибонуклеиновая кислотаИнформационная(и-РНК)ТранспортнаяРНК (т-РНК)Рибосомная РНК (р-РНК)
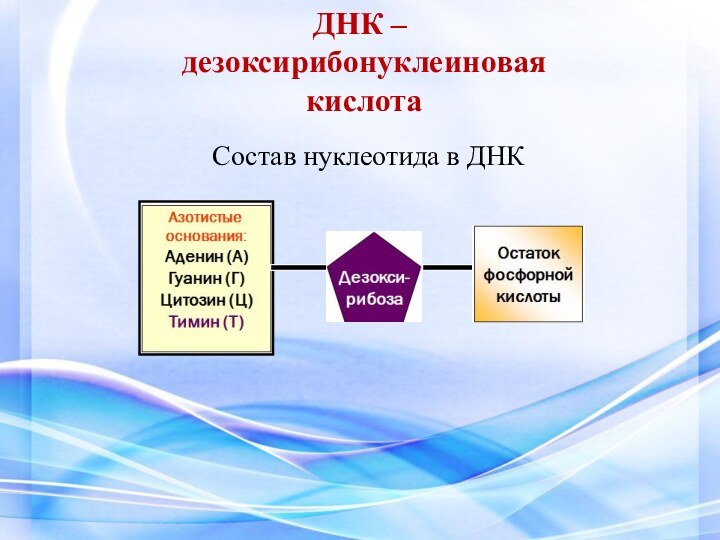
- 31. ДНК – дезоксирибонуклеиновая кислотаСостав нуклеотида в ДНК
- 32. Правило ЧаргаффаСодержание А=Т Содержание Г= ЦКомплиментарность -
- 33. Модель ДНК1953 г. – создание модели ДНК
- 37. РНК- рибонуклеиновая кислотаСостав нуклеотида в РНКРНК – это одноцепочечная молекула
- 38. Скачать презентацию
- 39. Похожие презентации
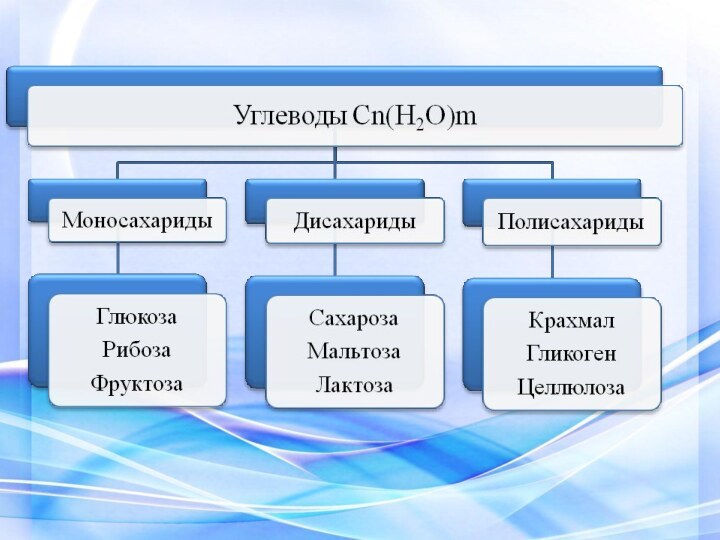
Углеводы, или сахариды, — органические вещества, в состав которых входит углерод, кислород, водород. Химический состав углеводов характеризуется их общей формулой Сm(Н2О)n, где m≥n. Количество атомов водорода в молекулах углеводов, как правило, в два раза больше






















Слайд 2 Углеводы, или сахариды, — органические вещества, в состав
которых входит углерод, кислород, водород.
характеризуется их общей формулой Сm(Н2О)n, где m≥n. Количество атомов водорода в молекулах углеводов, как правило, в два раза больше атомов кислорода (то есть как в молекуле воды). Отсюда и название — углеводы. В живых клетка их содержание 1-5%, в некоторых клетках может достигать 90%
Слайд 4
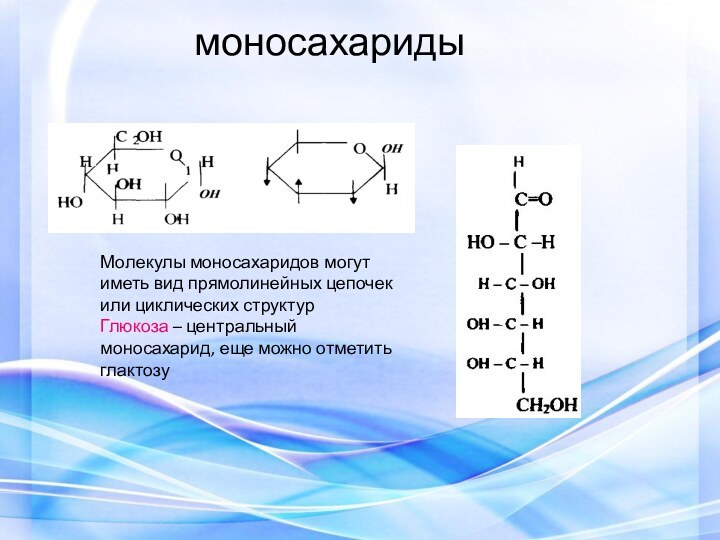
моносахариды
Молекулы моносахаридов могут иметь вид прямолинейных цепочек или
циклических структур
Глюкоза – центральный моносахарид, еще можно отметить глактозу
Слайд 5 Свойства моносахаридов: низкая молекулярная
масса; сладкий вкус; легко растворяются в воде; кристаллизуются
Слайд 6
Дисахариды (олигосахариды)
Наиболее широко распространены в
природе дисахариды:
Мальтоза- солодовый сахар, состоящая из двух остатков α-глюкозы;
лактоза
– молочный сахар (α-глюкоза + галактоза);сахароза – свекловичный сахар (α-глюкоза + фруктоза).
По своим свойств сходны с моносахарами
Слайд 7
Полисахариды
Свойства полисахаридов:
большая молекулярная масса (обычно сотни тысяч); не дают ясно
оформленных кристаллов; либо нерастворимы в воде, либо образуют растворы, напоминающие по свойствам коллоидные; сладкий вкус не характерен;
Слайд 8
Функции углеводов:
Энергетическая. Одна из основных функций углеводов. Углеводы
— основные источники энергии в животном организме. При расщеплении
1 г углевода выделяется 17,6 кДж.С6Н12О6 + О2 = 6СО2 + 6Н2О + 17,6 кДж
Запасающая. Выражается в накоплении крахмала клетками растений и гликогена клетками животных.
Опорно-строительная. Углеводы входят в состав клеточных мембран и клеточных стенок (гликокаликс, целлюлоза, хитин, муреин). Соединяясь с липидами и белками, образуют гликолипиды и гликопротеины.
Слайд 9 Рибоза и дезоксирибоза входят в состав мономеров нуклеотидов
ДНК, РНК и АТФ.
Рецепторная. Олигосахаридные фрагменты гликопротеинов и гликолипидов
клеточных стенок выполняют рецепторную функцию.6. Защитная. Слизи, выделяемые различными железами, богаты углеводами и их производными (например, гликопротеинами). Они предохраняют пищевод, кишечник, желудок, бронхи от механических повреждений, препятствуют проникновению в организм бактерий и вирусов.
Слайд 10
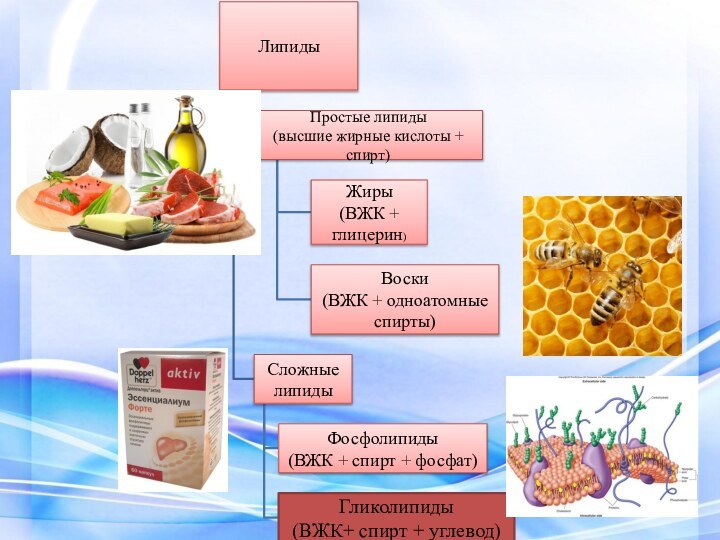
Липиды
Липиды — сборная
группа органических соединений, не имеющих единой химической характеристики. Их
объединяет то, что все они являются производными высших жирных кислот, нерастворимы в воде, но хорошо растворимы в органических растворителях (эфире, хлороформе, бензине).
Слайд 12
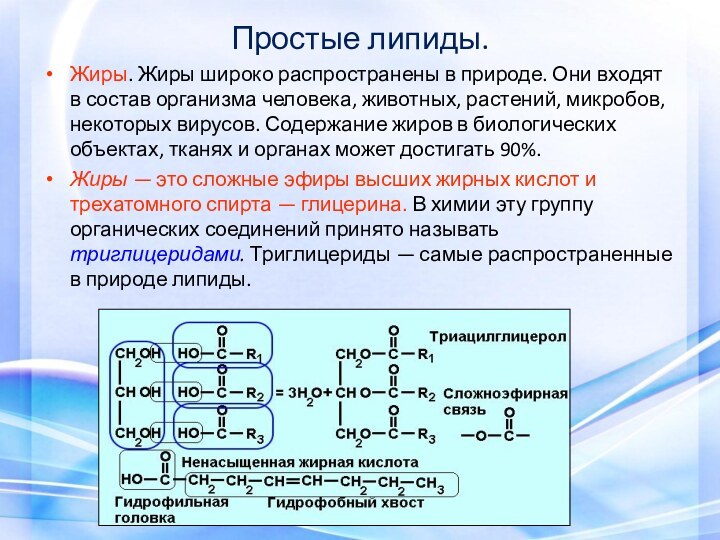
Простые липиды.
Жиры. Жиры широко распространены в природе. Они
входят в состав организма человека, животных, растений, микробов, некоторых
вирусов. Содержание жиров в биологических объектах, тканях и органах может достигать 90%.Жиры — это сложные эфиры высших жирных кислот и трехатомного спирта — глицерина. В химии эту группу органических соединений принято называть триглицеридами. Триглицериды — самые распространенные в природе липиды.
Слайд 13
Функции липидов.
Основная функция липидов — энергетическая. Калорийность
липидов выше, чем у углеводов. В ходе расщепления 1
г жиров до СО2 и Н2О освобождается 38,9 кДж.Структурная. Липиды принимают участие в образовании клеточных мембран. В составе мембран находятся фосфолипиды, гликолипиды, липопротеины.
Запасающая. Это особенно важно для животных, впадающих в холодное время года в спячку или совершающих длительные переходы через местность, где нет источников питания. Семена многих растений содержат жир, необходимый для обеспечения энергией развивающееся растение.
Терморегуляторная. Жиры являются хорошими термоизоляторами вследствие плохой теплопроводимости. Они откладываются под кожей, образуя у некоторых животных толстые прослойки. Например, у китов слой подкожного жира достигает толщины 1 м.
Защитно-механическая. Скапливаясь в подкожном слое, жиры защищают организм от механических воздействий.
Слайд 14 Каталитическая. Эта функция связана с жирорастворимыми витаминами (А,
D, E, K). Сами по себе витамины не обладают
каталитической активностью. Но они являются коферментами, без них ферменты не могут выполнять свои функции.Источник метаболический воды. Одним из продуктов окисления жиров является вода. Эта метаболическая вода очень важна для обитателей пустынь. Так, жир, которым заполнен горб верблюда, служит в первую очередь не источником энергии, а источником воды (при окислении 1 кг жира выделяется 1,1 кг воды).
Повышение плавучести. Запасы жира повышают плавучесть водных животных.
Слайд 15
Как устроен белок?
Белки –
это
сложные высокомолекулярные природные соединения, построенные из аминокислот.
Слайд 16
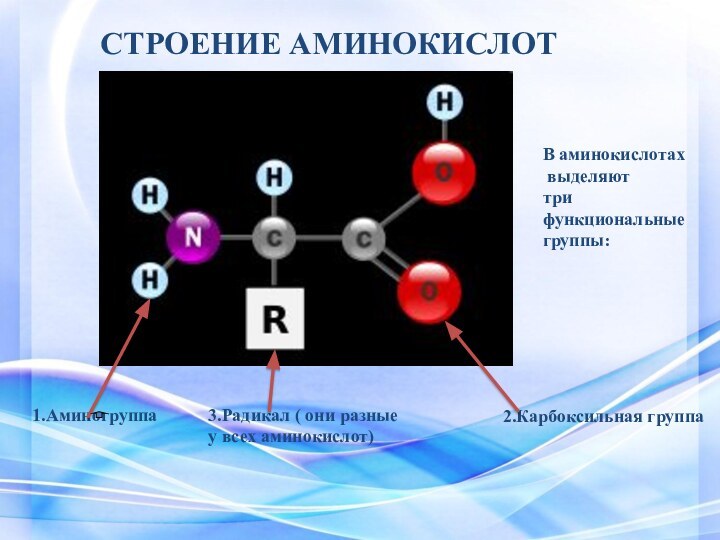
СТРОЕНИЕ АМИНОКИСЛОТ
В аминокислотах
выделяют
три функциональные
группы:
1.Аминогруппа
2.Карбоксильная
группа
3.Радикал ( они разные
у всех аминокислот)
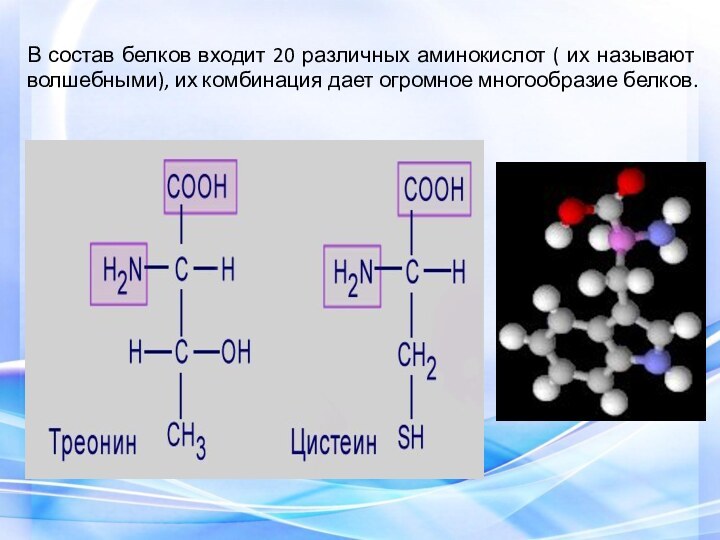
Слайд 17 В состав белков входит 20 различных аминокислот (
их называют волшебными), их комбинация дает огромное многообразие белков.
Слайд 18
ПЕПТИДНАЯ СВЯЗЬ
Пептидная связь — вид амидной связи,
возникающей при
образовании белков в результате взаимодействия α-аминогруппы (—NH2) одной аминокислоты
с α-карбоксильной группой (—СООН)другой аминокислоты.
Слайд 19
Свойства.
Размер белка может измеряться количеством аминокислот Самый большой
из известных в настоящее время белков — титин. Это
крупный эластичный белок, соединяющий миозин с линией Z .Сравнительный размер белков. Слева направо: Антитело, гемоглобин, инсулин, аденилаткиназа и глютаминсинтетаза.
Слайд 20
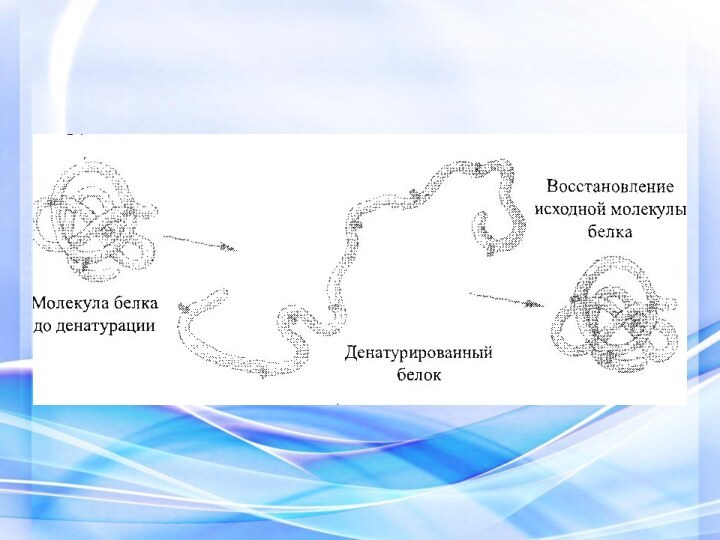
Денатурация.
Резкое изменение условий, например, нагревание или
обработка белка кислотой или щёлочью приводит к потере четвертичной,
третичной и вторичной структур белка, называемой денатурацией. Самый известный случай денатурации белка в быту — это приготовление куриного яйцаОБРАТИМАЯ
Если сохранена
первичная структура
НЕОБРАТИМАЯ
Если первичная
Структура разрушена
Слайд 22
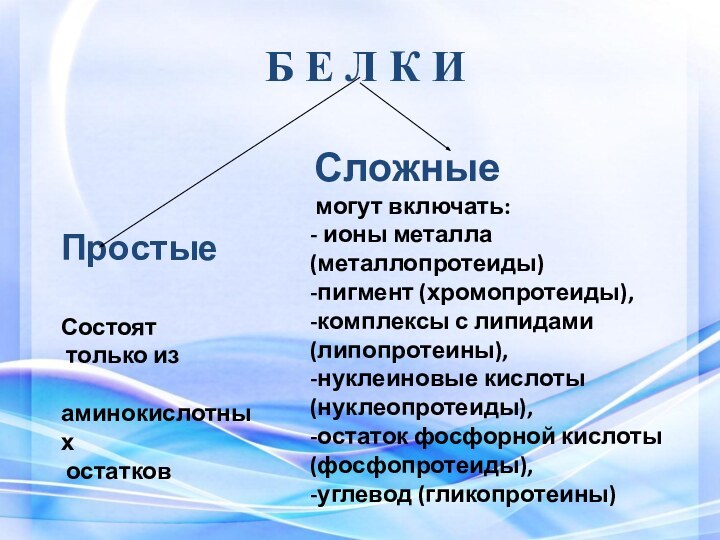
Б Е Л К И
Простые
Состоят
только из
аминокислотных
остатков
Сложные
могут включать:
- ионы металла (металлопротеиды)
-пигмент (хромопротеиды),
-комплексы с липидами (липопротеины),
-нуклеиновые кислоты(нуклеопротеиды),
-остаток фосфорной кислоты (фосфопротеиды),
-углевод (гликопротеины)
Слайд 24
Первичная структура — последовательность аминокислот в
полипептидной цепи.
Определяется и соответствует последовательности нуклеотидов в молекуле
ДНК
Слайд 25
Вторичная структура — локальное упорядочивание фрагмента полипептидной
цепи, стабилизированное водородными связями и гидрофобными взаимодействиями.
Слайд 26 Третичная структура — пространственное строение полипептидной
цепи — взаимное расположение элементов вторичной структуры, стабилизированное взаимодействием
между боковыми цепями аминокислотных остатков. В стабилизации третичной структуры принимают участие: ковалентные связи; ионные взаимодействия; водородные связи; гидрофобные взаимодействия.Слайд 27 Четверичная структура — субъединичная структура белка. Взаимное
расположение нескольких полипептидных цепей в составе единого белкового комплекса.
Слайд 29
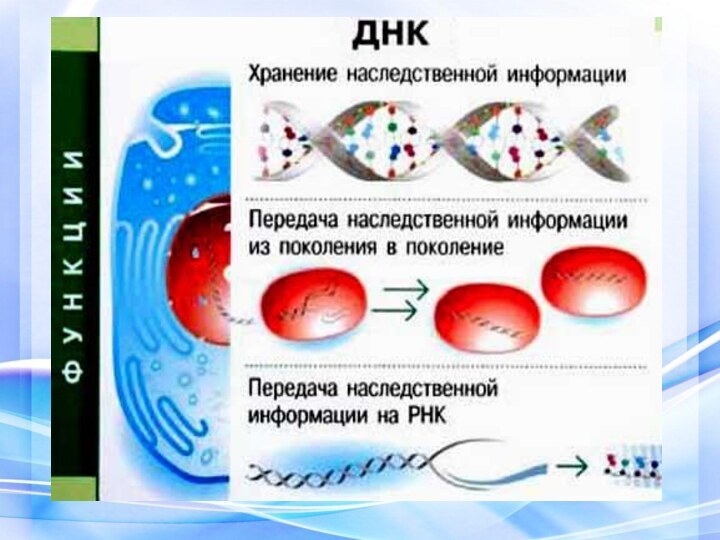
Нуклеиновые кислоты
природные высокомолекулярные органические соединения, обеспечивающие хранение и
передачу наследственной информации в живых организмах.
Открыты в 1869
году швейцарским биохимиком Фридрихом МишеромВпервые обнаружены в ядре («нуклеус» - ядро)
Слайд 30
Нуклеиновые кислоты
ДНК – дезоксирибонуклеиновая
кислота
РНК-
рибонуклеиновая
кислота
Информационная
(и-РНК)
Транспортная
РНК (т-РНК)
Рибосомная
РНК (р-РНК)
Слайд 32
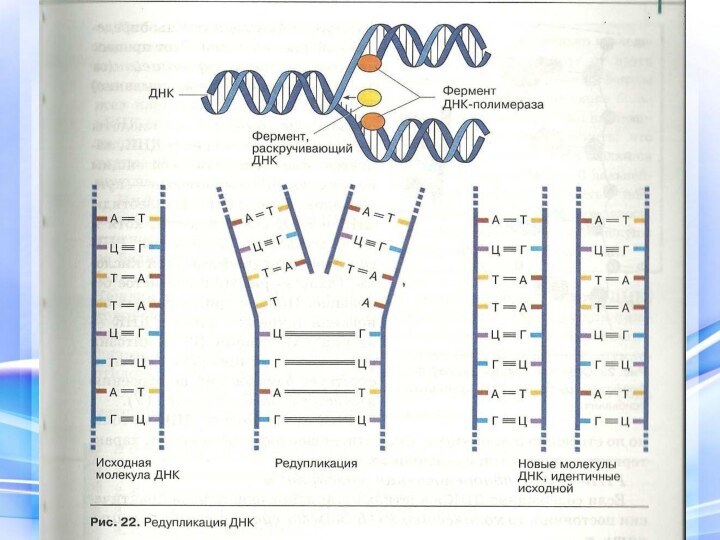
Правило Чаргаффа
Содержание А=Т
Содержание Г= Ц
Комплиментарность - это
взаимное дополнение азотистых оснований в молекуле ДНК.
Комплиментарные структуры
подходят
друг к другу как«ключ с замком»