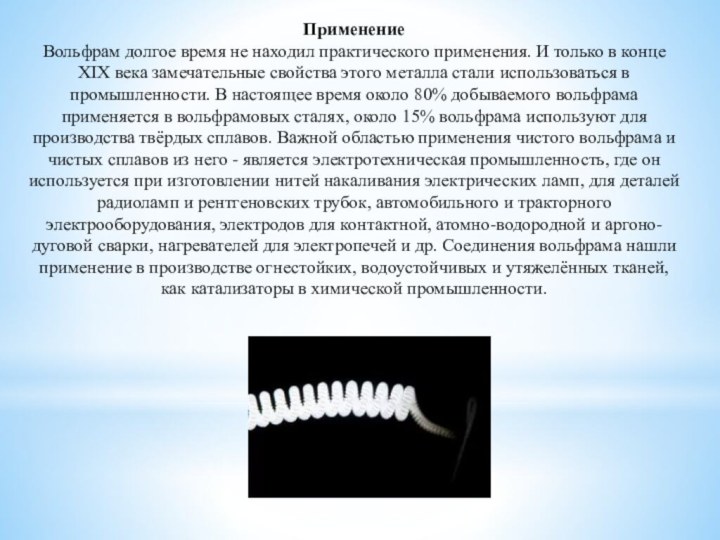
в Периодической системе химических элементов Д. И. Менделеева, обозначается
символом W (лат. Wolframium). При нормальных условиях представляет собой твёрдый блестящий серебристо-серый переходный металл.Вольфрам — самый тугоплавкий из металлов. Более высокую температуру плавления имеет только неметаллический элемент — углерод. При стандартных условиях химически стоек.