- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Относительная атомная и молекулярная масса.
Содержание
- 2. Атомно- молекулярное учение
- 3. этапы исторического развития XVII - XVIIIв.в.
- 4. Представление о том, что материя состоит из отдельных частиц
- 5. Основные положения АМУВещества состоят из атомов и
- 6. АТОМНАЯ ЕДИНИЦА МАССЫ≈ 10-10мma≈10-27÷10-25кгАБСОЛЮТНАЯma(H)=1,67375*10-27кгАБСОЛЮТНАЯma(C)=1,9927*10-26кгАБСОЛЮТНАЯma(O)=2,656812*10-26кгАБСОЛЮТНАЯ1 а.е.м.1/12 ma(C)а.е.м. -
- 7. Относительная атомная массаAr(Э)=«relativ»относительныйЕё получают при сравнении масс
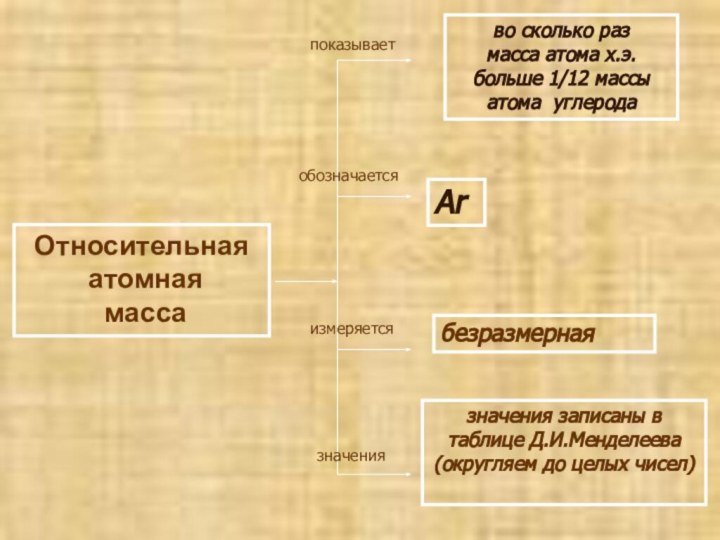
- 9. Относительная атомная массапоказываетобозначаетсяизмеряетсязначенияво сколько раз масса атома
- 10. Скачать презентацию
- 11. Похожие презентации
Атомно- молекулярное учение









Слайд 5
Основные положения АМУ
Вещества состоят из атомов и молекул
Молекулы
в химических реакциях разрушаются
Атомы в химических реакциях сохраняются
Атомы разных
химических элементов отличаются друг от друга размером, массой и другими свойствамиМолекулы и атомы находятся в непрерывном движении
Между молекулами имеются промежутки, размеры которых зависят от агрегатного состояния вещества
Слайд 6
АТОМНАЯ ЕДИНИЦА МАССЫ
≈ 10-10м
ma≈10-27÷10-25кг
АБСОЛЮТНАЯ
ma(H)=1,67375*10-27кг
АБСОЛЮТНАЯ
ma(C)=1,9927*10-26кг
АБСОЛЮТНАЯ
ma(O)=2,656812*10-26кг
АБСОЛЮТНАЯ
1 а.е.м.
1/12 ma(C)
а.е.м.
- это 1/12
массы атома углерода, масса которого равна 12 а.е.м.
1 а.е.м.
= =
=
1,66 * 10-27 кг
1 а.е.м. =
Слайд 7
Относительная атомная масса
Ar(Э)=
«relativ»
относительный
Её получают
при сравнении масс атомов
разных хмических элементов с 1 а.е.м.
безразмерная
Ar
элемента показывает во
сколько раз масса его атома больше 1/12 массы атома углеродаm(He)= 4 а.е.м.
Ar(He)=4