- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Материалы для ученика: Кристаллическая решетка
Содержание
- 2. Введение: Кристалл – это твердое вещество,
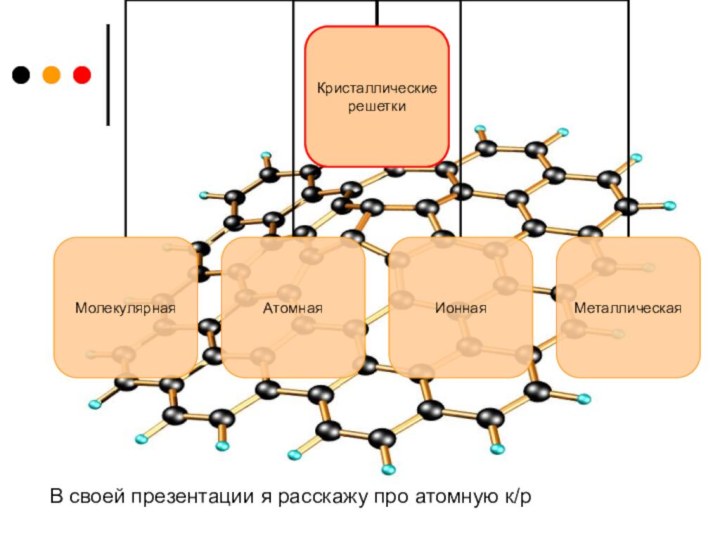
- 3. Кристаллическая решетка- …- это «пространственный каркас», который образуется при мысленном соединении узлов прямыми линиями.
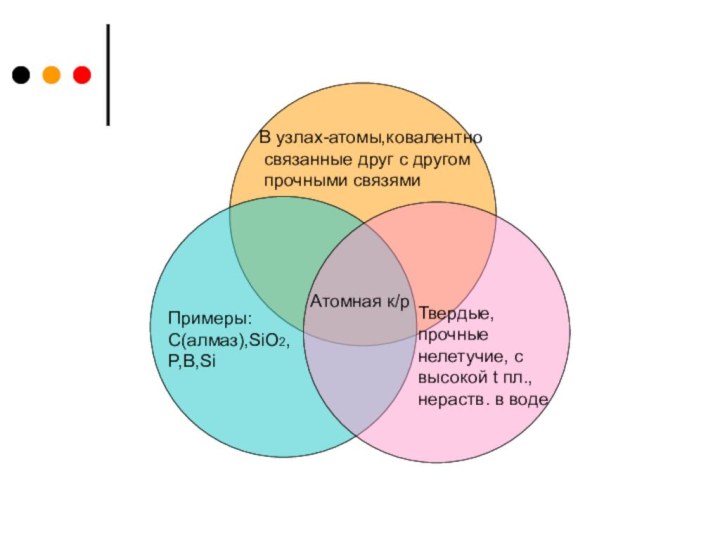
- 4. В своей презентации я расскажу про атомную к/р
- 6. Si, Кремний Кристаллическая решетка кремния
- 7. SiO2, «кварцевый песок»Имеет атомную кристаллическую решетку. SiO2
- 8. C, алмазКристаллическая решетка — кубическая гранецентрированная Каждый атом
- 9. Р, фосфорКрасный фосфор имеет атомную кристаллическую решетку с довольно сложным строением
- 10. ВыводСуществует огромное количество кристаллических структур. Их объединяет
- 11. Скачать презентацию
- 12. Похожие презентации
Введение: Кристалл – это твердое вещество, имеющее определенное упорядоченное строение. Частицы, из которых состоит кристалл, располагаются в определенном порядке, образуя кристаллическую решетку.








Слайд 3
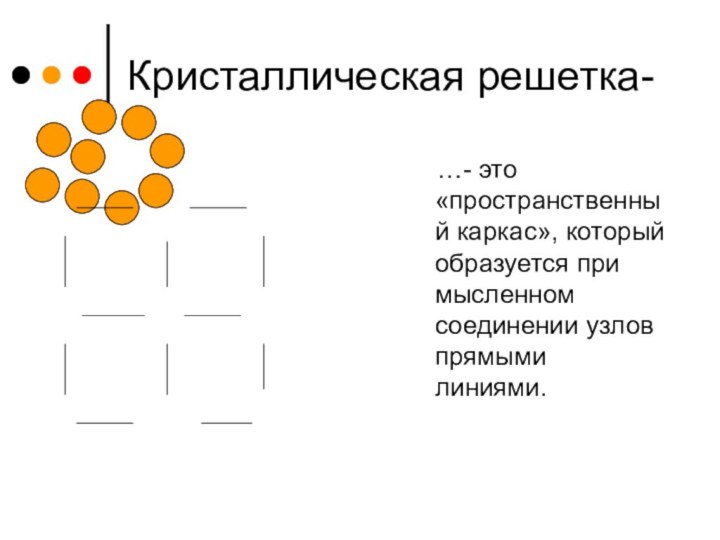
Кристаллическая решетка-
…- это «пространственный каркас», который
образуется при мысленном соединении узлов прямыми линиями.
Слайд 6
Si, Кремний
Кристаллическая решетка кремния кубическая
, как у алмаза, но из-за большей длины связи
между атомами Si—Si по сравнению с длиной связи С—С твердость кремния значительно меньше, чем алмаза. Кремний хрупок, только при нагревании выше 800 °C он становится пластичным веществом
Слайд 7
SiO2, «кварцевый песок»
Имеет атомную кристаллическую решетку.
SiO2 относится
к группе стеклообразующих оксидов, то есть склонен к образованию
переохлажденного расплава — стекла.
Слайд 8
C, алмаз
Кристаллическая решетка — кубическая гранецентрированная
Каждый атом углерода
в структуре алмаза расположен в центре тетраэдра, вершинами которого
служат четыре ближайших атома. Именно прочная связь атомов углерода объясняет высокую твёрдость алмаза.
Слайд 10
Вывод
Существует огромное количество кристаллических структур. Их объединяет главное
свойство кристаллического состояния вещества — закономерное положение атомов в кристаллической
решётке. Одно и то же вещество может кристаллизоваться в разных кристаллических решётках и обладать весьма различными свойствами (классический пример графит — алмаз).Атомная к/р присуща считанным веществам