Слайд 2
Цель урока : изучение класса органических соединений - алканов.
Слайд 3
Задачи:
Сформулировать знания учащихся о пространственном строении алканов.
Дать понятия
о гомологах, ознакомить с правилами составления названий орг. соединений
по систематической номенклатуре углеводородов.
Рассмотреть химические и физические свойства алканов, показать взаимосвязь между строением и свойствами.
Познакомить с основными областями применения насыщенных углеводородов.
Продолжить формирование умений анализировать, сравнивать, делать выводы; развить навыки культуры общения.
Воспитывать экологически образованную личность и ответственное отношение к учебе.
Слайд 4
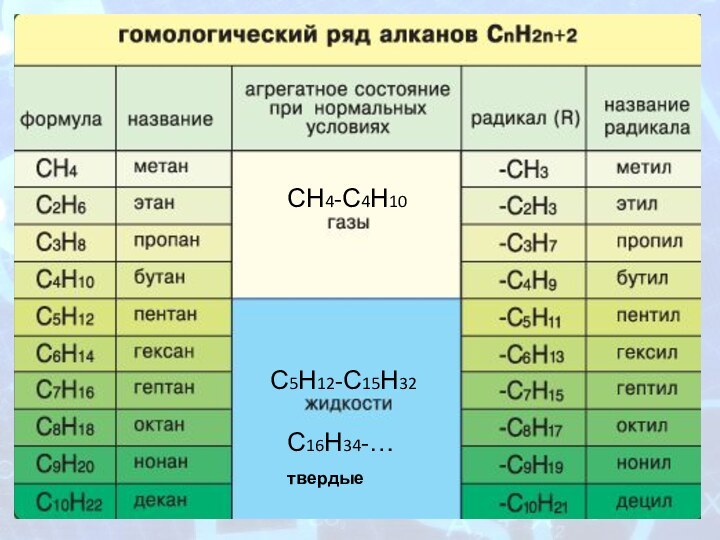
ГОМОЛОГИЧЕСКИЙ РЯД АЛКАНОВ
Вспомните, какие вещества мы называем гомологами?
ГОМОЛОГИ
–
это вещества со схожими
строением и свойствами,
но различающиеся
по составу
на одну или несколько
групп CH2 (гомологическая разность).
Слайд 5
СН4-С4Н10
С5Н12-С15Н32
С16Н34-…
твердые
Слайд 7
Алканы (предельные, насыщенные, парафины) – органические вещества, состоящие
из атомов углерода и водорода, связанных между собой одинарными
(сигма) связями.
Слайд 8
АЛКАНЫ
название предельных углеводородов
по международной номенклатуре (ИЮПАК).
ПАРАФИНЫ
исторически сохранившееся
название предельных углеводородов (от лат. parrum affinis – малоактивный).
Слайд 10
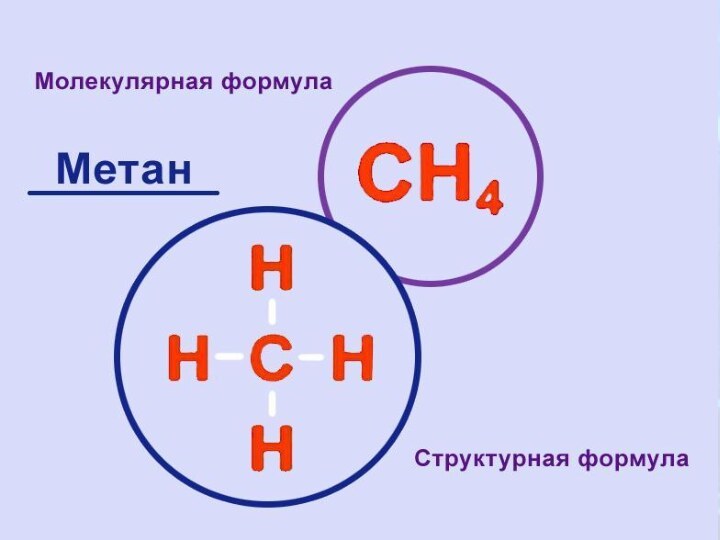
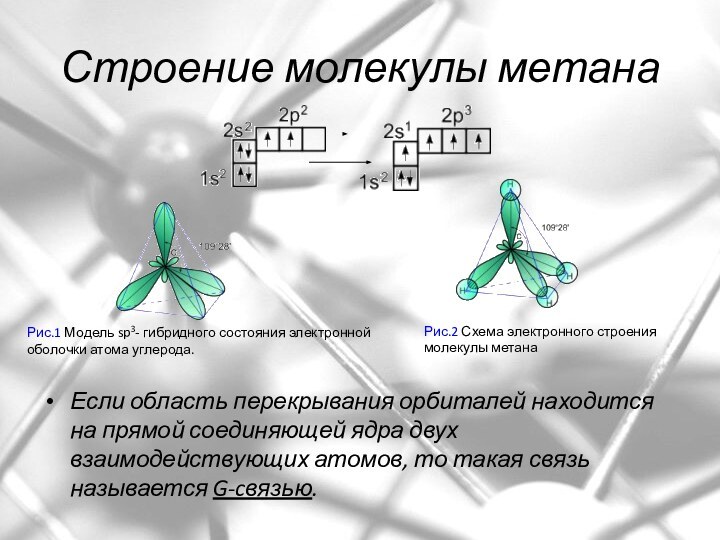
Строение молекулы метана
Если область перекрывания орбиталей находится на
прямой соединяющей ядра двух взаимодействующих атомов, то такая связь
называется G-cвязью.
Рис.1 Модель sp3- гибридного состояния электронной оболочки атома углерода.
Рис.2 Схема электронного строения молекулы метана
Слайд 11
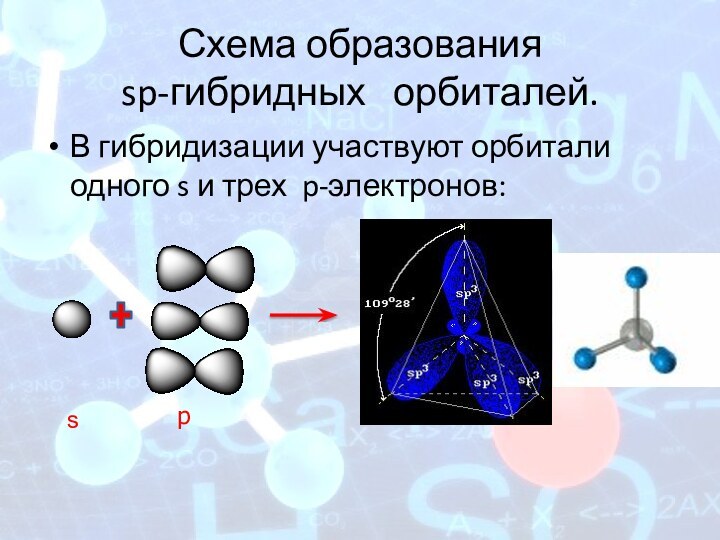
Схема образования
sp-гибридных орбиталей.
В гибридизации участвуют орбитали
одного s и трех p-электронов:
s
p
Слайд 12
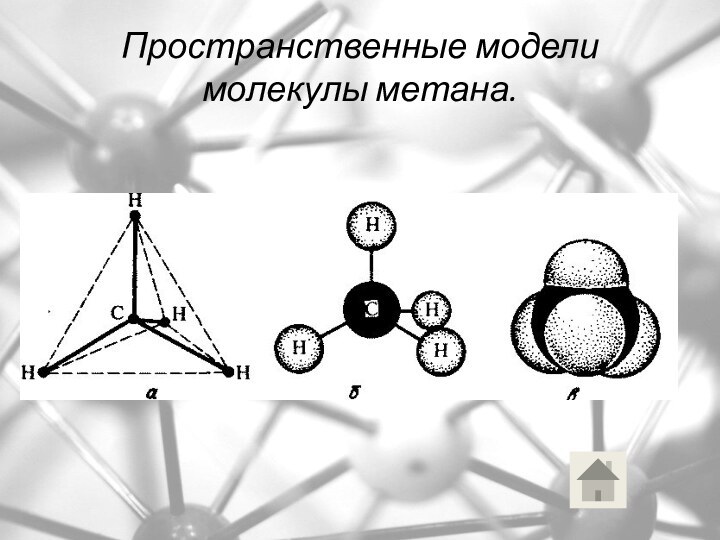
Пространственные модели
молекулы метана.
Слайд 13
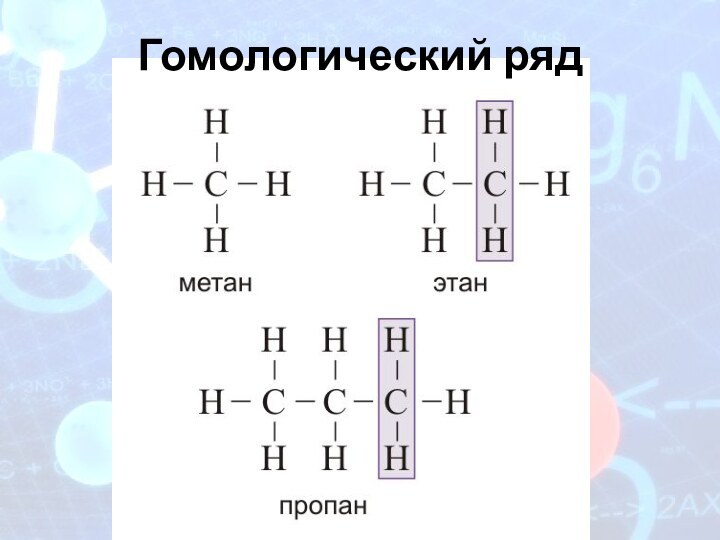
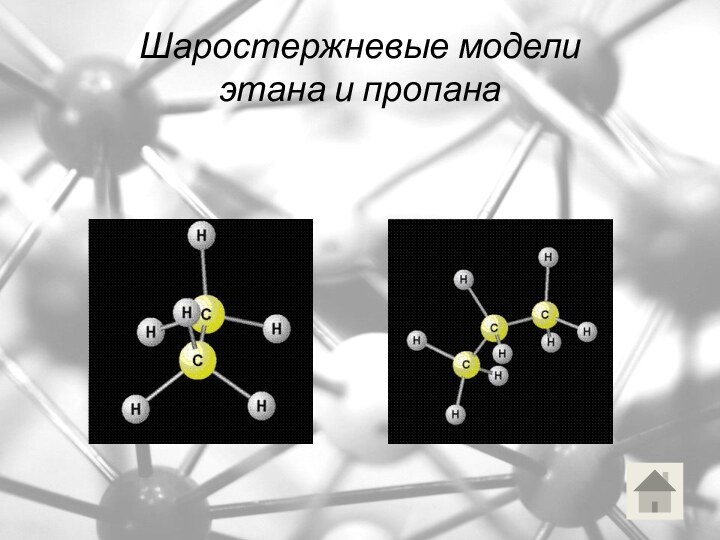
Шаростержневые модели
этана и пропана
Слайд 14
2
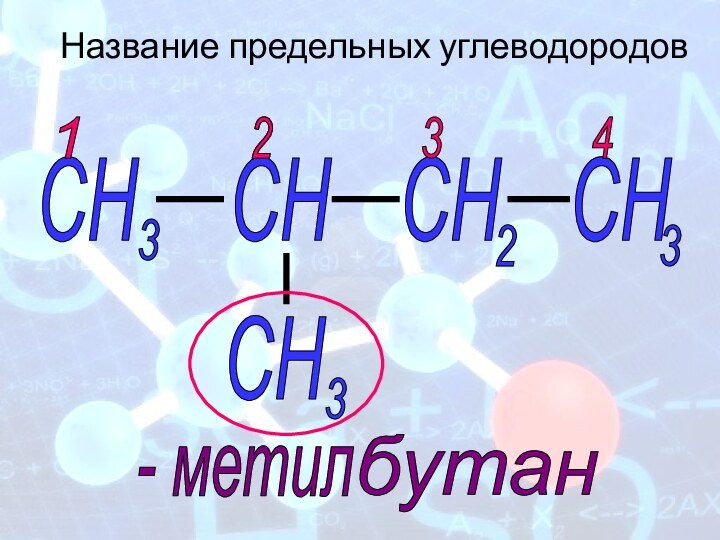
Название предельных углеводородов
СН
3
СН
СН
СН
СН
3
2
3
1
2
3
4
бутан
- метил
Слайд 15
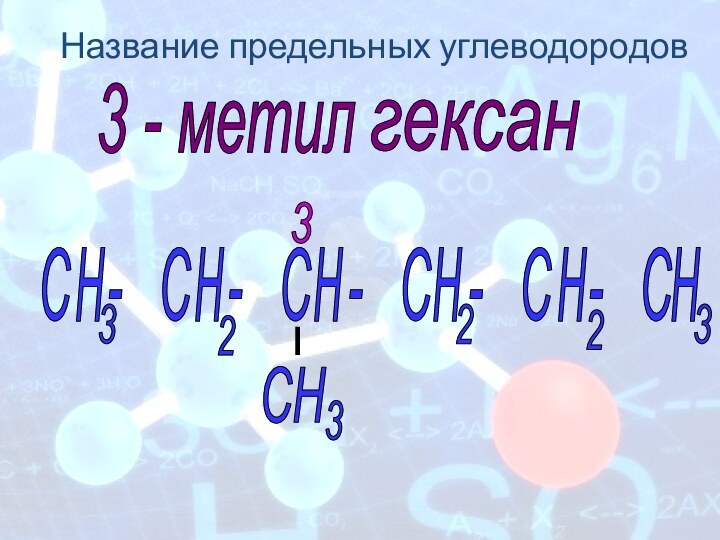
Название предельных углеводородов
3 - метил
гексан
С -
С - С - С
- С - С
3
СН
3
Н
Н
Н
Н
Н
Н
3
3
2
2
2
Слайд 16
Изомеры - это вещества имеющие
одинаковый качественный и
количественный
состав,
но отличаются по своему строению и свойствам.
Слайд 17
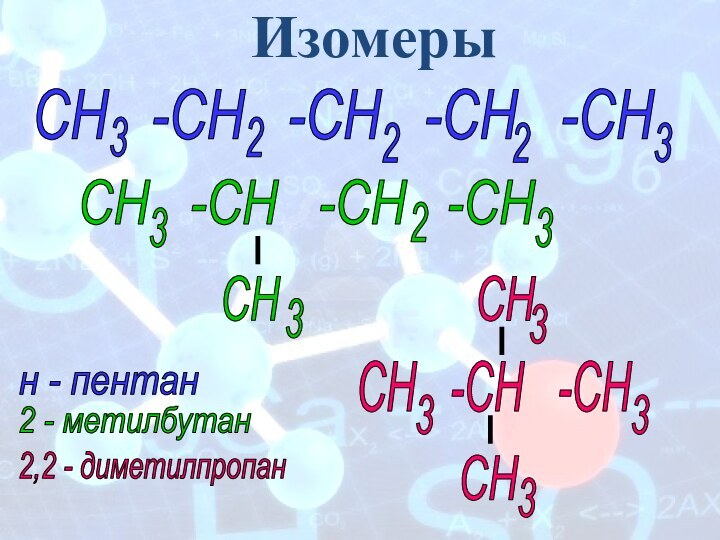
Изомеры
СН -СН -СН -СН
-СН
3
3
2
2
2
СН -СН -СН -СН
3
3
2
СН
3
СН -СН
-СН
СН
3
СН
3
3
3
н - пентан
2 - метилбутан
2,2 - диметилпропан
Слайд 18
Физические Свойства
С1 -С4 - газы,
С5 - С15 -
жидкости,
С16 - ... - твердые вещества.
Нерастворимы в воде,
в органических
растворителях
растворяются.
Слайд 19
Нахождение в природе:
Природный газ на 75%-85% состоит из
метана, от 25%-2% этана, пропана и других соединений.
Нефть и
ископаемый уголь (содержат не чистые углеводороды)
Месторождения угля (бурого), нефти, газа на Дальнем Востоке
Слайд 20
ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ. НАХОЖДЕНИЕ В ПРИРОДЕ.
МЕТАН – газ,
без цвета и запаха, почти в 2 раза легче
воздуха, мало растворим в воде. Он образуется в природе в результате разложения без доступа воздуха остатков растительных и животных организмов. Поэтому может быть обнаружен в заболоченных водоемах, где появляется в виде пузырьков газа, или накапливается в каменноугольных шахтах, куда выделяется из угольных пластов. В значительном количестве (80-97%) метан содержится в природном газе и в попутных нефтяных газах.
Слайд 21
НАХОЖДЕНИЕ АЛКАНОВ В ПРИРОДЕ.
МЕТАН образуется в природе
в результате разложения без доступа воздуха остатков растительных и
животных организмов. Поэтому может быть обнаружен в заболоченных водоемах, где появляется в виде пузырьков газа, или накапливается в каменноугольных шахтах, куда выделяется из угольных пластов. В значительном количестве (80–97 %) метан содержится в природном газе и в попутных нефтяных газах. В космосе метан является основной частью атмосфер многих планет, например Сатурна.
Слайд 22
ЭТАН, ПРОПАН И БУТАН входят в состав природного
и попутного нефтяного газов.
ЖИДКИЕ АЛКАНЫ содержатся в нефти.
Слайд 24
Как алканы
влияют на климат?
Метан
считается одним из парниковых газов и остается предметом активных
обсуждений и исследований в связи с проблемами глобального изменения климата.
Какие птицы
помогали шахтёрам?
Канарейки очень чувствительны к содержанию в воздухе метана. Эту особенность использовали в своё время шахтёры, которые, спускаясь под землю, брали с собой клетку с канарейкой. Если пения давно не было слышно, значит, следовало
подниматься наверх
как можно
быстрее.
Удивительное
рядом!
Слайд 25
Тест по теме «Алканы»
Готовимся к ОГЭ!
Слайд 26
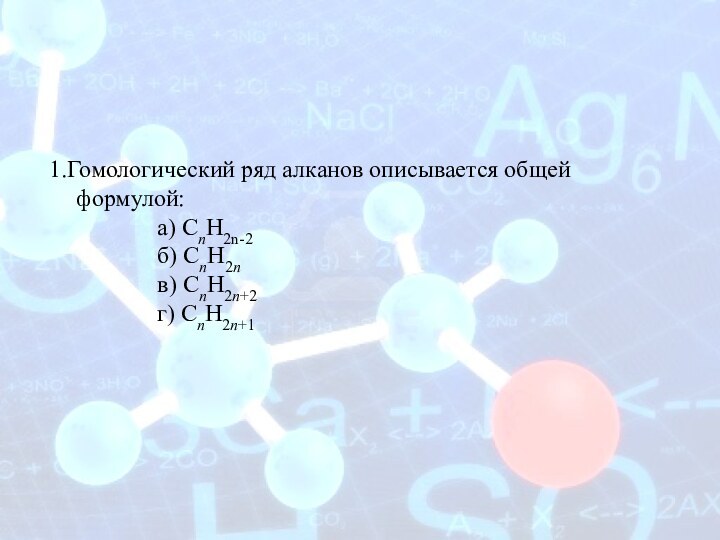
1.Гомологический ряд алканов описывается общей формулой:
а) СnH2n-2
б) CnH2n
в)
СnH2n+2
г) CnH2n+1
Слайд 27
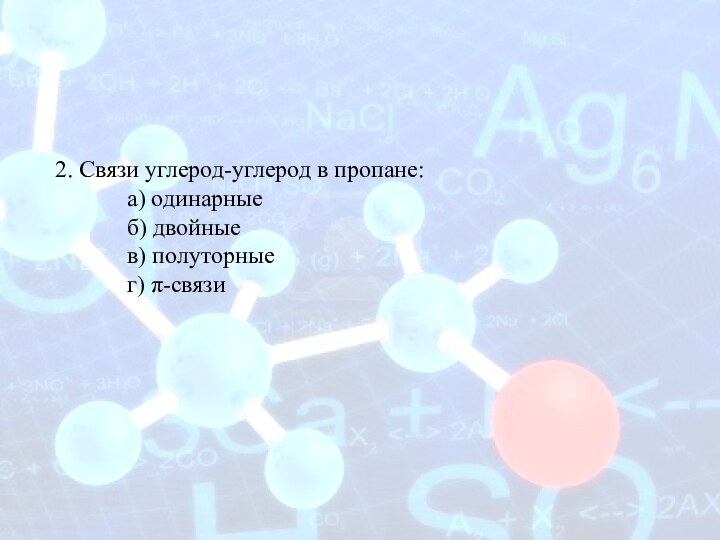
2. Связи углерод-углерод в пропане:
а) одинарные
б) двойные
в) полуторные
г)
π-связи
Слайд 28
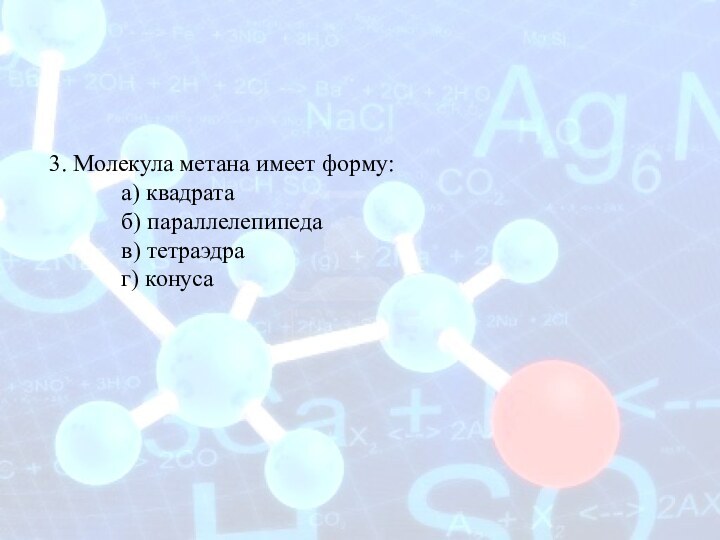
3. Молекула метана имеет форму:
а) квадрата
б) параллелепипеда
в) тетраэдра
г)
конуса
Слайд 29
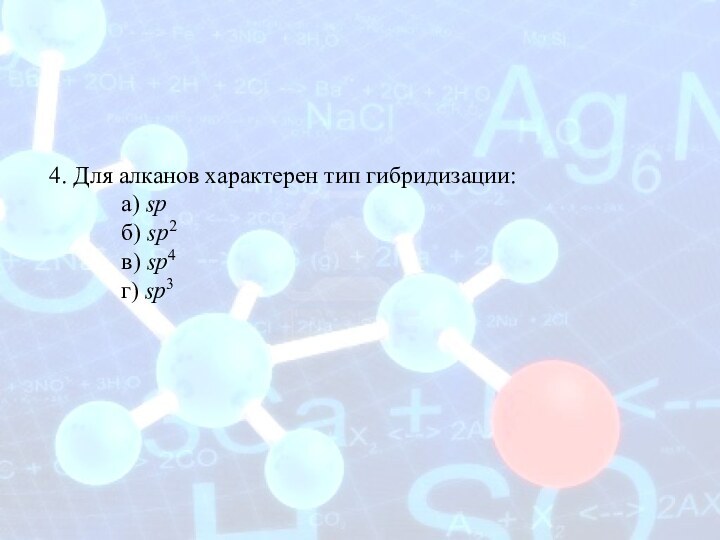
4. Для алканов характерен тип гибридизации:
а) sp
б) sp2
в)
sp4
г) sp3
Слайд 30
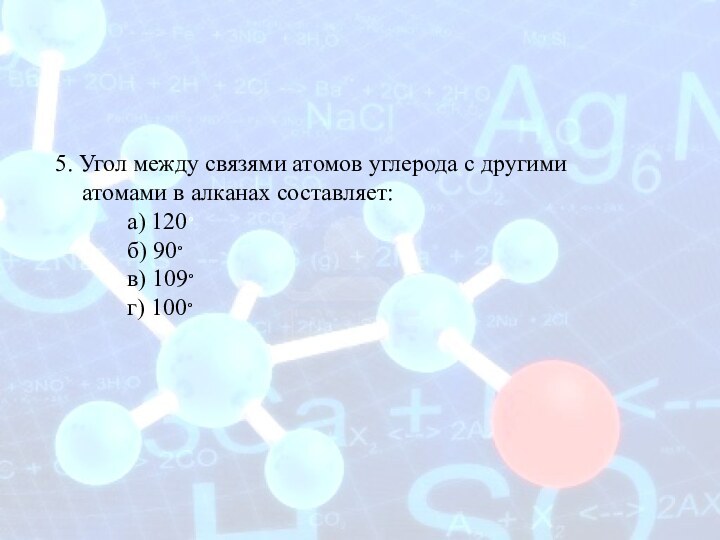
5. Угол между связями атомов углерода с другими
атомами в алканах составляет:
а) 120°
б) 90°
в) 109°
г) 100°
Слайд 31
6. Установите порядок определения названия углеводорода:
а) определяют местонахождение
радикалов
б) выбирают самую длинную цепь и нумеруют атомы углерода
в ней
в) определяют корень названия по числу атомов углерода в длинной цепи
г) составляют приставку в виде цифр, греческих числительных, названий радикалов
Слайд 32
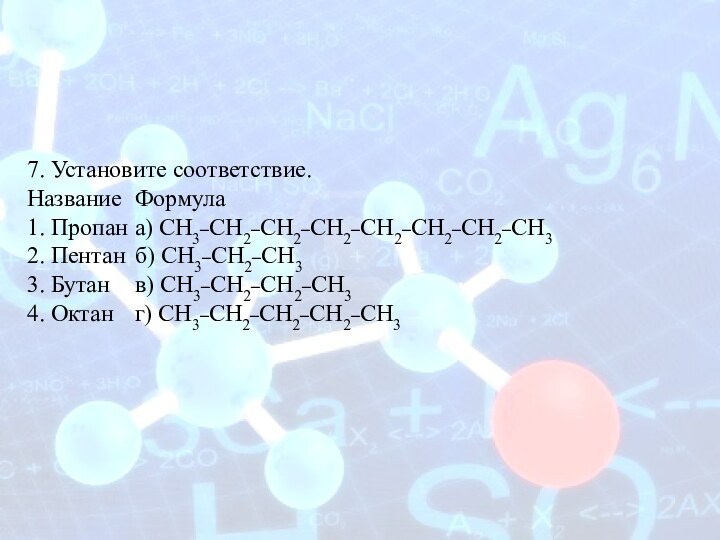
7. Установите соответствие.
Название Формула
1. Пропан а) СН3–СН2–СН2–СН2–СН2–СН2–СН2–СН3
2. Пентан б) СН3–СН2–СН3
3. Бутан в)
СН3–СН2–СН2–СН3
4. Октан г) СН3–СН2–СН2–СН2–СН3
Слайд 33
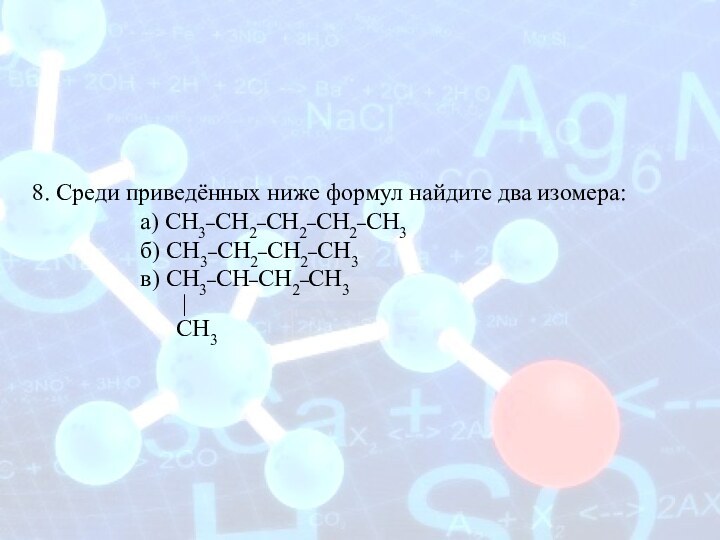
8. Среди приведённых ниже формул найдите два изомера:
а)
СН3–СН2–СН2–СН2–СН3
б) СН3–СН2–СН2–СН3
в) СН3–СН–СН2–СН3
|
СН3
Слайд 34
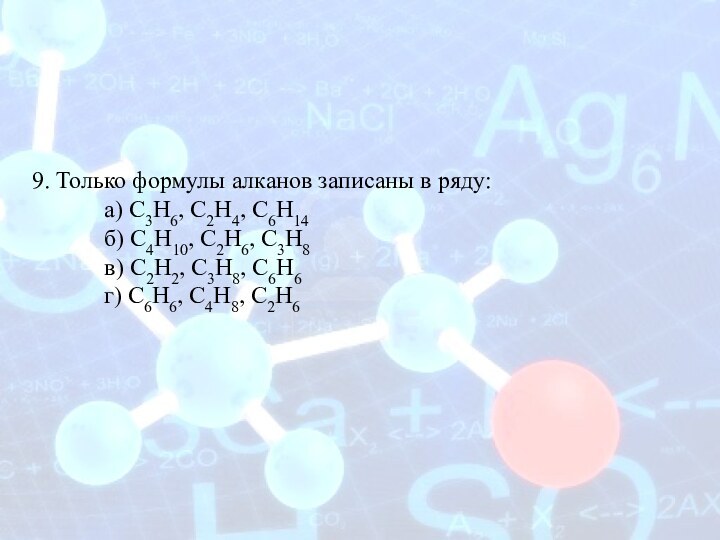
9. Только формулы алканов записаны в ряду:
а) С3Н6,
С2Н4, С6Н14
б) С4Н10, С2Н6, С3Н8
в) С2Н2, С3Н8, С6Н6
г) С6Н6,
С4Н8, С2Н6
Слайд 35
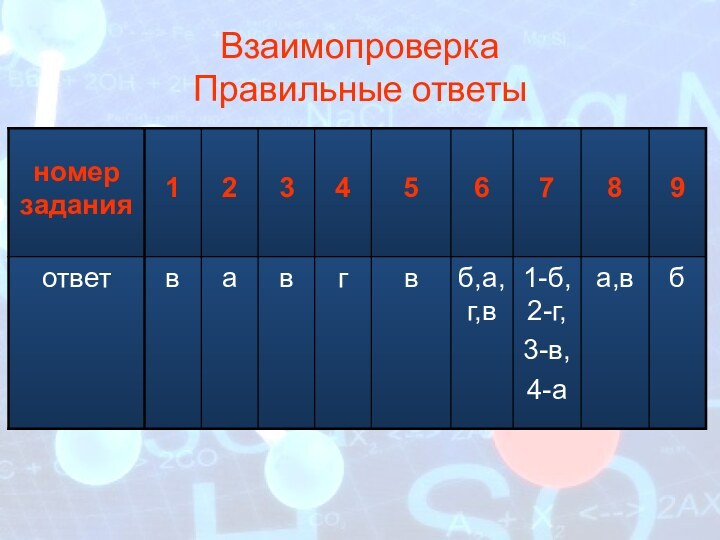
Взаимопроверка
Правильные ответы
Слайд 36
Рефлексия
5
4
3
Прием
«Гора успеха!»
Произведи самооценку и определи свое положение
на
«Горе успеха»
Слайд 37
Химические свойства алканов
Проблемный вопрос: Почему алканы считают малоактивными
веществами?
Слайд 38
Запомни!
Предельные углеводороды
не вступают в реакции присоединения. Для
них характерны реакции замещения, окисления и разложения. Алканы не
обесцвечивают раствор перманганата калия и бромную воду.
Слайд 39
Химические Свойства
1. Реакция горения.
Q
2
2
+
Слайд 40
Химические Свойства
2. Реакция замещения.
=
+
HCl
4
+
4
Слайд 41
3. Изомеризация
Под влиянием катализаторов при нагревании углеводороды
нормального строения подвергаются изомеризации - перестройке углеродного скелета с
образованием алканов разветвленного строения.
CH3-CH2-CH2-CH3 AlCl3 CH3-CH-CH3
CH3
n-бутан 2-метил пропан
.
Слайд 42
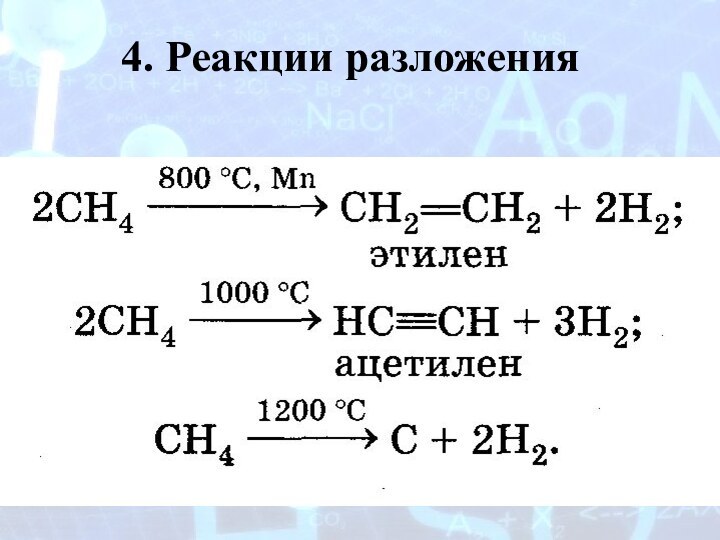
4. Реакции разложения
При увеличении температуры можно
достичь такой степени протекания реакции, при которой органические вещества
– углеводороды – полностью разлагаются на углерод и водород. Такой процесс называется пиролизом.
СН4 С+2Н2
Слайд 44
Проверь себя
1. Общая формула Анлканов?
2. Назовите гомологи пентана.
3.
Что такое Изомерия?
4. Назовите физические свойства метана.
5. Напишите структурную
формулу октана.