- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Материал к занятию : гидролиз
Содержание
- 2. ОпределениеГидролиз (вода и разложение) — один из видов
- 3. Гидролизу подвергаются соединения различных классов: соли, углеводы, белки, сложные эфиры, жиры
- 4. В общем виде Гидролиз можно представить уравнением:
- 5. Гидролиз сложных эфиров - обратимый процесс
- 6. Степень гидролиза – его качественная характеристикаПод степенью
- 7. Гидролиз солей Взаимодействие ионов соли с водой,
- 8. 2. Гидролиз соли сильной кислоты и слабого
- 9. 3. Гидролиз соли слабой кислоты и слабого
- 10. Источникиhttp://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%BE%D0%BB%D0%B8%D0%B7http://bse.sci-lib.com/article010250.htmlwww.dic.academic.ruhttp://www.tonnel.ru/?l=cal&aid=244&godik=2011http://www.risk.ru/users/robinsya/13659/
- 11. Скачать презентацию
- 12. Похожие презентации
ОпределениеГидролиз (вода и разложение) — один из видов химических реакций сольволиза, где при взаимодействии веществ с водой происходит разложение исходной молекулы с образованием новых соединений.










Слайд 3
Гидролизу подвергаются соединения различных классов:
соли,
углеводы,
белки,
сложные эфиры,
жиры
Слайд 4
В общем виде Гидролиз можно представить уравнением:
где А—В
— гидролизующееся вещество, А—Н и В—ОН — продукты
Слайд 6
Степень гидролиза – его качественная характеристика
Под степенью гидролиза
подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации
её ионов в растворе.Обозначается α (или hгидр); α = (cгидр/cобщ)·100 %
где cгидр — число молей гидролизованной соли, cобщ — общее число молей растворённой соли.
Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
Слайд 7
Гидролиз солей
Взаимодействие ионов соли с водой, приводящее к
образованию молекул слабого электролита, называют гидролизом солей.
1. Гидролиз соли
слабой кислоты и сильного основания:Na2CO3 + Н2О = NaHCO3 + NaOH
CO32− + H2O = HCO3− + OH−
(раствор имеет щелочную среду, реакция протекает обратимо)
Слайд 8
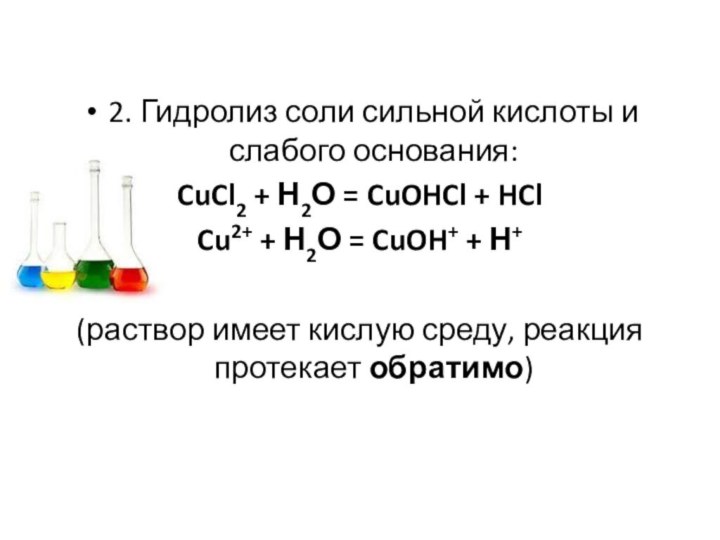
2. Гидролиз соли сильной кислоты и слабого основания:
CuCl2
+ Н2О = CuOHCl + HCl
Cu2+ + Н2О =
CuOH+ + Н+(раствор имеет кислую среду, реакция протекает обратимо)
Слайд 9
3. Гидролиз соли слабой кислоты и слабого основания:
Al2S3
+ 6H2O = 2Al(OH)3 + 3H2S
2Al3+ + 3S2− +
6Н2О = 2Al(OH)3(осадок) + ЗН2S(газ)(Гидролиз в этом случае протекает практически полностью, так как оба продукта гидролиза уходят из сферы реакции в виде осадка или газа).