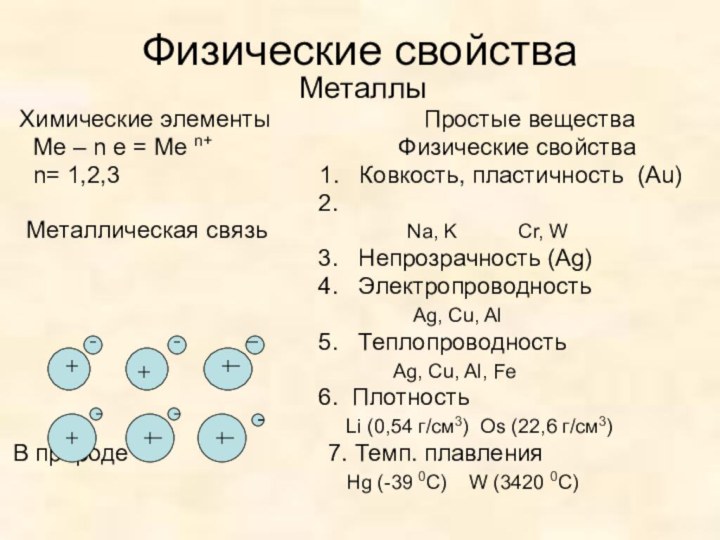
Простые
веществаМе – n e = Ме n+ Физические свойства
n= 1,2,3 1. Ковкость, пластичность (Au)
2.
Металлическая связь Na, K Cr, W
3. Непрозрачность (Ag)
4. Электропроводность
Ag, Cu, Al
5. Теплопроводность
Ag, Cu, Al, Fe
6. Плотность
Li (0,54 г/см3) Os (22,6 г/см3)
В природе 7. Темп. плавления
Hg (-39 0C) W (3420 0C)