Слайд 2
История
Открытие Дмитрием Менделеевым периодической таблицы химических элементов
в марте 1869 года стало настоящим прорывом в химии.
Российскому ученому удалось систематизировать знания о химических элементах и представить их в виде таблицы, которую и сейчас обязательно на уроках химии изучают школьники . В предложенной ученым таблице химические элементы располагались в зависимости от их свойств, обеспечивающихся величиной их молекулярной массы.
Слайд 3
Интересной особенностью таблицы Менделеева было также наличие пустых
клеток, которые в будущем были заполнены открытыми химическими элементами,
предсказанными ученым (германий, галлий, скандий). После открытия периодической таблицы в нее много раз вносились добавления и поправки. Совместно с шотландским химиком Уильямом Рамзаем Менделеев добавил в таблицу группу инертных газов (нулевую группу). В дальнейшем история периодической таблицы Менделеева была напрямую связана с открытиями в другой науке – физике. Работа над таблицей периодических элементов продолжается до сих пор, и современные ученые добавляют новые химические элементы по мере их открытия.
Слайд 4
Значение периодической системы Дмитрия Менделеева сложно переоценить, так
как благодаря ей:
Систематизировались знания о свойствах уже открытых
химических элементов;
Появилась возможность прогнозирования открытия новых химических элементов;
Начали развиваться такие разделы физики, как физика атома и физика ядра.
Слайд 6
По легенде, мысль о системе химических элементов пришла
к Менделееву во сне, однако известно, что однажды на
вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». Написав на карточках основные свойства каждого элемента (их в то время было известно 63, из которых один — дидим Di — оказался в дальнейшем смесью двух вновь открытых элементов празеодима и неодима), Менделеев начинает многократно переставлять эти карточки, составлять из них ряды сходных по свойствам элементов, сопоставлять ряды один с другим. Итогом работы стал отправленный в 1869 году в научные учреждения России и других стран первый вариант системы в котором элементы были расставлены по девятнадцати горизонтальным рядам
Слайд 7
и по шести вертикальным столбцам. В 1870 году
Менделеев в «Основах химии» публикует второй вариант системы («Естественную
систему элементов»), имеющий более привычный нам вид: горизонтальные столбцы элементов-аналогов превратились в восемь вертикально расположенных групп; шесть вертикальных столбцов первого варианта превратились в периоды, начинавшиеся щелочным металлом и заканчивающиеся галогеном. Каждый период был разбит на два ряда; элементы разных вошедших в группу рядов образовали подгруппы. Сущность открытия Менделеева заключалась в том, что с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически. После определённого количества разных по свойствам элементов, расположенных по возрастанию атомного веса, свойства начинают повторяться. Например, натрий похож на калий, фтор похож на хлор, а золото похоже на серебро и медь.
Слайд 8
Разумеется, свойства не повторяются в точности, к ним
добавляются и изменения. Отличием работы Менделеева от работ его
предшественников было то, что основ для классификации элементов у Менделеева была не одна, а две — атомная масса и химическое сходство. Для того, чтобы периодичность полностью соблюдалась, Менделеевым были предприняты очень смелые шаги: он исправил атомные массы некоторых элементов (например, бериллия, индия, урана, тория, церия, титана, иттрия), несколько элементов разместил в своей системе вопреки принятым в то время представлениям об их сходстве с другими (например, таллий, считавшийся щелочным металлом, он поместил в третью группу согласно его фактической максимальной валентности), оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы. В 1871 году на основе этих работ Менделеев сформулировал Периодический закон, форма которого со временем была несколько усовершенствована.
Слайд 9
Научная достоверность Периодического закона получила подтверждение очень скоро:
в 1875—1886 годах были открыты галлий (экаалюминий), скандий (экабор)
и германий (экасилиций), для которых Менделеев, пользуясь периодической системой, предсказал не только возможность их существования, но и, с поразительной точностью, целый ряд физических и химических свойств.
Слайд 11
Элементы полученные искусственным путём
17 марта 1950 года в
университете Беркли (штат Калифорния, США) искусственным путем был получен
новый радиоактивный химический элемент, которому присвоили атомный номер 98 в периодической системе и символ Cf (Californium). 113-й химический элемент, открытый специалистами японского института естественных наук «Рикэн», получил название нихоний(Nh).Элементы 115 и 117 получили названия московий (Mc) и теннессин (Ts). 118-й элемент получил название Оганесон (Og) в честь профессора Юрия Оганесяна, внесшего вклад в исследования сверхтяжелых элементов. Так же были получены элементы с 119 по 126 : унуненний (Uue), унбинилий(Ubn), унбиуний (Ubu), унбибий (Ubb), унбитрий (Ubt), унбиквадий (Ubq), унбипентий (Ubp), унбигексий ( Unh).
Слайд 12
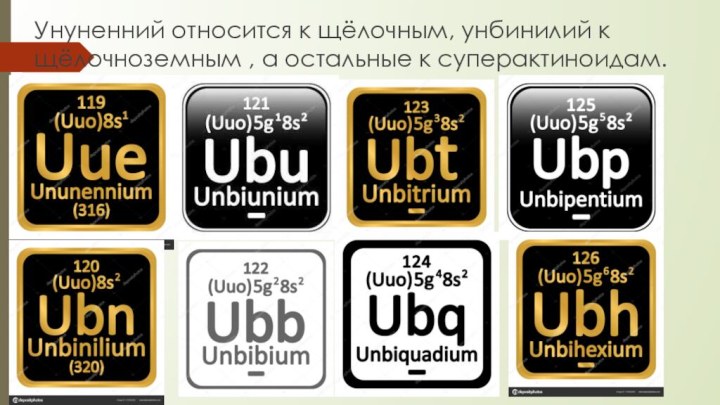
Унуненний относится к щёлочным, унбинилий к щёлочноземным ,
а остальные к суперактиноидам.
Слайд 13
Сейчас известно, что в земной коре содержатся следовые количества
93-го и 94-го элементов — нептуния и плутония. Но исторически эти элементы сначала
получили искусственно и лишь потом обнаружили в составе минералов. Американские власти почти на шесть лет задержали и публикацию об открытии 95-го элемента, америция, который в конце 1944 года был выделен группой Сиборга из продуктов нейтронной бомбардировки плутония в ядерном реакторе. Несколькими месяцами ранее физики из этой же команды получили первый изотоп 96-го элемента с атомным весом 242, синтезированный при бомбардировке урана-239 ускоренными альфа-частицами. Его назвали кюрием в знак признания научных заслуг Пьера и Марии Кюри, открыв тем самым традицию наименования трансуранов в честь классиков физики и химии.