- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Общие свойства металлов. Щелочные металлы
Содержание
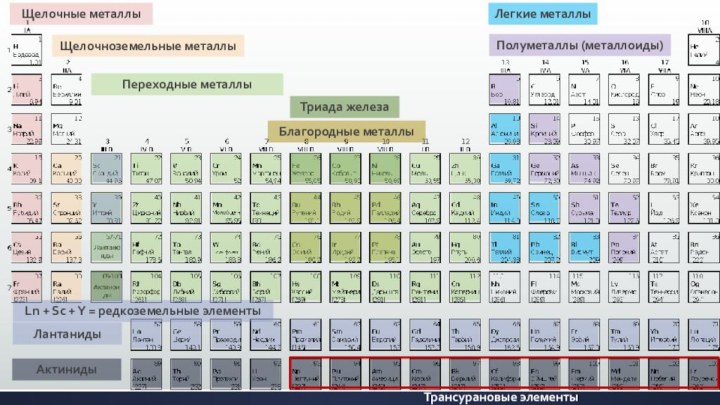
- 2. Щелочные металлыЩелочноземельные металлыПереходные металлыТриада железаБлагородные металлыЛантанидыАктинидыLn + Sc + Y = редкоземельные элементыТрансурановые элементыЛегкие металлыПолуметаллы (металлоиды)
- 3. Часть I.Нахождение в природе и физические свойства металлов
- 4. μεταλλον — «рудник, копь»Рудник (от слова руда) — горнопромышленное предприятие по добыче полезных ископаемых Копи (от копать) — устаревшее название сооружения для наземной и подземной разработки полезных ископаемых.
- 5. Руды, минералыЖелезная рудаМарганцевая рудаСвинцовая рудаЗолотая руда
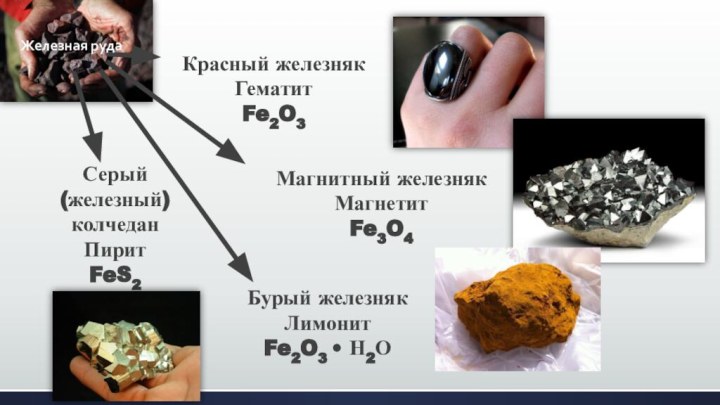
- 6. Красный железнякГематитFe2O3Магнитный железнякМагнетитFe3O4Бурый железнякЛимонитFe2O3 • Н2ОЖелезная рудаСерый (железный) колчеданПиритFeS2
- 7. Марганцевая рудаПиролюзитMnO2ГаусманитMn3O4Родохрозит(марганцевый шпат)MnCO3
- 8. Свинцовая рудаГаленитPbSЦерусситPbCO3АнглезитPbSO4
- 9. Металлическая связь - ответ на вопрос что удерживает атомы металлов в слитках, кристаллах и изделиях!
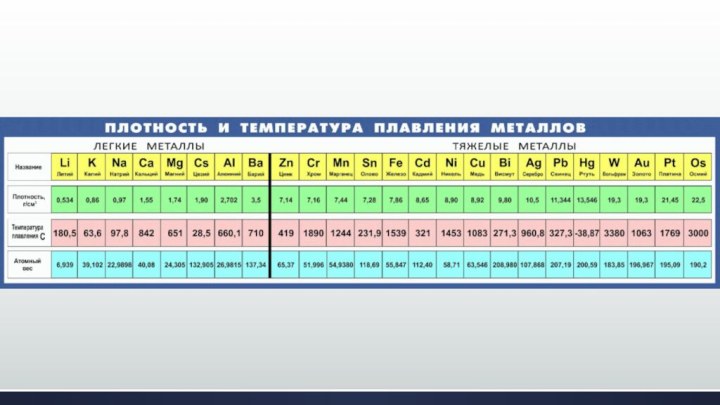
- 12. OsPtAuWReTaплотностьтугоплавкость
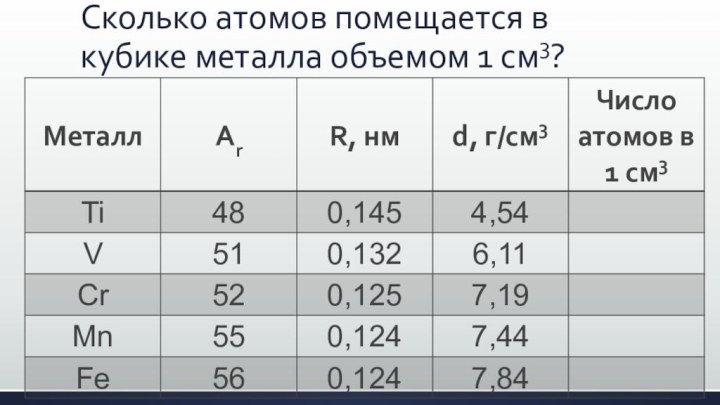
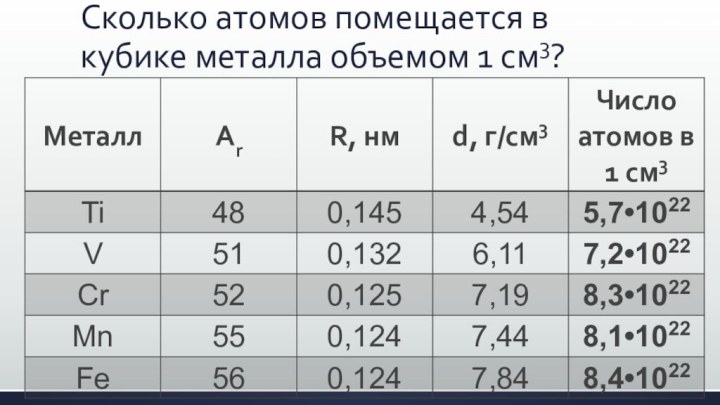
- 13. Сколько атомов помещается в кубике металла объемом 1 см3?
- 14. Сколько атомов помещается в кубике металла объемом 1 см3?
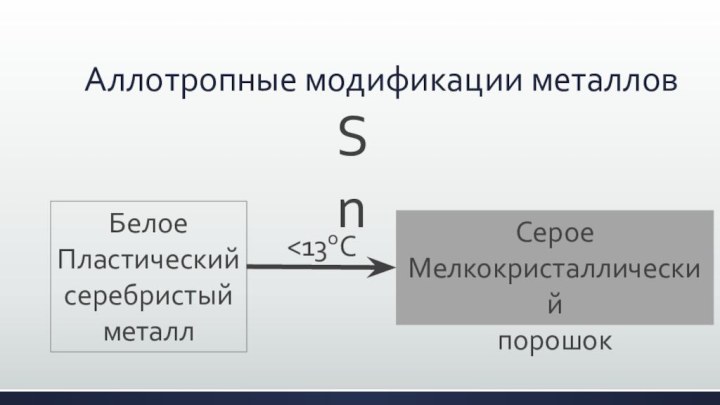
- 15. Аллотропные модификации металловSnСероеМелкокристаллическийпорошокБелоеПластический серебристый металл
- 17. Аллотропные модификации металловFe
- 18. Cu2+Зеленое
- 19. Соединения и химические свойства металловЧасть II.
- 22. Щелочные металлыI A группа
- 23. Li – lithos (греч.) – «камень» (1818
- 25. Тривиальные названия соединений щелочных металлов(учить наизусть!!!)
- 26. Тривиальные названия соединений щелочных металлов(учить наизусть!!!)
- 27. Свойства s-металлов 1. Простые электронные конфигурации:
- 28. Скачать презентацию
- 29. Похожие презентации
Щелочные металлыЩелочноземельные металлыПереходные металлыТриада железаБлагородные металлыЛантанидыАктинидыLn + Sc + Y = редкоземельные элементыТрансурановые элементыЛегкие металлыПолуметаллы (металлоиды)





















Слайд 2
Щелочные металлы
Щелочноземельные металлы
Переходные металлы
Триада железа
Благородные металлы
Лантаниды
Актиниды
Ln + Sc
+ Y = редкоземельные элементы
Слайд 4
μεταλλον — «рудник, копь»
Рудник (от слова руда) — горнопромышленное предприятие по добыче полезных ископаемых
Копи (от копать) — устаревшее название сооружения для
наземной и подземной разработки полезных ископаемых.
Слайд 6
Красный железняк
Гематит
Fe2O3
Магнитный железняк
Магнетит
Fe3O4
Бурый железняк
Лимонит
Fe2O3 • Н2О
Железная руда
Серый
(железный)
колчедан
Пирит
FeS2
Слайд 9 Металлическая связь - ответ на вопрос что удерживает атомы
металлов в слитках, кристаллах и изделиях!
Слайд 15
Аллотропные модификации металлов
Sn
Серое
Мелкокристаллический
порошок
Белое
Пластический
серебристый
металл
Слайд 23 Li – lithos (греч.) – «камень» (1818 г.
- Дэви, эл-лиз LiOH)
Na – содий/натроний (nitron - сода),
1807 г. - Г.ДэвиK – потассий (поташ, зола), (1807 г. - Дэви)
Rb – rubidus (лат.), «красный» (1863 г., Р.В.Бунзен)
Cs – caesius (лат.), «небесно-голубой» (1860 г. –Бунзен, Кирхгоф)
Fr – «экацезий» (1939 г., М. Перей)
Происхождение названия и первооткрыватель
Слайд 27
Свойства s-металлов
1. Простые электронные конфигурации: ns1, ns2
2.
Низкие Tпл. И малые значения энергии ионизации
3. Близкие соотношения
Z/R4. Высокая реакционная способность
5. Взаимодействуют с водой
2Na + 2H2O = 2NaOH + H2
6. Горят при нагревании на воздухе
2Na + O2= Na2O2 (пероксид)
7. Li горит в азоте
6Li + N2 = 2Li3N
8. Растворяются в жидком аммиаке
9. Гидроксиды – сильные основания: KOH ⇔ K+ + OH–





























