элементов подгруппы углерода:
а) ns2np2
б) ns2np3
в) ns2np4
г)
ns1np2
2. Наиболее характерная валентность элементов подгруппы углерода:
а) II
б) III
в) IV
г) V
3. Неметаллические свойства элементов подгруппы углерода в группе сверху вниз:
а) уменьшаются
б) уменьшаются, затем возрастают
в) возрастают
г) не изменяются
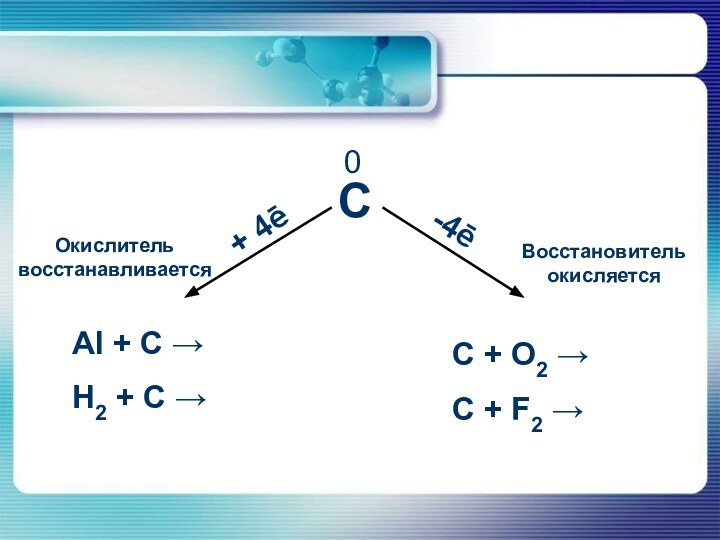
4. Углерод является:
а) восстановителем
б) восстановителем и окислителем
в) окислителем
г) не проявляет окислительно-восстановительных свойств
5. Атомную слоистую кристаллическую решетку имеет:
а) алмаз
б) фуллерен
в) графит
г) карбин
6. Наибольшей прочностью отличается кристаллическая решетка:
а) атомная
б) ионная
в) атомная слоистая
г) молекулярная
7. Наиболее химически активна аллотропная модификация углерода:
а) алмаз
б) фуллерен
в) графит
г) карбин