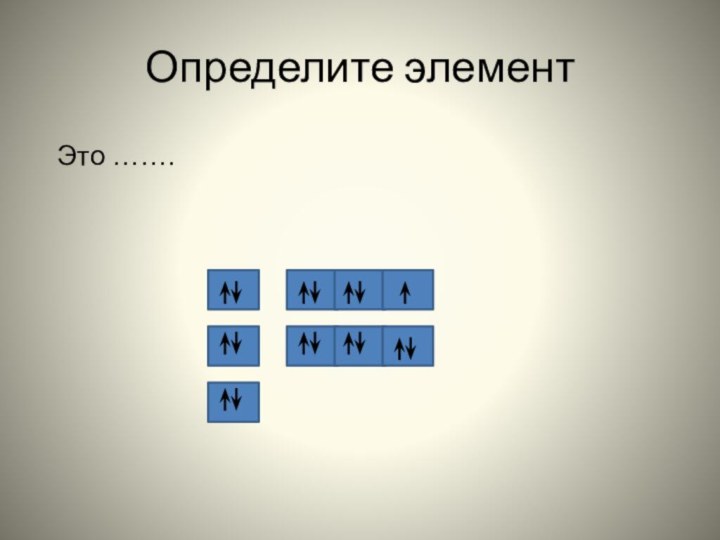
число; изотопы
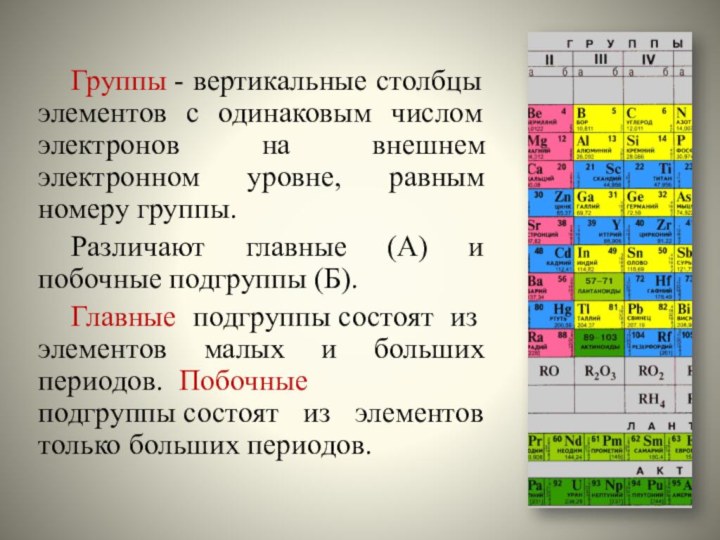
Номер периода
Номер группы для главных подгрупп
Число нейтронов N
= A – ZЭлектронные формулы, например, Li )2 )1 P )2)8)5 Ar)2 )8 )8 O )2 )6
1s2 2s1
1s2 2s2 2p4