- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Al – металл
Содержание
- 2. АлюминийМеталл
- 3. История открытияПервое знакомство человека с металлами произошло
- 4. Строение атомовАлюминий – элемент III группы, главной
- 5. Физические свойстваМеханически прочныйПлотность – 2,7 г/см3Электрическая проводимостьТеплопроводностьПластичностьОбразует
- 6. Химические свойстваC водой:
- 8. Получение 1) Очистка природных соединений2) В лаборатории:
- 9. БокситыБокситы – горная порода, состоящая главным образом
- 10. КорундМинерал . Обладает большой твердостью, применяется как абразивный материал.
- 11. АлюмосиликатыАлюмосиликаты составляют основную массу земной коры. Их
- 12. КриолитВ настоящее время приготавливается искусственным путем, применяется
- 13. Нахождение в природеВ природе алюминий встречается только
- 14. ПрименениеВ авиационной промышленности.Для кабели и провода.Детали аппаратов
- 15. Применение
- 16. Скачать презентацию
- 17. Похожие презентации
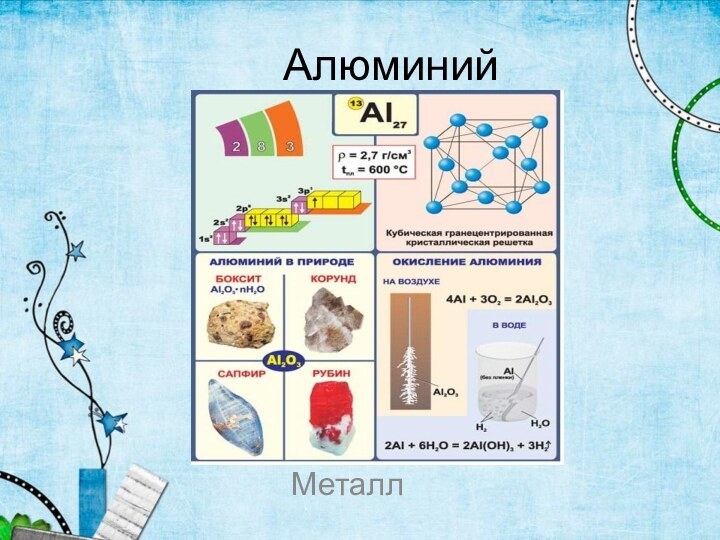
АлюминийМеталл














Слайд 4
Строение атомов
Алюминий – элемент III группы, главной подгруппы.
Порядковый
номер - 13
Р-элемент
На последнем энергетическом уровне 3 электрона
Степень окисления
+3Валентность III
Высший оксид Al2O3
Носится к группе легких металлов
Наиболее распространенный металл и третий по распространенности химический элемент в земной коре
Слайд 5
Физические свойства
Механически прочный
Плотность – 2,7 г/см3
Электрическая проводимость
Теплопроводность
Пластичность
Образует сплавы
Легкий,
парамагнитный металл
Серебристого цвета
Стойкий к коррозии(за счёт быстрого образования оксидных
плёнок , защищающих поверхность от дальнейшего взаимодействия.температура плавления у технического алюминия — 658 °C, у алюминия высокой чистоты — 660 °C
температура кипения — 2500 °C
Слайд 6
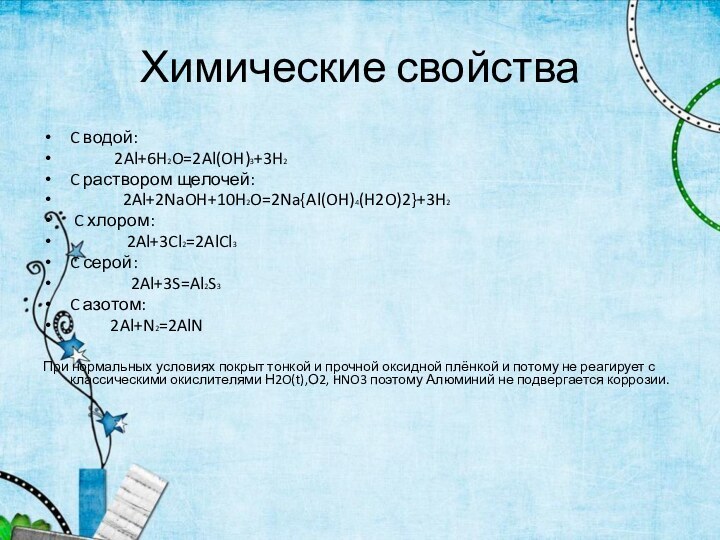
Химические свойства
C водой:
2Al+6H2O=2Al(OH)3+3H2
C раствором щелочей:
2Al+2NaOH+10H2O=2Na{Al(OH)4(H2O)2}+3H2C хлором:
2Al+3Cl2=2AlCl3
C серой:
2Al+3S=Al2S3
C азотом:
2Al+N2=2AlN
При нормальных условиях покрыт тонкой и прочной оксидной плёнкой и потому не реагирует с классическими окислителями Н2O(t),О2, HNO3 поэтому Алюминий не подвергается коррозии.
Слайд 8
Получение
1) Очистка природных соединений
2) В лаборатории:
4Al+3O2=2Al2O3(сжигание в О2)
2Al(OH)3=Al2O3+3H2O
3) Осаждение из солей
AlCl3+2NaOH=Al(OH)3+3NaClAl2S3+6H2O=2Al(OH)3+3H2S
Na{Al(OH)4}+HCl=Al(OH)3+NaCl+H2O
Слайд 9
Бокситы
Бокситы – горная порода, состоящая главным образом из
гидратированного оксида алюминия и оксидов железа, которые придают им
красный цвет.
Слайд 11
Алюмосиликаты
Алюмосиликаты составляют основную массу земной коры. Их можно
рассматривать как соли, образованные оксидами алюминия, кремния, щелочных и
щелочноземельных металлов. При выветривании многих алюмосиликатов образуется глина.Драгоценный камень Берилл представляет собой
алюмосиликат бериллия
Слайд 12
Криолит
В настоящее время приготавливается искусственным путем, применяется в
металлургии алюминия.
Криолит с криолитинитом и хиолитом, Ильменские горы, Урал.
Горный
Слайд 13
Нахождение в природе
В природе алюминий встречается только в
соединениях:
Бокситы — Al2O3 • H2O (с примесями SiO2, Fe2O3,
CaCO3)Нефелины — KNa3[AlSiO4]4
Алуниты — KAl(SO4)2 • 2Al(OH)3
Глинозёмы (смеси каолинов с песком SiO2, известняком CaCO3, магнезитом MgCO3)
Корунд — Al2O3
Полевой шпат (ортоклаз) — K2O×Al2O3×6SiO2
Каолинит — Al2O3×2SiO2 × 2H2O
Алунит — (Na,K)2SO4×Al2(SO4)3×4Al(OH)3
Берилл — 3ВеО • Al2О3 • 6SiO2