Слайд 2
лекция1
Аналитическая химия 2. ФХМА
Основы аналитической химии. / под
ред.
Ю.А. Золотова. Т.1-2. М. 2010.
2. Аналитическая химия.
/ под ред Л.Н.Москвина.
Т.1-3. М.: Академия, 2008.
3. Кельнер Р. и др. Аналитическая химия. Проблемы и подходы.Т.1-2. / Пер. с англ., под ред. Ю.А. Золотова. М.: Мир, 2004.
Литература
Слайд 3
лекция1
Аналитическая химия 2. ФХМА
Аналитическая химия – это наука,

развивающая общую методологию, методы и средства получения информации о
химическом составе вещества и разрабатывающая способы анализа различных объектов (ИЮПАК)
Характеристическое свойство – это свойство, проявляемое одним веществом или группой веществ в условиях определенных внешних воздействий на них
Аналитическая форма – химическая форма аналита, в котором он проявляет характеристическое свойство
Аналитический сигнал – это физическая величина, функционально связанная с концентрацией определяемого компонента (аналита)
Физическая величина – характеристика одного из свойств физического объекта, общую в качественном отношении для многих физических объектов, но в количественном отношении индивидуальную для каждого из них
Метод – это совокупность принципов, положенных в основу анализа безотносительно к конкретному объекту и определяемому веществу
Методика – подробное описание всех условий и операций проведения анализа определенного объекта
Слайд 4
лекция1
Аналитическая химия 2. ФХМА
Виды химического анализа
Качественный анализ –
определение состава анализируемого объекта на уровне образующих его атомов,
молекул, фаз и т.д.
Количественный анализ – определения количества образующих анализируемый объект атомов, молекул, фаз и т.д.
Полуколичественный анализ – приблизительная оценка уровня содержания определяемого компонента
Разведочный анализ – установление качественного состава с приблизительной оценкой уровня содержания отдельных компонентов
Неорганический и органический анализ
по природе определяемых частиц:
Элементный анализ - определение элементного состава вещества
Изотопный анализ – определение конкретных изотопов
Вещественный анализ – определение форм компонентов анализируемого объекта
Молекулярный анализ – определение химических соединений
Фазовый анализ – анализ включений (фаз) в неоднородном объекте
Структурно-групповой анализ – определение функциональных групп (отдельных групп органических соединений)
Слайд 5
лекция1
Аналитическая химия 2. ФХМА
Недеструктивный анализ – анализ без
разрушения анализируемого объекта
Деструктивный анализ – анализ с разрушением анализируемого
объекта
Лабораторный и внелабораторный анализ
on situ - Анализ на месте отбора проба
in situ - Анализ непосредственно в объекте
on line - Анализ на линии пробоотбора
Дистанционный анализ – беспробоотборное установление состава анализируемого объекта
Количественный анализ – определения количества образующих анализируемый объект атомов, молекул, фаз и т.д.
Полуколичественный анализ – приблизительная оценка уровня содержания определяемого компонента
Разведочный анализ – установление качественного состава с приблизительной оценкой уровня содержания отдельных компонентов
Неорганический и органический анализ
Локальный анализ – анализ отдельных фрагментов объекта
Слайд 6
лекция1
Аналитическая химия 2. ФХМА
Методы анализа
Химические методы основаны на
химических превращениях исследуемого вещества.
2. Физические методы основаны на измерении
каких-либо физических характеристик вещества.
3. Физико-химические методы основаны на изменении физических свойств исследуемой системы в результате определенных химических реакций.
4. Биологические методы анализа основаны на исследовании отклика живых организмов на изменения в окружающей среде.
Слайд 7
лекция1
Аналитическая химия 2. ФХМА
Истинное значение (xист) – значение
физической величины, которое идеальным образом характеризует ее в качественном
и количественном отношении.
Погрешность (Δx, Δ) – отклонение результата измерения от истинного значения.
Предел обнаружения - минимальное содержание определяемого компонента в пробе, при которой можно надежно зарегистрировать аналитический сигнал.
Нижняя граница определяемых концентраций (предел определения) - наименьшее значение содержания, которое можно определить с погрешностью, не превышающей заданную.
Верхняя граница определяемых концентраций – наибольшее значение содержания, которое можно определить с погрешностью, не превышающей заданную.
Коэффициент чувствительности – значение первой производной зависимости аналитического сигнала от концентрации.
Слайд 8
лекция1
Аналитическая химия 2. ФХМА
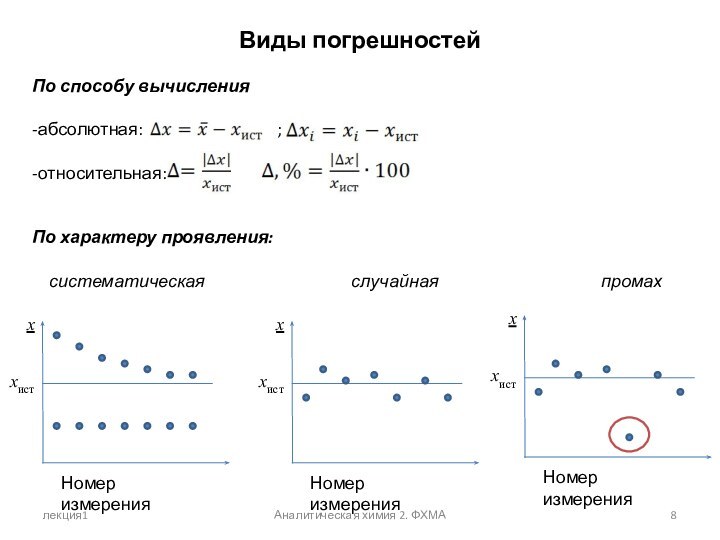
Виды погрешностей
По способу вычисления
-абсолютная:
;
-относительная: ;
По характеру проявления:
систематическая случайная промах
Слайд 9
лекция1
Аналитическая химия 2. ФХМА
Виды систематических погрешностей
Инструментальные: погрешности при
измерении аналитического сигнала на конкретном приборе
Методические: погрешности при пробоотборе,
пробоподготовке, наличием в пробе мешающих компонентов
Реактивные: погрешности связанные с примесями в используемых при анализе реактивов
Способы выявления систематических погрешностей
-Варьирование величины пробы (увеличение или уменьшение концентрации)
-Введено-найдено
-Сравнение с независимым методом
-Анализ стандартного образца
Устранение систематических погрешностей
Учет погрешностей известной природы
Рандомизация
Релятивизация
Слайд 10
лекция1
Аналитическая химия 2. ФХМА
Расчет случайных погрешностей
Среднее:
, , где n – число измерений
Стандартное отклонение:
Доверительный интервал (Δx): Интервал в котором с определенной вероятностью (доверительной вероятностью) находится истинное значение.
Доверительная вероятность (P): вероятность того, что измеренное (найденное путем анализа) значение случайной величины, отличается от ее среднего или истинного значения не более чем на заданную величину.
Слайд 11
лекция1
Аналитическая химия 2. ФХМА
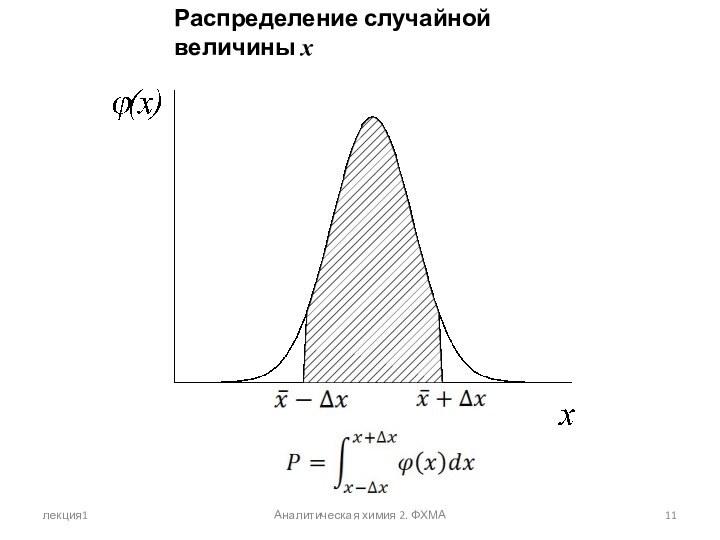
Распределение случайной величины x
Слайд 12
лекция1
Аналитическая химия 2. ФХМА
Расчет доверительного интервала с помощью
t-распределения Стьюдента
Значения t для различной доверительной вероятности
Слайд 13
лекция1
Аналитическая химия 2. ФХМА
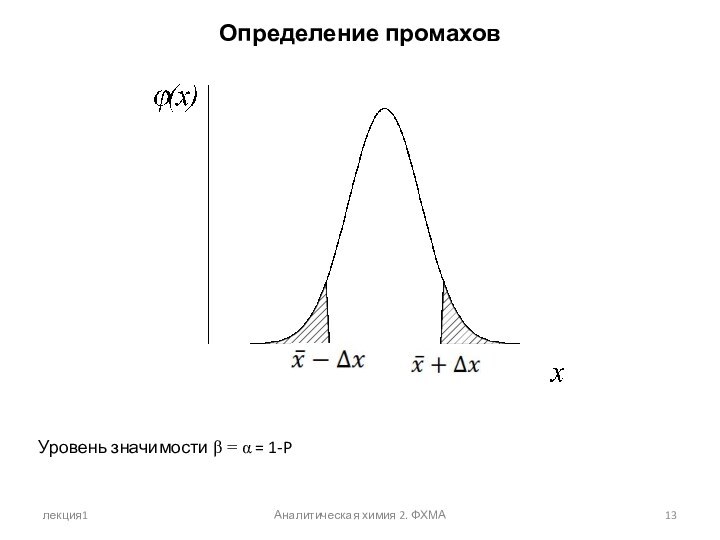
Определение промахов
Уровень значимости β =
α = 1-P
Слайд 14
лекция1
Аналитическая химия 2. ФХМА
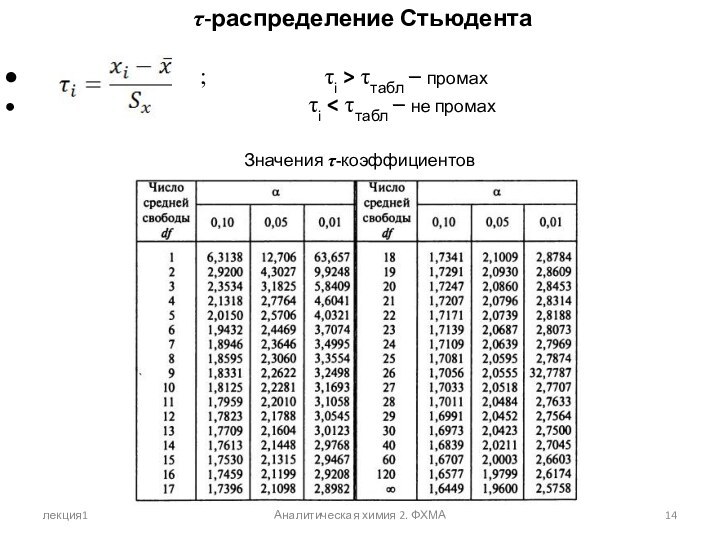
τ-распределение Стьюдента
; τi > τтабл – промах
τi < τтабл – не промах
Значения τ-коэффициентов
Слайд 15
лекция1
Аналитическая химия 2. ФХМА
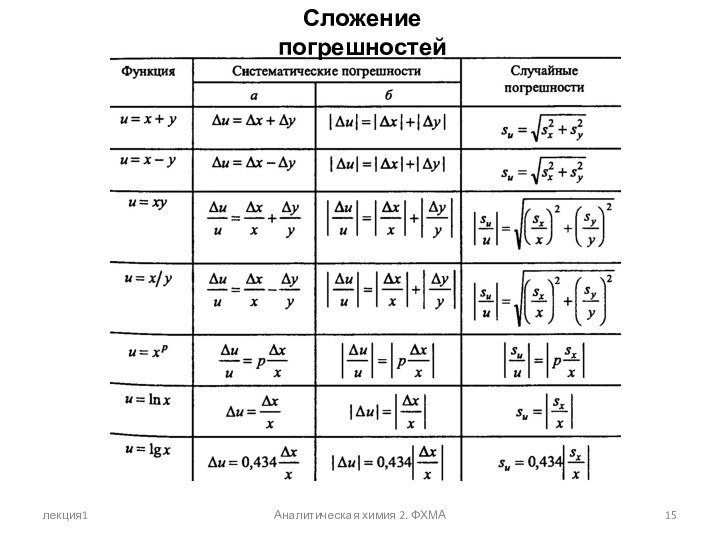
Сложение погрешностей
Слайд 16
лекция1
Аналитическая химия 2. ФХМА
Правильность – степень близости среднего

значения, полученного из большой серии результатов измерений, каждый из
которых может состоять из нескольких наблюдений, к истинному значению измеряемой величины.
Точность – степень близости результата измерений к истинному значению измеряемой величины
Прецизионность – степень близости друг к другу независимых результатов измерений одной и той же величины, проведенных при конкретных регламентированных условиях.
Повторяемость (сходимость) – прецизионность результатов измерений в условиях повторяемости, когда результаты измерений получены по одной и той же методике на идентичных объектах, в одной и той же лаборатории, одним и тем же оператором, с использованием одного и того же оборудования в пределах короткого интервала времени.
Воспроизводимость – прецизионность результатов измерений в условиях воспроизводимости, когда результаты измерений получены по одной и той же методике на идентичных объектах, но в разных лабораториях, разными операторами, с использованием разного оборудования, средств измерений и реактивов
Слайд 17
лекция1
Аналитическая химия 2. ФХМА
Связь аналитического сигнала с концентрацией
y=
f(Cx)
y - аналитический сигнал
Cx – определяемая концентрация
Способы определения концентрации:
без
использования образцов сравнения (безэталонный способ)
с использованием образцов сравнения
Образец сравнения (стандартный образец) - это образец вещества (материала) с установленными значениями одной или более величин в результате метрологической аттестации, характеризующими состав и/или структуру и/или свойство этого вещества (материала)
Слайд 18
лекция1
Аналитическая химия 2. ФХМА
Методы, основанные на использовании образцов
сравнения
Внешнего стандарта (метод стандартов)
один образец сравнения:
два образца сравнения – 1-й с меньшей концентраций по сравнению с определяемой, 2-й с большей (метод ограничивающих растворов):
Внутреннего стандарта
, где K – коэффициент, учитывающий различную
чувствительность стандартного и анализируемого
компонента
Слайд 19
лекция1
Аналитическая химия 2. ФХМА
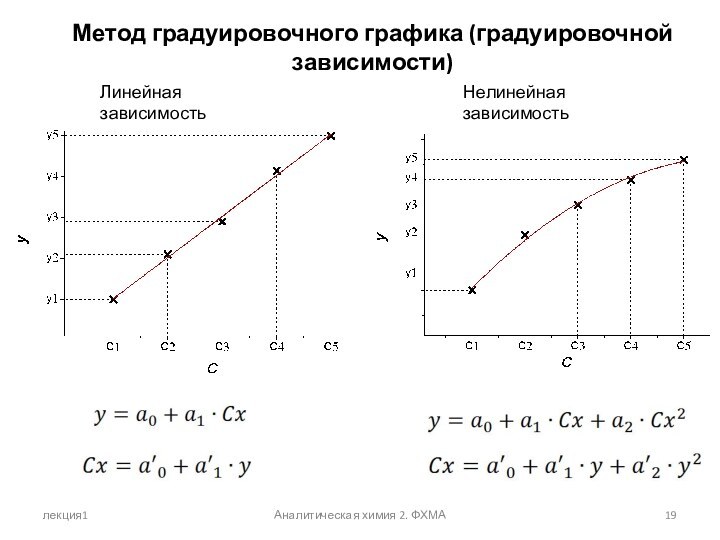
Метод градуировочного графика (градуировочной зависимости)
Линейная
зависимость
Нелинейная зависимость
Слайд 20
лекция1
Аналитическая химия 2. ФХМА
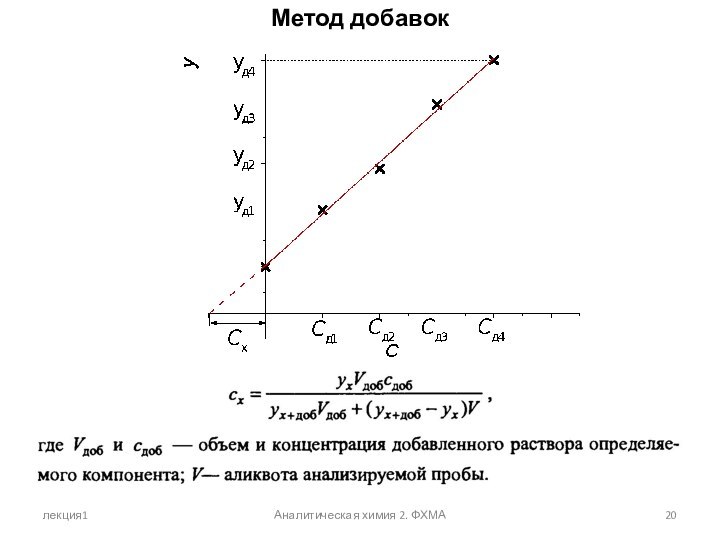
Метод добавок