- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химические свойства карбоновых кислот
Содержание
- 2. Разминка Номенклатура.Изомерия.Химические свойства КК, общие с неорганическими кислотами.
- 3. Проверь себя!
- 4. Цель урока: изучить химические свойства предельных одноосновных карбоновых кислот
- 5. Проблема Некоторые лекарственные препараты нельзя запивать целым
- 6. Ответьте на вопросы:Как происходит перераспределение электронной плотности
- 7. Реакции с разрывом связи О - НДиссоциация.
- 8. Реакции с разрывом связи С - ОРеакция
- 9. Изопентилацетат или изопентиловый эфир уксусной кислоты
- 11. 2. Образование галогенангидридов при взаимодействии с галогенидами
- 12. 3. Межмолекулярная дегидратация карбоновых кислот с образованием ангидридов.2R-CO-OH + Р2О5 → (R-CO-)2O + 2Н2О.
- 13. 4. Взаимодействие с аммиаком с образованием амидов
- 14. Реакции с разрывом связи С – Н
- 15. Окислительно – восстановительные реакции
- 16. В атмосфере кислорода карбоновые кислоты окисляются
- 18. Домашнее задание:1 ВАРИАНТ ЗАДАНИЯ: § 20, опорный
- 19. сегодня я узнал…было интересно…было трудно…я понял,
- 20. «Острова»Бермудскийтреугольнико. ГрустиО. удовольствияо.Тревогио.Просветленияо. ВоодушевленияО.Неопределенностио. Недоуменияо.Радости
- 21. Скачать презентацию
- 22. Похожие презентации
Разминка Номенклатура.Изомерия.Химические свойства КК, общие с неорганическими кислотами.


















Слайд 5
Проблема
Некоторые лекарственные препараты нельзя запивать целым рядом
напитков, в том числе кислые фрукты и соки, маринады,
блюда с уксусом нельзя употреблять в пищу наряду с антибиотиками пенициллинового ряда и эритромицином.Как вы думаете, чем вызван данный запрет?
Слайд 6
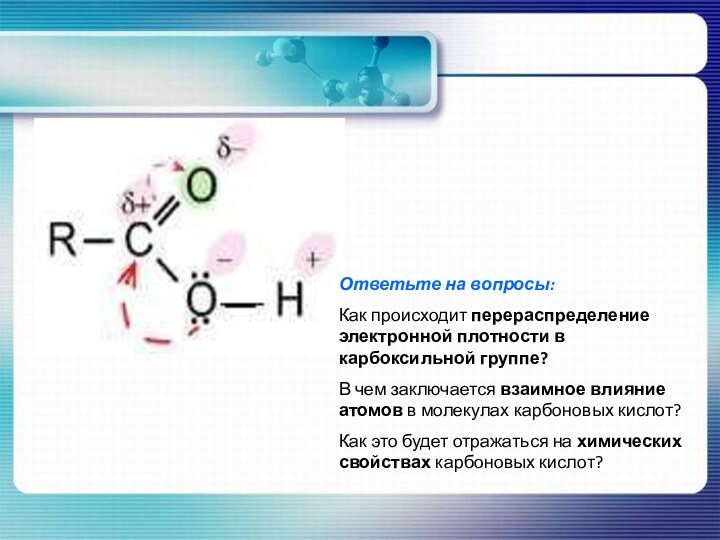
Ответьте на вопросы:
Как происходит перераспределение электронной плотности в
карбоксильной группе?
В чем заключается взаимное влияние атомов в молекулах
карбоновых кислот? Как это будет отражаться на химических свойствах карбоновых кислот?
Слайд 7
Реакции с разрывом связи О - Н
Диссоциация.
2. Взаимодействие с активными металлами.
3. Взаимодействие с
основаниями – реакция нейтрализации.4. Взаимодействие с основными оксидами.
5. Взаимодействие с солями более слабых кислот.
Слайд 8
Реакции с разрывом связи С - О
Реакция этерификации
– образование сложного эфира при взаимодействии со спиртами.
OH+ ׀׀
CH3COOH + C2H5OH ↔ CH3 — C — O — C2H5 + H2O
Слайд 11
2. Образование галогенангидридов при взаимодействии
с галогенидами фосфора
или тионилхлоридом SOCl2
RCOOH + РСl 5 → RCOCl +
РОСl3 + HClхлорангидрид
RCOOH + SOCl2 → RCOCl + HCl + SO2
тионилхлорид
Слайд 12
3. Межмолекулярная дегидратация карбоновых кислот
с образованием ангидридов.
2R-CO-OH
+ Р2О5 → (R-CO-)2O + 2Н2О.
Слайд 13
4. Взаимодействие с аммиаком с образованием амидов кислот.
t
R — COOH + NH3 → R — COO — NH4 → R — CO — NH2 + H2O
амид
R-СО-Сl + NН3 → R-СО-NН2 + HCl.
хлорангидрид амид
Р205
R - CO-NH2 → CH3-C ≡ N + Н2О
амид нитрил
Слайд 14 Реакции с разрывом связи С – Н (
у α – С – атома)
+ Cl2 P кр + Cl2 P кр + Cl2 P кр CH3COOH → ClCH2COOH → Cl2 CHCOOH → Сl3COOH
уксусная - HCl монохлоруксусная - HCl дихлоруксусная - HCl трихлоруксусная
кислота кислота кислота кислота
Слайд 15
Окислительно – восстановительные реакции
2[Н]
СН3СООН
→ СН3СНО + Н2О4[Н]
СН3СООН → СН3СН2ОН + Н2О
6[Н]
СН3СООН → С2Н6 + 2Н20
Карбоновые кислоты при действии восстановителей в присутствии катализаторов способны превращаться в альдегиды, спирты и даже углеводороды
Слайд 18
Домашнее задание:
1 ВАРИАНТ ЗАДАНИЯ: § 20, опорный КОНСПЕКТ,
2 ВАРИАНТ ЗАДАНИЯ: § 20, опорный КОНСПЕКТ, цепочка превращений
ТВОРЧЕСКОЕ
ЗАДАНИЕ: ПРЕЗЕНТАЦИЯ О ПРИМЕНЕНИИ ОРГАНИЧЕСКИХ КИСЛОТ (ПО ЖЕЛАНИЮ)
Слайд 19
сегодня я узнал…
было интересно…
было трудно…
я понял, что…
теперь
я могу…
я почувствовал, что…
я приобрел…
я научился…
у меня получилось …
меня
удивило…урок дал мне для жизни…
мне захотелось…
Продолжи фразу.