- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Карбоновые кислоты 11 класс
Содержание
- 2. Karboksüülhapped – карбоновые кислотыRasvhapped - жирные кислотыAminohapped
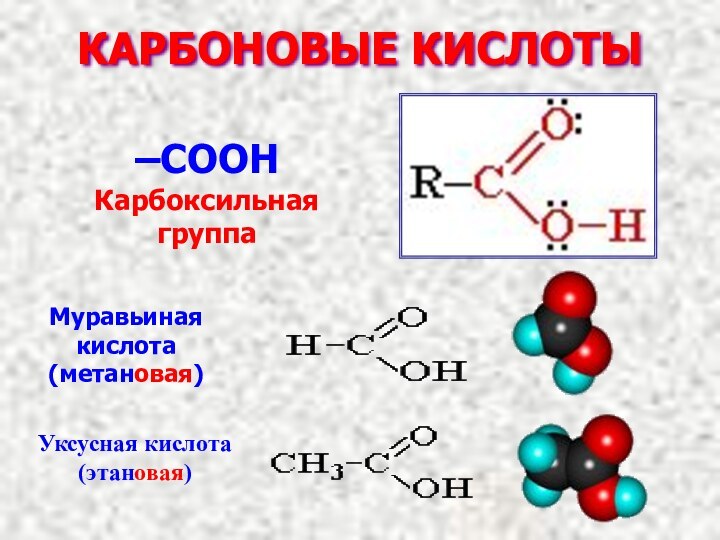
- 3. КАРБОНОВЫЕ КИСЛОТЫ –COOHКарбоксильная группа
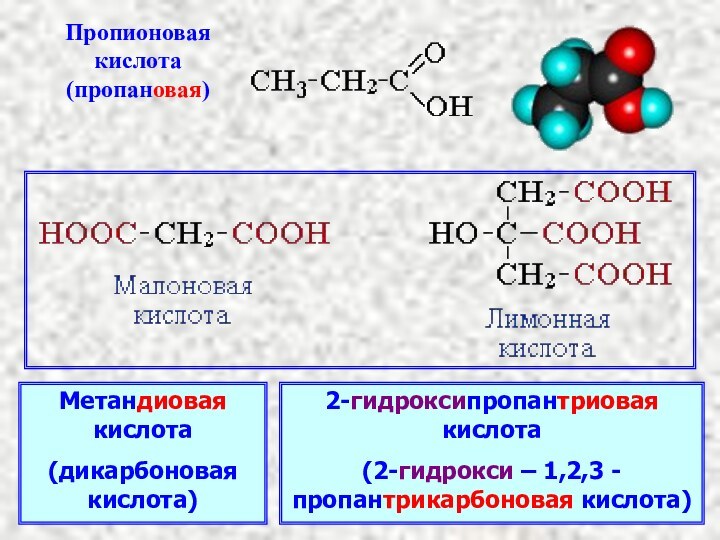
- 4. Метандиовая кислота(дикарбоновая кислота)2-гидроксипропантриовая кислота(2-гидрокси – 1,2,3 -пропантрикарбоновая кислота)
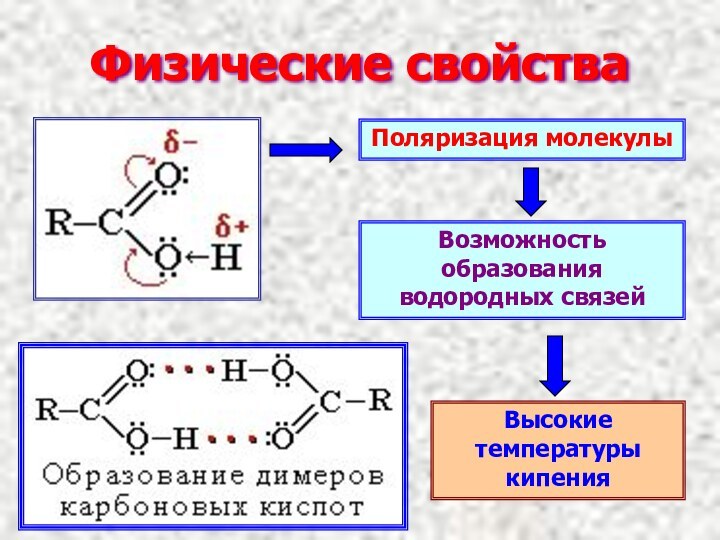
- 6. Физические свойстваПоляризация молекулыВозможность образования водородных связейВысокие температуры кипения
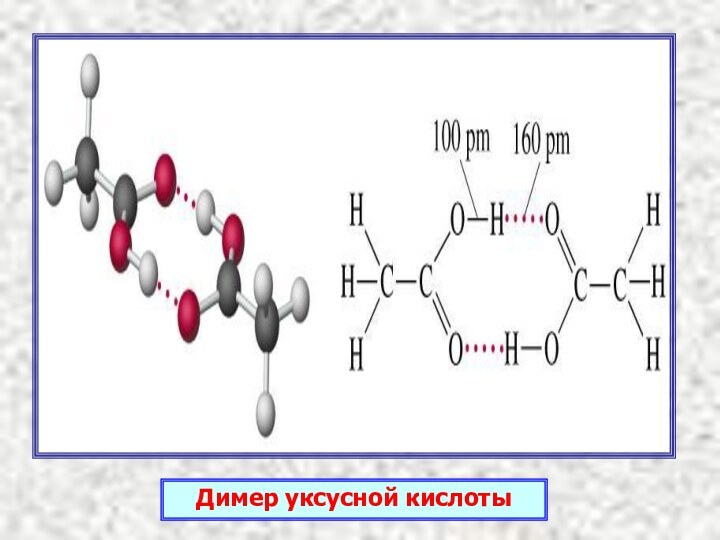
- 7. Димер уксусной кислоты
- 8. Растворимость в водеС увеличением молекулярной массы растворимость кислот в воде уменьшается из-за гидрофобности углеводородного радикала
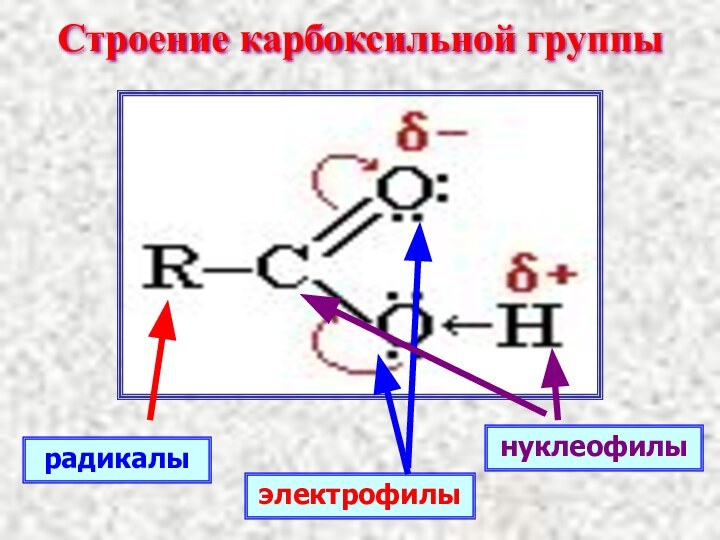
- 9. Строение карбоксильной группы радикалынуклеофилыэлектрофилы
- 10. Химические свойстваПроявляют общие свойства кислотЯвляются более сильными
- 11. 2RCOOH + Mg → (RCOO)2Mg + H22СH3COOH
- 12. Галогензамещенные кислоты––Br2→ Образуются при замещении водорода на
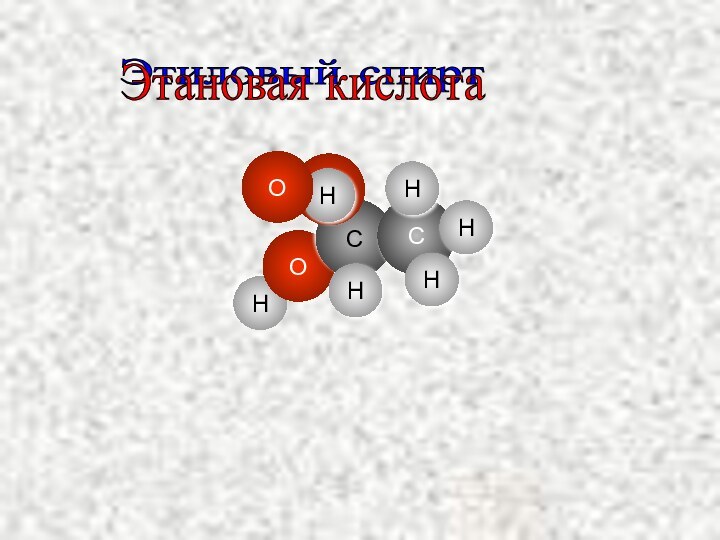
- 13. HOCOCHHHЭтиловый спирт HHЭтановая кислота O
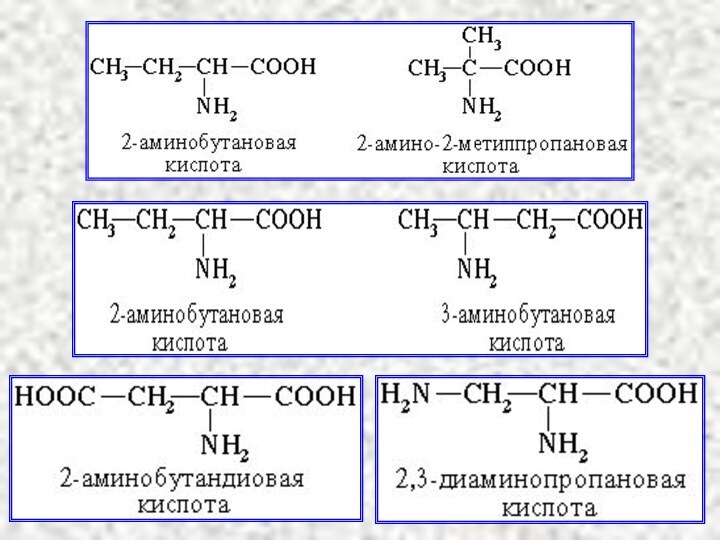
- 14. Замещенные карбоновые кислоты ГидроксикислотыHO–R–COOH АминокислотыNH2–R–COOH Проявляют двойственные
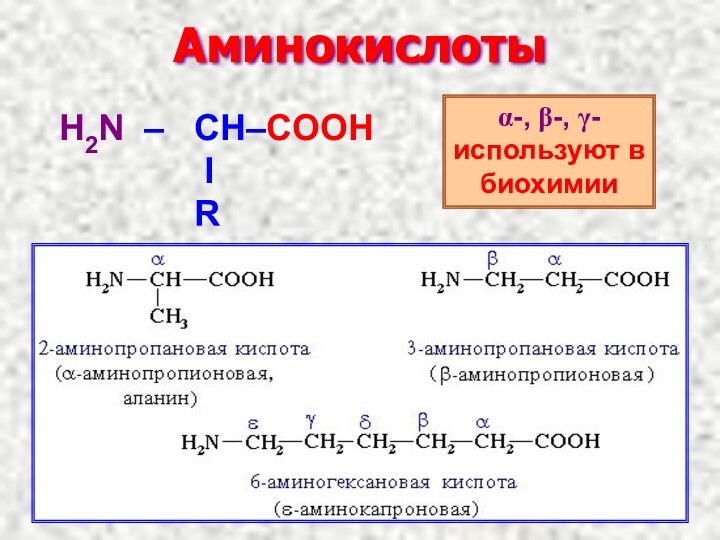
- 15. Аминокислоты α-, β-, γ- используют в биохимии
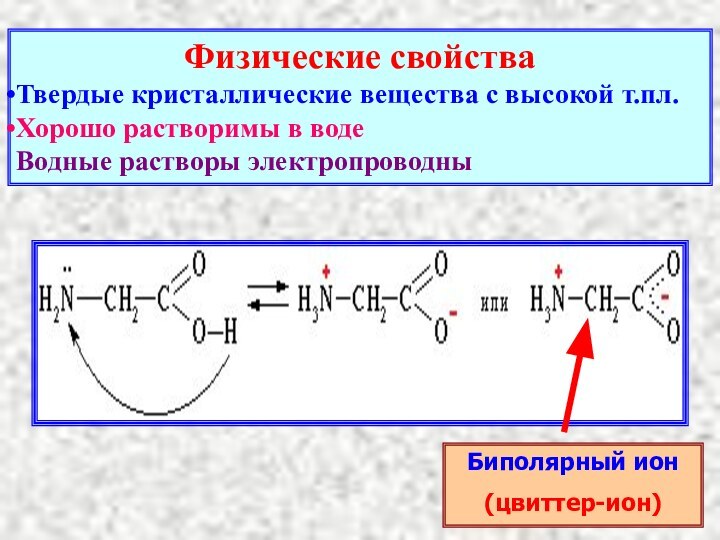
- 17. Физические свойстваТвердые кристаллические вещества с высокой т.пл. Хорошо растворимы в водеВодные растворы электропроводны Биполярный ион(цвиттер-ион)
- 18. Химические свойства Аминокислоты являются амфотерными соединениямиH2N–CH2–COOH +
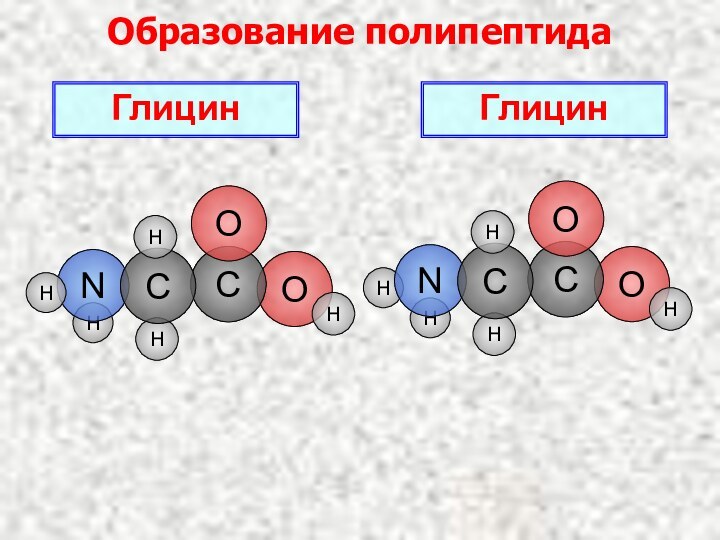
- 19. Образование полипептидаГлицин HOHHГлицин
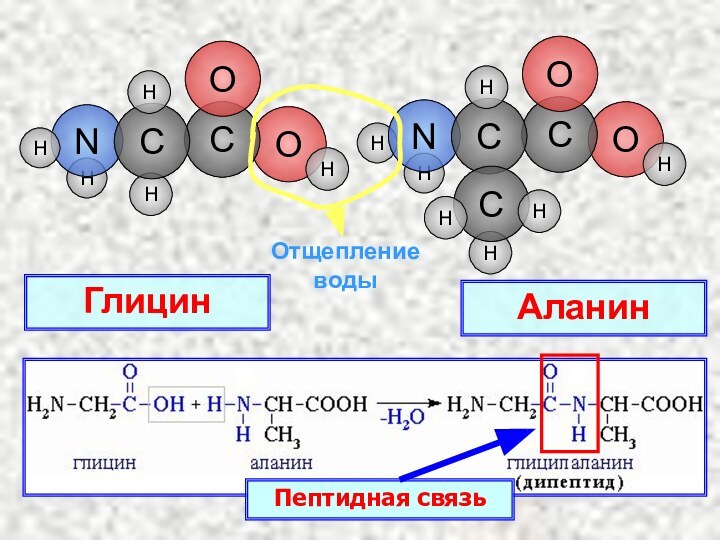
- 20. HOHHHHOCNOCHHCHHОтщепление водыГлицин Аланин Пептидная связь
- 21. Скачать презентацию
- 22. Похожие презентации
Karboksüülhapped – карбоновые кислотыRasvhapped - жирные кислотыAminohapped - аминокислотыKaksikioon – биполярный ионPiptiidside - пептидная связьPolüamiidid - полиамиды



![Карбоновые кислоты 11 класс Химические свойства Аминокислоты являются амфотерными соединениямиH2N–CH2–COOH + HCl → Cl− [H3N–CH2–COOH]+Как основаниеH2N–CH2–COOH](/img/tmb/12/1180434/26110a51b875b1d87f914146164888f6-720x.jpg)
Слайд 4
Метандиовая кислота
(дикарбоновая кислота)
2-гидроксипропантриовая кислота
(2-гидрокси – 1,2,3 -пропантрикарбоновая кислота)
Слайд 6
Физические свойства
Поляризация молекулы
Возможность образования водородных связей
Высокие температуры кипения
Слайд 8
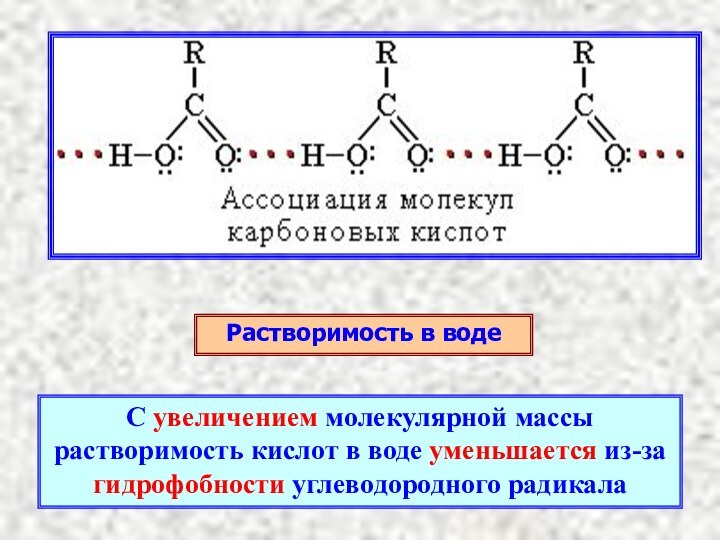
Растворимость в воде
С увеличением молекулярной массы растворимость кислот
в воде уменьшается из-за гидрофобности углеводородного радикала
Слайд 10
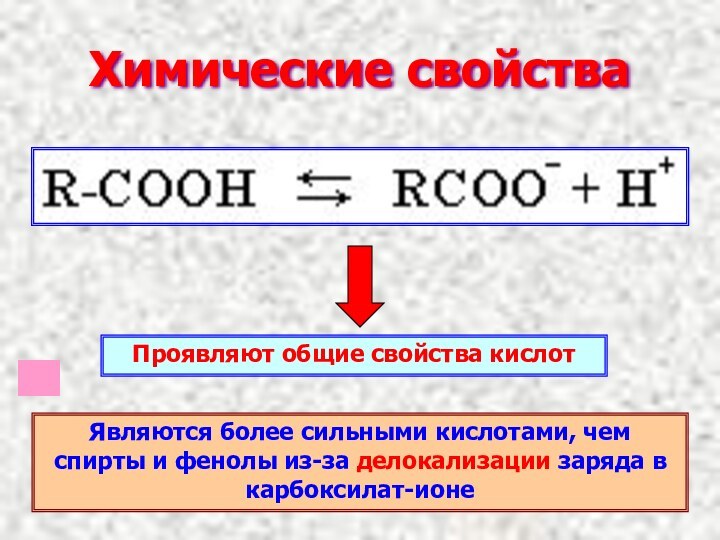
Химические свойства
Проявляют общие свойства кислот
Являются более сильными кислотами,
чем спирты и фенолы из-за делокализации заряда в карбоксилат-ионе
Слайд 11
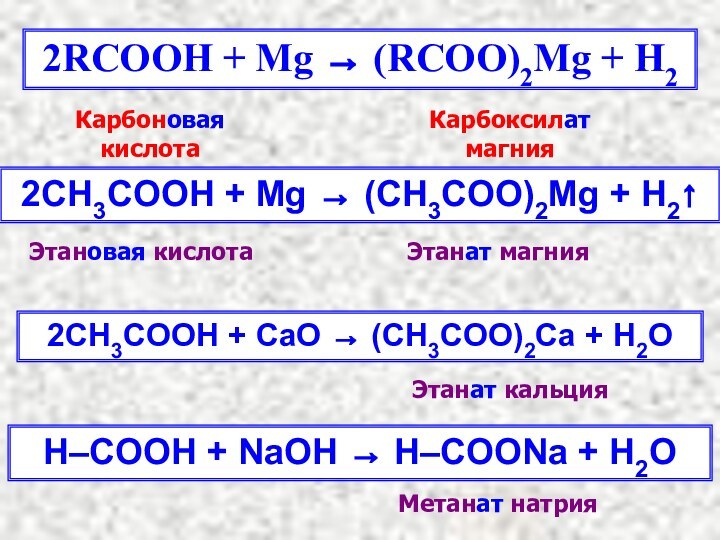
2RCOOH + Mg → (RCOO)2Mg + H2
2СH3COOH +
Mg → (CH3COO)2Mg + H2↑
Карбоновая кислота
Карбоксилат магния
Этановая кислота
Этанат магния
2СH3COOH
+ СaO → (CH3COO)2Ca + H2OH–COOH + NaOH → H–COONa + H2O
Этанат кальция
Метанат натрия
Слайд 12
Галогензамещенные кислоты
––Br2→
Образуются при замещении водорода на галоген
в углеводородном радикале
Галогензамещённые кислоты – более сильные кислоты, чем
карбоновые, за счёт -I эффекта атома галогена
Слайд 14
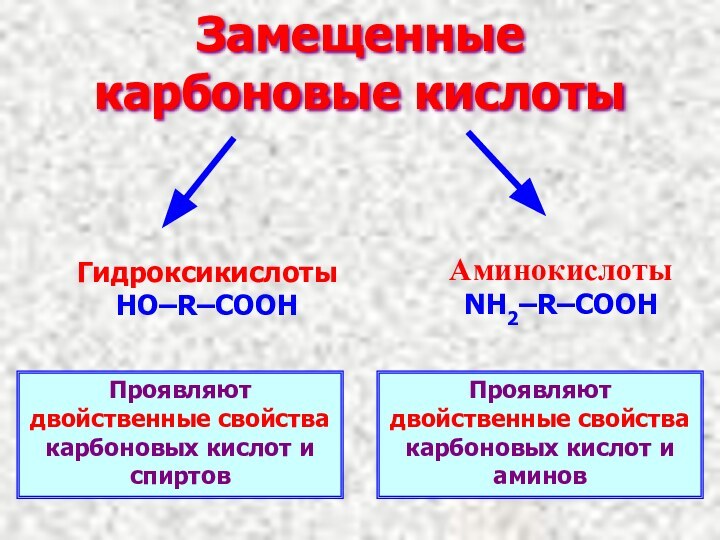
Замещенные карбоновые кислоты
Гидроксикислоты
HO–R–COOH
Аминокислоты
NH2–R–COOH
Проявляют двойственные свойства
карбоновых кислот и спиртов
Проявляют двойственные свойства карбоновых кислот и
аминов
Слайд 17
Физические свойства
Твердые кристаллические вещества с высокой т.пл.
Хорошо
растворимы в воде
Водные растворы электропроводны
Биполярный ион
(цвиттер-ион)
Слайд 18
Химические свойства
Аминокислоты являются амфотерными соединениями
H2N–CH2–COOH + HCl
→ Cl− [H3N–CH2–COOH]+
Как основание
H2N–CH2–COOH + NaOH → H2N–CH2–COO− Na+
+ H2OКак кислота





























