кислотным остатком
Электролиты, диссоциирующие с образованием катионов водорода и
анионов кислотного остаткаЧто такое кислоты?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть




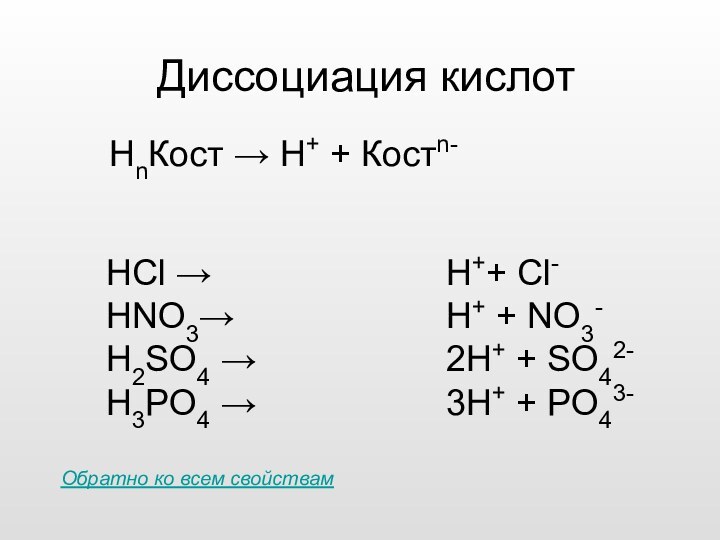











Что такое кислоты?
Обратно ко всем свойствам
3
H2
Реакция возможна, если:
Металл находится в ряду активности до водорода;
В результате реакции получается растворимая соль;
Кислота растворима
Al2(SO4)3 +
Обратно ко всем свойствам
MgO +
2
HCl →
MgCl2 + H2O
MgO + 2H+ + 2Cl- → Mg2+ + 2Cl- + H2O
MgO + 2H+ → Mg2+ + H2O
Обратно ко всем свойствам
Na3PO4 +
3
H2O
3
3Na+ + 3OH- + 3H+ + PO43- → 3Na+ + PO43- + 3H2O
H+ + OH- → H2O
Реакция между щелочью и кислотой с образованием соли и воды называется реакцией нейтрализации.
!
Обратно ко всем свойствам
Li2CO3 +
H3PO4 →
Li3PO4 +
H2O +
CO2
3
2
2
3
3
6Li+ + 3CO32- + 6H+ + PO43- → 6Li+ + 2PO43- + 3H2O + 3CO2
2H+ + CO32- → H2O + CO2
Реакция возможна, если в результате образуется осадок, газ или слабый электролит
Обратно ко всем свойствам
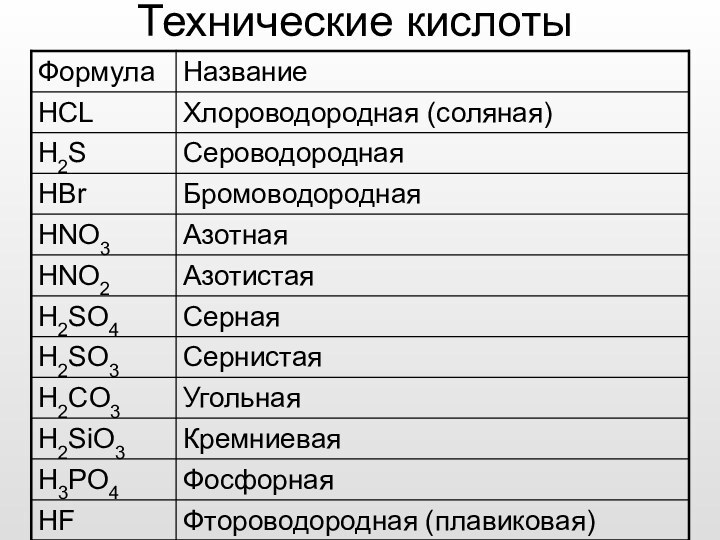
Пищевые кислоты