один из которых – кислород в степени окисления -2.
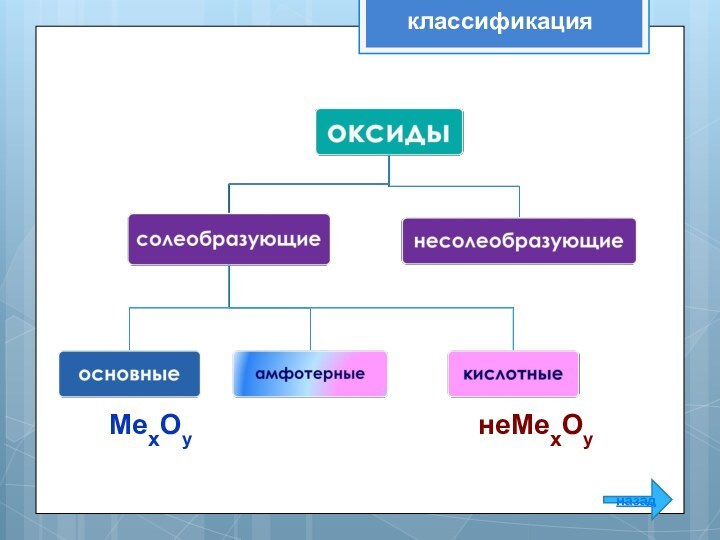
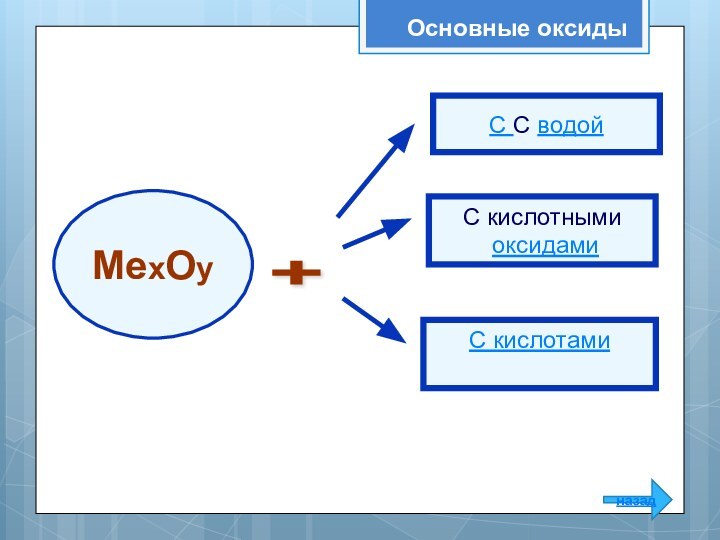
МехОу
Физические свойства:
Агрегатное состояние:
Цвет:
Растворимость в воде:
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть

















Физические свойства:
Агрегатное состояние:
Цвет:
Растворимость в воде: