- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Основания, кислоты, соли
Содержание
- 2. Цель урока: обобщить и систематизировать знания по
- 3. Проверка выполнения домашнего задания№1 стр. 73Фосфорная кислота
- 4. Проверка выполнения домашнего задания№ 3 стр. 73N2O3
- 5. Проверка выполнения домашнего задания№4 стр. 73Только четыре
- 6. Проверка знаний, полученных на предыдущем урокеКакие вещества
- 7. Закрепление знаний, полученных на предыдущем урокеРазделите предложенные
- 8. Закрепление знаний, полученных на предыдущем урокеРазделите предложенные
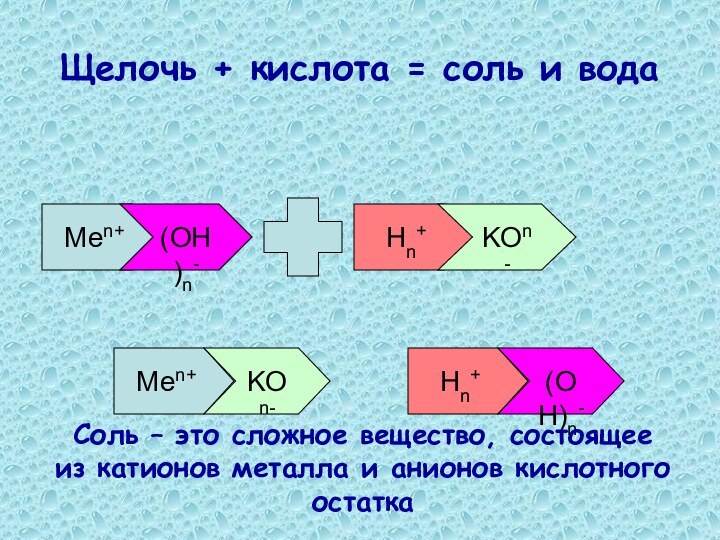
- 9. Щелочь + кислота = соль и водаMen+
- 11. Скачать презентацию
- 12. Похожие презентации
Цель урока: обобщить и систематизировать знания по темам: основания и кислоты; познакомиться с новым классом неорганических веществ – солями.







Слайд 3
Проверка выполнения домашнего задания
№1 стр. 73
Фосфорная кислота
Формула
- H3PO4
Кислородсодержащая
Трехосновная
Растворимая
С.О.: H+1 P+5 O-2
H3+1 P+5 O4-2 Заряд аниона: -3
Соответствующий оксид - P2O5
Слайд 4
Проверка выполнения домашнего задания
№ 3 стр. 73
N2O3 –
Оксид азота (III) – азотистая HNO2
CO2 – Оксид углерода
(IV) – угольная H2CO3P2O5 – Оксид фосфора (V)– фосфорнаяH3PO4
SiO2 – Оксид кремния (IV)– кремниевая H2SiO3
SO2 – Оксид серы (IV) – сернистая H2SO3
Слайд 5
Проверка выполнения домашнего задания
№4 стр. 73
Только четыре оксида
соответствуют кислотам, перечисленным в параграфе:
N2O3 – Оксид азота (III)
– азотистая HNO2N2O5 – Оксид азота (V) – азотная HNO3
SO3 – Оксид серы (VI) – серная H2SO4
CO2 – Оксид углерода (IV) – угольная H2CO3
Слайд 6
Проверка знаний, полученных на предыдущем уроке
Какие вещества называются
основаниями?
Что такое щелочи?
Какие вещества называются кислотами?
Чем отличается гидроксид металла
от гидроксида неметалла?Назовите при помощи какой качественной реакции можно распознать щелочь?
Как можно распознать кислоту?
В двух склянках даны бесцветные растворы, один – раствор кислоты, другой – щелочи. Как распознать, где какое вещество находится? (составьте инструкцию)
Слайд 7
Закрепление знаний, полученных на предыдущем уроке
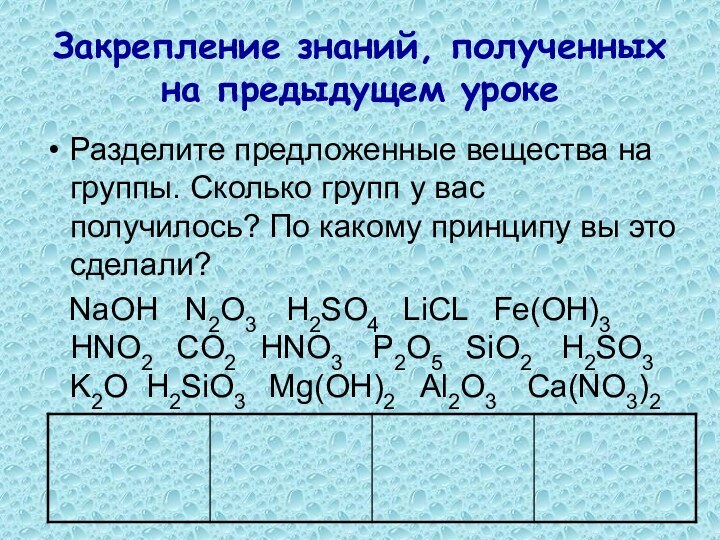
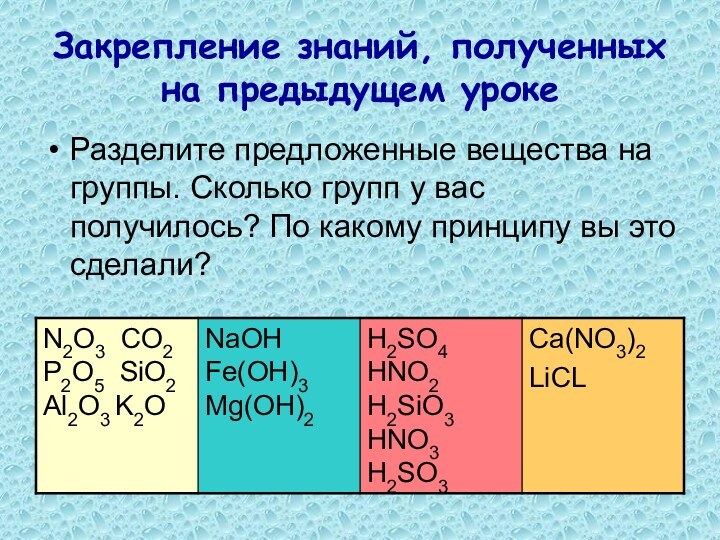
Разделите предложенные вещества
на группы. Сколько групп у вас получилось? По какому
принципу вы это сделали?NaOH N2O3 H2SO4 LiCL Fe(OH)3 HNO2 CO2 HNO3 P2O5 SiO2 H2SO3 K2O H2SiO3 Mg(OH)2 Al2O3 Ca(NO3)2