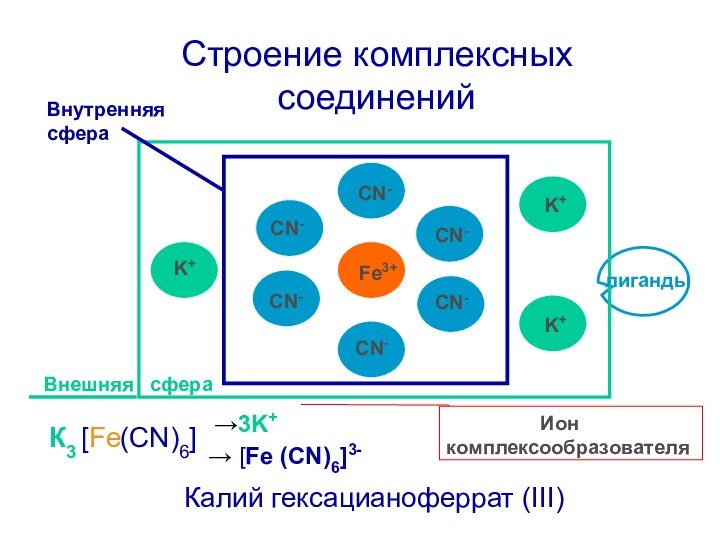
Ион комплексообразователя
лиганды
Внутренняя сфера
Внешняя
сфера[ (CN)6]
К3
Fe
→3K+
→ [Fe (CN)6]3-
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть



![Презентация Комплексные соединения Номенклатура комплексных соединенийК[Co(CN)(CO)2(NO)] -калийдикарбонилнитрозилцианокобальт (0)1) NH4SCN+Cr(SCN)3+2NH3NH4[Cr(SCN)4(NH3)2] аммоний диаммин тетратиоцианатохромат(III) 2) CoCl3+ 5NH3 [CoCl(NH3)5]Cl2пентаамминкобальт(III)хлорохлорид3)](/img/tmb/13/1202772/a9c69b35ae479f4343571963b78d01d1-720x.jpg)
![Презентация Комплексные соединения 2. По принадлежности к определённому классу соединенийкомплексныедиамминсеребро(I) гидрооксидкислотыоснования солиH[AuCl4][Ag(NH3)2]OHK2[HgI4] водород тетрахлороаурат(III) калий тетраиодомеркурат(II)Классификация](/img/tmb/13/1202772/f403af9122e3d5694e1904f42b5564b5-720x.jpg)
![Презентация Комплексные соединения 3. По природе лигандовАммиакаты[Ni(NH3)6]Cl2 Аквакомплексы[Co(H2O)6]SO4 АцидокомплексыK[Cu(CN)2]Карбонилы [Fe(CO)5]Гидроксокомплексы K3[Al(OH)6 ]ЦианидныеK4[Со(CN)6]Карбонатные[Fe(CO3)(NH3)]ClРазнолигандные[CoI(NH3)5]Cl2NH4[Cr(SCN)4(NH3)2]Классификация комплексных соединений по разным признакам](/img/tmb/13/1202772/6c5b57430f706d80cd1e788aac6cf8bb-720x.jpg)

![Презентация Комплексные соединения Классификация комплексных соединений по разным признакам4.2. По наличию или отсутствию цикловПростыеFe4[Fe(CN)6]3берлинская лазурьFe3[Fe(CN)6]2турнбулева](/img/tmb/13/1202772/34662ec6d939658e06d022481017ed2c-720x.jpg)
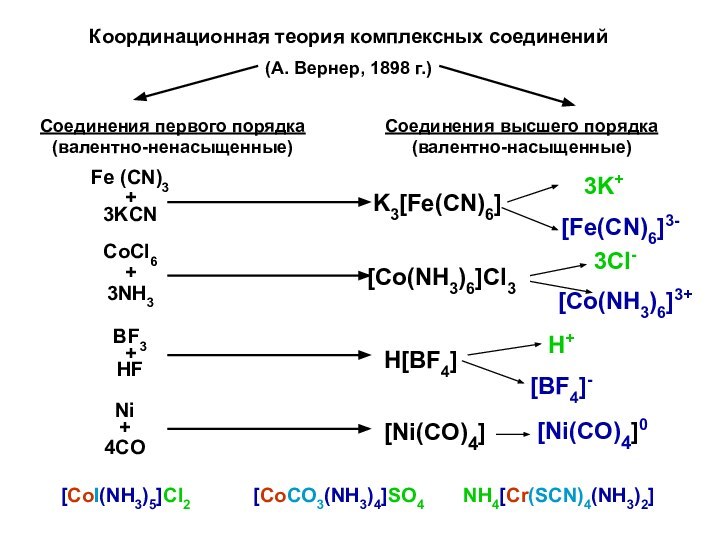
[ (CN)6]
К3
Fe
→3K+
→ [Fe (CN)6]3-
H+
[BF4]-
[Ni(CO)4]0
[CoI(NH3)5]Cl2
[CoCO3(NH3)4]SO4
NH4[Cr(SCN)4(NH3)2]
Монодентантные лиганды – координационная ёмкость =1 Cl-, Br-, I-, CN-, NH3 и др.
Бидентантные лиганды – координационная ёмкость =2
SO42-, CO32-, C2O42- и др. К3[Fe(C2O4)3]
Полидентантные лиганды – лиганды с координационной
ёмкостью 3,4,6.
2. В названии комплекса сначала перечисляют лиганды (по первым буквам русского алфавита), затем центральный атом.
3. Нейтральные лиганды называют без изменения; к названиям отрицательно заряженных лигандов прибавляют окончание «о».
4. Если одинаковых лигандов в комплексе несколько, перед их названием употребляют соответствующее греческое числительное.
5. Название комплексообразователя зависит от заряда комплекса.
5.1. Для нейтрального и катионного – именительный падеж (рус. яз.)
5.2. Для анионного комплекса - латинский язык (суффикс «ат»)
хлорид
пентааква
хлоро
хром(III)
хлорид
моногидрат
[CrCl2(H2O)4]Cl⋅ 2H2O
хром(III)
дигидрат
хлорид
тетрааква
дихлоро
[Co(CN)2(NH3)4]Cl
Тетраамминдициано
-кобальт (III)
хлорид
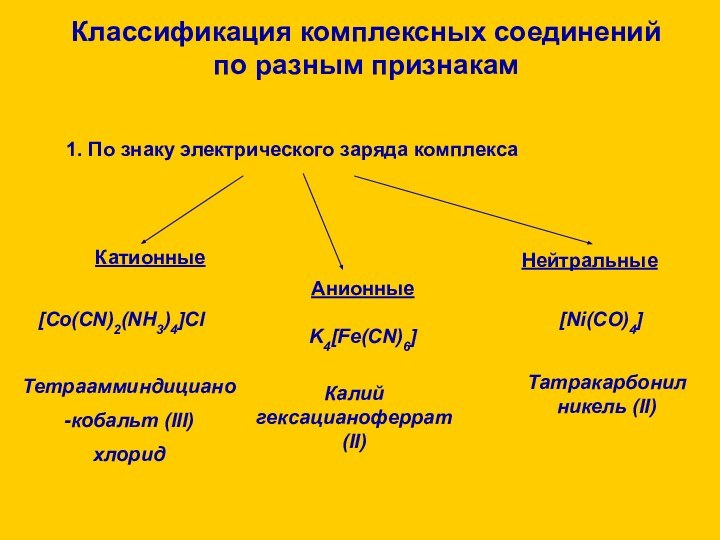
Анионные
K4[Fe(CN)6]
Калий гексацианоферрат (II)
Нейтральные
[Ni(CO)4]
Татракарбонил никель (II)
Катионные
μ - гидроксо-
бис-
[пентаамминхром (III)]
хлорид
Изо- и гетерополикислоты
H2Cr2O7
H2[O3Cr — O — CrO3]
водород
μ-оксо-бис-
[триоксохромат(VI)]
Н2Si2O5
H2[O2Si−O−SiO2]
водород
μ-оксо-бис-
[диоксосиликат(IV)]
фосфорномолибденовая
H3PO4 ∙ 12MoO3 ∙ nH2O
фосфорновольфрамовая H3PO4 ∙ 12WO3 ∙ nH2O
кремниймолибденовая H4SiO4 ∙ 12MoO3 ∙ nH2O
кремнийвольфрамовая H4SiO4 ∙ 12WO3 ∙ nH2O
боровольфрамовая H3BO3 ∙ 12WO3 ∙ nH2O